一种从废弃SCR催化剂(主要含78%TiO2、V2O5及SiO2、Al2O3等)中回收钛、钒的工艺流程如图所示:

(1)Ti在周期表中的位置是_____________ ,价层电子排布式是________________ 。
(2)已知V2O5的化学性质与氧化铝相似,则“碱浸”过程中发生反应的离子方程式Al2O3+ 2OH-= 2AlO +H2O、
+H2O、__________ 、___________ 。
(3)沉淀X的主要成分是H2SiO3、_________ (填化学式)。
(4)在焙烧NH4VO3时,气体产物经过与_______ (填化学式)反应后,可以在生产流程中循环利用。
(5)反型钙钛矿电池使用具有光催化活性的TiO2(通过氮掺杂生成TiO2-aNb,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
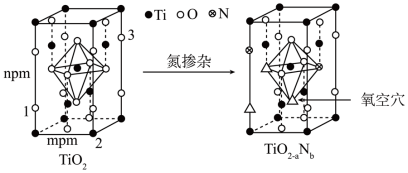
已知原子1、2的分数坐标为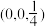 和
和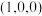 ,则原子3的坐标分别为
,则原子3的坐标分别为______ ,设阿伏加德罗常数的值为NA,TiO2的密度为_______ g·cm-3(列出计算式)。TiO2-aNb晶体中a=_______ 。

(1)Ti在周期表中的位置是
(2)已知V2O5的化学性质与氧化铝相似,则“碱浸”过程中发生反应的离子方程式Al2O3+ 2OH-= 2AlO
 +H2O、
+H2O、(3)沉淀X的主要成分是H2SiO3、
(4)在焙烧NH4VO3时,气体产物经过与
(5)反型钙钛矿电池使用具有光催化活性的TiO2(通过氮掺杂生成TiO2-aNb,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。

已知原子1、2的分数坐标为
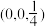 和
和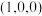 ,则原子3的坐标分别为
,则原子3的坐标分别为
更新时间:2022-09-30 06:15:47
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】根据 A-I 在周期表中的位置,用元素符号或化学式回答下列问题。
(1)表中元素,化学性质最不活泼的是_____ ,只有负价而无正价的是_____ ,氧化性最强的单质是____ ;
(2)最高价氧化物的水化物碱性最强的是_____ ,酸性最强的是_____ ,呈两性的是_____ ;
(3)A 分别与 D、E、F、G、H 形成的化合物中,最稳定的是_____ ;
(4)在 B、C、D、E、F、G、H 中,原子半径最大的是_____ ;
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外 M 电子层与 K 电子层上的电子数相等,甲、乙两元素相比较,金属性较强的是_______ 可以验证该结论的实验是_ 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物碱性最强的是
(3)A 分别与 D、E、F、G、H 形成的化合物中,最稳定的是
(4)在 B、C、D、E、F、G、H 中,原子半径最大的是
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外 M 电子层与 K 电子层上的电子数相等,甲、乙两元素相比较,金属性较强的是
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】下表是元素周期表的一部分:
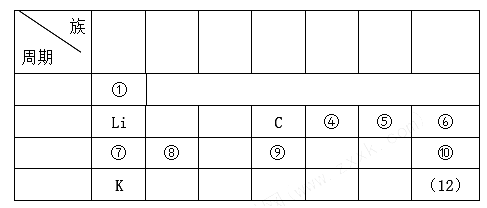
(1)表中元素______ 的非金属性最强(填写元素符号,下同);元素______ 的单质室温下呈液态,它的原子序数是_________ 。
(2)表中元素⑤和⑦、①和⑤均可以组成原子比例为1:1的物质,这两种物质内所含有相同的化学键是__________ (填写“离子键”、“极性共价键”或“非极性共价键”)。
(3)表中元素⑥⑩(12)氢化物的稳定性由大到小的顺序为:_________ (填写化学式,下同)。
(4)表中有一种元素的单质可作为半导体材料,它在元素周期表中的位置是_____ 。
(5)用电子式表示表中⑧⑩两元素形成化合物的过程__________________ 。

(1)表中元素
(2)表中元素⑤和⑦、①和⑤均可以组成原子比例为1:1的物质,这两种物质内所含有相同的化学键是
(3)表中元素⑥⑩(12)氢化物的稳定性由大到小的顺序为:
(4)表中有一种元素的单质可作为半导体材料,它在元素周期表中的位置是
(5)用电子式表示表中⑧⑩两元素形成化合物的过程
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】已知X、Y、Z、W为四种短周期元素,其原子序数依次增大,且由这些元素所组成的单质在常温下均呈气态。X、Y、W处于不同周期,且在一定条件下其单质能发生反应:X2+Y2→甲,X2+W2→乙,甲、乙可化合生成离子化合物丙。试回答下列问题:
(1)W元素在周期表中的位置是_________ ;甲的空间构型为___________ 。
(2)丙的水溶液呈酸性,用离子方程式表示其原因____________________________ 。
(3)X、Z可组成四原子化合物丁,丁是一种二元弱酸,写出丁在水中的电离方程式_________________ ;X、Y组成的液态化合物Y2X416克与足量丁反应生成Y2和液态水,放出Q kJ的热量,请写出该反应的热化学方程式___________
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则负极的电极反应式为____________________ 。
(1)W元素在周期表中的位置是
(2)丙的水溶液呈酸性,用离子方程式表示其原因
(3)X、Z可组成四原子化合物丁,丁是一种二元弱酸,写出丁在水中的电离方程式
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则负极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】利用某油脂厂制硬化油废弃的镍催化剂(主要含有Ni,还含有Fe、Cu)为原料制备电池材料 及
及 的工艺流程如下:
的工艺流程如下:

已知:①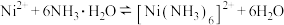
②制备过程中,降低 沉淀速率,可以避免沉淀团聚,提升电池性能
沉淀速率,可以避免沉淀团聚,提升电池性能
③25℃时相关物质的 见下表:
见下表:
回答下列问题:
(1)反应器I中加入NaOH溶液的主要目的是___________ 。
(2)25℃时加入 调节溶液的pH,则pH的理论最小值为
调节溶液的pH,则pH的理论最小值为___________ (溶液中离子浓度 时,认为该离子沉淀完全)。滤渣II中还含有少量FeOOH,写出该环境下,由
时,认为该离子沉淀完全)。滤渣II中还含有少量FeOOH,写出该环境下,由 生成FeOOH的离子方程式
生成FeOOH的离子方程式___________ 。
(3)反应器IV中,需先加氨水,再加过量NaOH,先加氨水的目的是___________ 。
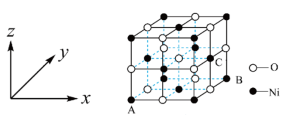
(4)镍的氧化物也常用作催化剂,NiO的晶胞结构如图所示,该晶体中Ni周围与其等距离且最近的Ni有___________ 个,原子坐标参数表示晶胞内部各原子的相对位置,若该晶胞中原子坐标参数A为 ,B为
,B为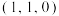 ,则C的原子坐标参数为
,则C的原子坐标参数为___________ 。
 及
及 的工艺流程如下:
的工艺流程如下:
已知:①
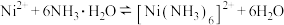
②制备过程中,降低
 沉淀速率,可以避免沉淀团聚,提升电池性能
沉淀速率,可以避免沉淀团聚,提升电池性能③25℃时相关物质的
 见下表:
见下表:| 物质 |  |  |  |  |
 | 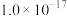 | 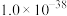 | 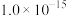 |  |
(1)反应器I中加入NaOH溶液的主要目的是
(2)25℃时加入
 调节溶液的pH,则pH的理论最小值为
调节溶液的pH,则pH的理论最小值为 时,认为该离子沉淀完全)。滤渣II中还含有少量FeOOH,写出该环境下,由
时,认为该离子沉淀完全)。滤渣II中还含有少量FeOOH,写出该环境下,由 生成FeOOH的离子方程式
生成FeOOH的离子方程式(3)反应器IV中,需先加氨水,再加过量NaOH,先加氨水的目的是
(4)镍的氧化物也常用作催化剂,NiO的晶胞结构如图所示,该晶体中Ni周围与其等距离且最近的Ni有
 ,B为
,B为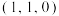 ,则C的原子坐标参数为
,则C的原子坐标参数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】铟(In)是制造半导体、电光源等的重要原料,广泛用于航空航天、光电信息、太阳能电池等领域。从铜冶炼过程中产生的铟砷烟灰(主要含有ZnO、PbO、Fe2O3、In2O3、As2O3、In2S3、SiO2)中提取铟的流程如图所示:
②“萃取”过程中萃取剂可用 H2A2表示,其在酸性溶液中可萃取三价金属离子。
③ln3+与Al3+相似,易水解。
请回答下列问题:
(1)滤渣的主要成分除SiO2外还有___________ (填化学式);“氧化酸浸”过程中,As2O3中的砷元素被氧化为最高价的含氧酸,写出此反应的离子方程式:___________ 。
(2)“还原铁”操作的目的是___________ 。
(3)萃取是化学实验中常用的分离方法,其操作过程为:检查分液漏斗是否漏液→加萃取剂和萃取液→振荡→___________ →静置→……
(4)“萃取”过程的离子方程式In3++3H2A2=In(HA2)3+3H+, 实验证明,在有机相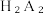 体积分数为55%、温度为25°C时,水相的 pH 对 ln3+萃取率的影响如图所示。结果表明,pH>2.1时, In³+ 萃取率快速下降,其原因是
体积分数为55%、温度为25°C时,水相的 pH 对 ln3+萃取率的影响如图所示。结果表明,pH>2.1时, In³+ 萃取率快速下降,其原因是___________ 。___________ g(用含a 的分数表示);“置换”后所得浊液需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已经洗涤干净的具体操作为 ___________ 。
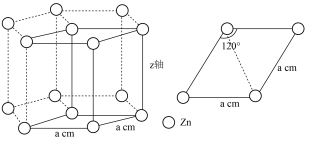
(6)锌是一种重要的金属,晶体结构属于六方晶系,其晶体结构、晶胞沿z轴的投影图如图所示,设Zn原子半径为r1nm,,晶胞边长为a cm,高为 h cm,则该晶体的空间利用率为___________ (列出计算式即可)。

②“萃取”过程中萃取剂可用 H2A2表示,其在酸性溶液中可萃取三价金属离子。
③ln3+与Al3+相似,易水解。
请回答下列问题:
(1)滤渣的主要成分除SiO2外还有
(2)“还原铁”操作的目的是
(3)萃取是化学实验中常用的分离方法,其操作过程为:检查分液漏斗是否漏液→加萃取剂和萃取液→振荡→
(4)“萃取”过程的离子方程式In3++3H2A2=In(HA2)3+3H+, 实验证明,在有机相
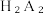 体积分数为55%、温度为25°C时,水相的 pH 对 ln3+萃取率的影响如图所示。结果表明,pH>2.1时, In³+ 萃取率快速下降,其原因是
体积分数为55%、温度为25°C时,水相的 pH 对 ln3+萃取率的影响如图所示。结果表明,pH>2.1时, In³+ 萃取率快速下降,其原因是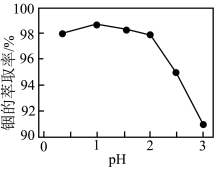
(6)锌是一种重要的金属,晶体结构属于六方晶系,其晶体结构、晶胞沿z轴的投影图如图所示,设Zn原子半径为r1nm,,晶胞边长为a cm,高为 h cm,则该晶体的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】铜是人类最早发现的金属之一,铜及其化合物在生活和生产中有着广泛的应用。根据信息回答下列问题:
(1)基态铜原子的外围电子排布式为___________ ,单质铜是由___________ 键形成的晶体。
(2)与铜同周期,N能层电子数与铜相同,熔点最低的金属是___________ 。
(3)农药波尔多液的有效杀菌成分是Cu2(OH)2SO4(碱式硫酸铜),Cu2(OH)2SO4中非金属元素电负性由小到大的顺序是___________ 。
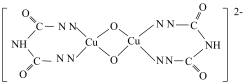
(4)氨缩脲与胆矾溶液反应得到如下图所示的离子,该离子中含配位键,还含有的化学键有___________ (填字母)。
a.极性键 b.非极性键 c. σ键 d.π键
氨缩脲( )分子中σ键与π键的数目之比为
)分子中σ键与π键的数目之比为___________ 。
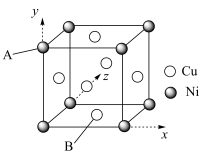
(5)白铜(铜镍合金)的立方晶胞结构如图所示,其中原子A位于顶点,原子B位于面心。则该晶体中铜原子和镍原子的个数比为___________ 。
(1)基态铜原子的外围电子排布式为
(2)与铜同周期,N能层电子数与铜相同,熔点最低的金属是
(3)农药波尔多液的有效杀菌成分是Cu2(OH)2SO4(碱式硫酸铜),Cu2(OH)2SO4中非金属元素电负性由小到大的顺序是
(4)氨缩脲与胆矾溶液反应得到如下图所示的离子,该离子中含配位键,还含有的化学键有

a.极性键 b.非极性键 c. σ键 d.π键
氨缩脲(
 )分子中σ键与π键的数目之比为
)分子中σ键与π键的数目之比为(5)白铜(铜镍合金)的立方晶胞结构如图所示,其中原子A位于顶点,原子B位于面心。则该晶体中铜原子和镍原子的个数比为

您最近一年使用:0次
【推荐1】Ⅰ.硒(Se)是一种重要的化学元素,在医药、农业、能源和电子等领域有广泛应用。
(1)以下不能用元素周期律解释的是___________。
(2)硒化铅可用作玻璃和陶瓷的着色剂,其晶胞结构如图所示:___________ 。
A.离子键 B.共价键
②晶体中每个Se周围与其最近的,且距离相等的Se有___________ 个。
Ⅱ.工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、Ag2Se等)回收Se。
② 室温下Ksp(Ag2SO4)=10−5;Ksp(AgCl)=10−9.75。
(3)“焙烧”前,将阳极泥中大块颗粒粉碎的目的是___________ 。
(4)“烟气”中含有SO2和SeO2,被水吸收发生反应,SO2与和SeO2的物质的量之比为___________ ,SeO2体现了___________ 。
A.氧化性 B.还原性
(5)“提纯”步骤中用到真空蒸馏工艺,真空的作用是___________ 、___________ 。
(6)小组同学测定某CuSO4∙xH2O晶体样品热分解的质量变化情况(如图所示),258℃失去全部结晶水,x=___________ 。(结果保留2位小数)___________ 。
Ⅲ.亚硒酸(H2SeO3)是主要的含硒化合物,是二元弱酸。常温下,H2SeO3溶液中某些微粒的物质的量分数与pH的关系如图所示:
(9)向滴有酚酞的H2SeO3溶液中加入氨水,当溶液由粉红色变为红色时,反应的离子方程式为___________ 。
(1)以下不能用元素周期律解释的是___________。
| A.键的极性:H−Se < H−Br | B.原子半径:Se > Br |
| C.稳定性:H2Se < HBr | D.酸性:H2SeO3 < HBrO4 |
(2)硒化铅可用作玻璃和陶瓷的着色剂,其晶胞结构如图所示:
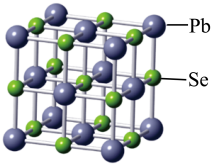
A.离子键 B.共价键
②晶体中每个Se周围与其最近的,且距离相等的Se有
Ⅱ.工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、Ag2Se等)回收Se。
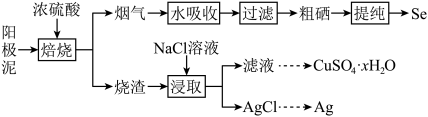
② 室温下Ksp(Ag2SO4)=10−5;Ksp(AgCl)=10−9.75。
(3)“焙烧”前,将阳极泥中大块颗粒粉碎的目的是
(4)“烟气”中含有SO2和SeO2,被水吸收发生反应,SO2与和SeO2的物质的量之比为
A.氧化性 B.还原性
(5)“提纯”步骤中用到真空蒸馏工艺,真空的作用是
(6)小组同学测定某CuSO4∙xH2O晶体样品热分解的质量变化情况(如图所示),258℃失去全部结晶水,x=
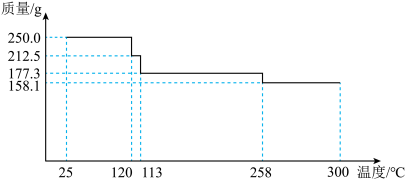
Ⅲ.亚硒酸(H2SeO3)是主要的含硒化合物,是二元弱酸。常温下,H2SeO3溶液中某些微粒的物质的量分数与pH的关系如图所示:
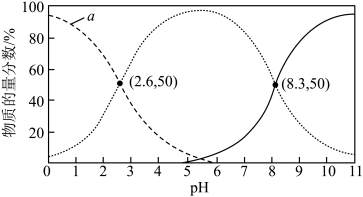
A.曲线a表示的是SeO 物质的量分数随pH变化 物质的量分数随pH变化 |
| B.Ka1=10−5.5 |
C.pH=3时, =100.4 =100.4 |
D.向H2SeO3溶液中逐滴加入NaOH溶液,pH=8.3时溶液中存在:2c(Na+)=3[c(HSeO )+ c(SeO )+ c(SeO )+ c(H2SeO3)] )+ c(H2SeO3)] |
(9)向滴有酚酞的H2SeO3溶液中加入氨水,当溶液由粉红色变为红色时,反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】现有含淀粉、NaCl、Na2SO4、CaCl2的混合溶液,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下:
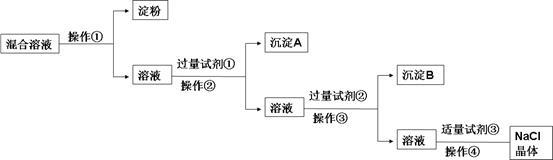
(1)操作①是利用胶体不能通过_____________ 而把淀粉胶体和溶液进行分离。
(2)写出上述实验过程中所用试剂的化学式:
试剂①___________________ ;试剂③_____________________ 。
(3)判断试剂①已过量的操作是:__________________ 。
(4)控制试剂③适量的方法是:__________________ 。
(5)试剂②的作用(用化学方程式表示):__________________ 。

(1)操作①是利用胶体不能通过
(2)写出上述实验过程中所用试剂的化学式:
试剂①
(3)判断试剂①已过量的操作是:
(4)控制试剂③适量的方法是:
(5)试剂②的作用(用化学方程式表示):
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】一种由海绵铜( 和少量
和少量 等)为原料制备
等)为原料制备 的工艺流程如下:
的工艺流程如下:
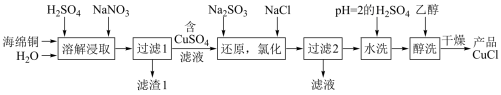
已知:① 为白色固体,难溶于水和乙醇,可溶于氯离子浓度较大的溶液中。
为白色固体,难溶于水和乙醇,可溶于氯离子浓度较大的溶液中。
② 有水存在时在空气中易被氧化,在酸性条件下较稳定。
有水存在时在空气中易被氧化,在酸性条件下较稳定。
(1)为减少“溶解浸取”时产生 等有害气体,选用约为
等有害气体,选用约为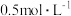 的硫酸,过程中几乎无气体产生。若硫酸浓度过大,
的硫酸,过程中几乎无气体产生。若硫酸浓度过大, 的用量
的用量_______ (填“增大”“减小”或“不变)。
(2)“还原,氯化”时,溶液 及
及 的用量对
的用量对 产率的影响如图1、图2所示:
产率的影响如图1、图2所示:


① 与
与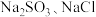 在溶液中反应生成
在溶液中反应生成 的离子方程式为
的离子方程式为_______ 。
②当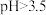 时,
时, 产率减小,其原因是
产率减小,其原因是_______ 。
③随着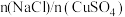 增大
增大 产率增加,但增加到一定程度后
产率增加,但增加到一定程度后 产率减少,其原因是
产率减少,其原因是_______ 。
(3)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为 。
。 被氧化为
被氧化为 的化学方程式为
的化学方程式为_______ 。
(4)国家标准规定合格 产品的主要质量指标为
产品的主要质量指标为 的质量分数大于96.50%。准确称取所制备的
的质量分数大于96.50%。准确称取所制备的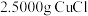 样品置于过量的
样品置于过量的 溶液中,待样品完全溶解后,用容量瓶配成
溶液中,待样品完全溶解后,用容量瓶配成 溶液,取出
溶液,取出 ,用
,用 的
的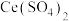 溶液滴定到终点,反应中
溶液滴定到终点,反应中 被还原为
被还原为 ,消耗
,消耗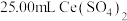 溶液。通过计算说明上述样品中
溶液。通过计算说明上述样品中 的质量分数是否符合标准
的质量分数是否符合标准_______ 。
 和少量
和少量 等)为原料制备
等)为原料制备 的工艺流程如下:
的工艺流程如下:
已知:①
 为白色固体,难溶于水和乙醇,可溶于氯离子浓度较大的溶液中。
为白色固体,难溶于水和乙醇,可溶于氯离子浓度较大的溶液中。②
 有水存在时在空气中易被氧化,在酸性条件下较稳定。
有水存在时在空气中易被氧化,在酸性条件下较稳定。(1)为减少“溶解浸取”时产生
 等有害气体,选用约为
等有害气体,选用约为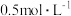 的硫酸,过程中几乎无气体产生。若硫酸浓度过大,
的硫酸,过程中几乎无气体产生。若硫酸浓度过大, 的用量
的用量(2)“还原,氯化”时,溶液
 及
及 的用量对
的用量对 产率的影响如图1、图2所示:
产率的影响如图1、图2所示:

①
 与
与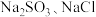 在溶液中反应生成
在溶液中反应生成 的离子方程式为
的离子方程式为②当
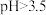 时,
时, 产率减小,其原因是
产率减小,其原因是③随着
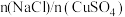 增大
增大 产率增加,但增加到一定程度后
产率增加,但增加到一定程度后 产率减少,其原因是
产率减少,其原因是(3)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为
 。
。 被氧化为
被氧化为 的化学方程式为
的化学方程式为(4)国家标准规定合格
 产品的主要质量指标为
产品的主要质量指标为 的质量分数大于96.50%。准确称取所制备的
的质量分数大于96.50%。准确称取所制备的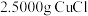 样品置于过量的
样品置于过量的 溶液中,待样品完全溶解后,用容量瓶配成
溶液中,待样品完全溶解后,用容量瓶配成 溶液,取出
溶液,取出 ,用
,用 的
的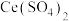 溶液滴定到终点,反应中
溶液滴定到终点,反应中 被还原为
被还原为 ,消耗
,消耗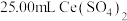 溶液。通过计算说明上述样品中
溶液。通过计算说明上述样品中 的质量分数是否符合标准
的质量分数是否符合标准
您最近一年使用:0次



