Ⅰ. X元素在第3周期中电负性最大,Y、Z元素同主族且位置相邻,Y原子的最外层电子排布为 nsnnpn+2。请填写下列空白。
(1)写出X元素M层的电子排布式_______ 。
(2)XY2是一种高效安全的消毒剂,熔点 -59.5 ℃,沸点10 ℃,构成该晶体的微粒之间的作用力是_______ 。
(3)ZX2 常用于有机合成。ZX2 分子的空间构型是_______ 。写出 ZX2 的等电子体(分子离子各一个)_______ 、_______ 。
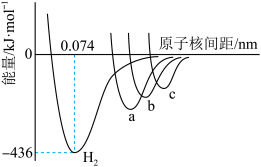
(4)图中四条曲线分别表示H2、Cl2、Br2、I2分子的形成过程中能量随原子核间距的变化关系,其中表示Cl2 的是曲线_______ (填“a”、“b”或“c”),理由是_______ 。
Ⅱ. 钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。
(5)根据下图所示晶胞结构,推算晶体中Y、Cu、Ba和O原子个数比,确定其化学式为_______ ;
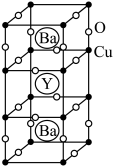
(6)根据(5)所推出的化合物的组成,(该化合物中各元素的化合价为Y +3、Ba +2),计算该物质中+2价和+3价的Cu离子个数比为_______ 。
(1)写出X元素M层的电子排布式
(2)XY2是一种高效安全的消毒剂,熔点 -59.5 ℃,沸点10 ℃,构成该晶体的微粒之间的作用力是
(3)ZX2 常用于有机合成。ZX2 分子的空间构型是
(4)图中四条曲线分别表示H2、Cl2、Br2、I2分子的形成过程中能量随原子核间距的变化关系,其中表示Cl2 的是曲线

Ⅱ. 钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。
(5)根据下图所示晶胞结构,推算晶体中Y、Cu、Ba和O原子个数比,确定其化学式为

(6)根据(5)所推出的化合物的组成,(该化合物中各元素的化合价为Y +3、Ba +2),计算该物质中+2价和+3价的Cu离子个数比为
更新时间:2022-10-03 19:58:03
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】磷酸亚铁锂 可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,广泛应用于新能源汽车,可采用
可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,广泛应用于新能源汽车,可采用 、
、 、
、 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:
(1)基态Fe原子的价电子排布式为___________ ,基态P原子中未成对电子数为___________ ,N、O和P电负性由大到小的顺序是___________ 。
(2)下列Li原子轨道表示式表示的状态中,能量最高的是_______ (填标号)。
A. B.
B.
C. D.
D.
Li的第一电离能小于相邻元素Be的第一电离能,原因是_______ 。
(3)苯胺( )的晶体类型是
)的晶体类型是___________ , 苯胺中含有的
苯胺中含有的 键数目为
键数目为___________ 。苯胺与甲苯( )的相对分子质量相近,但苯胺的熔点沸点(184.4℃)高于甲苯的沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点沸点(184.4℃)高于甲苯的沸点(110.6℃),原因是_______ 。
(4)钴酸锂( )的一种晶胞如图所示(仅标出Li,Co与O未标出),晶胞中含有
)的一种晶胞如图所示(仅标出Li,Co与O未标出),晶胞中含有 的个数为
的个数为___________ 。晶胞边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该钴酸锂晶体的密度可表示为
,该钴酸锂晶体的密度可表示为___________  (用含有
(用含有 的代数式表示)。
的代数式表示)。

 可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,广泛应用于新能源汽车,可采用
可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,广泛应用于新能源汽车,可采用 、
、 、
、 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:(1)基态Fe原子的价电子排布式为
(2)下列Li原子轨道表示式表示的状态中,能量最高的是
A.
 B.
B.
C.
 D.
D.
Li的第一电离能小于相邻元素Be的第一电离能,原因是
(3)苯胺(
 )的晶体类型是
)的晶体类型是 苯胺中含有的
苯胺中含有的 键数目为
键数目为 )的相对分子质量相近,但苯胺的熔点沸点(184.4℃)高于甲苯的沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点沸点(184.4℃)高于甲苯的沸点(110.6℃),原因是(4)钴酸锂(
 )的一种晶胞如图所示(仅标出Li,Co与O未标出),晶胞中含有
)的一种晶胞如图所示(仅标出Li,Co与O未标出),晶胞中含有 的个数为
的个数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该钴酸锂晶体的密度可表示为
,该钴酸锂晶体的密度可表示为 (用含有
(用含有 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】钛的化合物如TiO2、Ti(NO3)4、TiCl4、Ti(BH4)2等均有着广泛用途。
(1)写出Ti的基态原子的外围电子排布式_____ 。
(2)TiCl4熔点是﹣25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于_____ 晶体;BH4﹣中B原子的杂化类型为_____ 。
(3)在 TiO2催化作用下,可将CN﹣氧化成CNO﹣,进而得到N2。与CNO﹣互为等电子体的分子化学式为(只写一种)________ 。
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2•H2O(绿色)。绿色晶体中配体是_______ 。
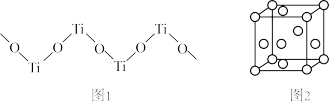
(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为______ 。
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为ρg•cm﹣3,阿伏伽德罗常数为NA,则该晶胞的边长为___ cm。
(1)写出Ti的基态原子的外围电子排布式
(2)TiCl4熔点是﹣25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于
(3)在 TiO2催化作用下,可将CN﹣氧化成CNO﹣,进而得到N2。与CNO﹣互为等电子体的分子化学式为(只写一种)
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2•H2O(绿色)。绿色晶体中配体是
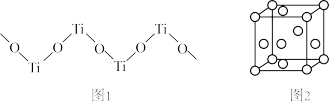
(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为ρg•cm﹣3,阿伏伽德罗常数为NA,则该晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硅是地壳中储量仅次于氧的元素,在自然界中主要以 SiO2和硅酸盐的形式存在。
(1)基态硅原子的价电子排布式为______ ,核外电子共有___________ 种运动状态。
(2)硅、金刚石和碳化硅晶体的熔点从高到低依次是_______ ,判断的依据为:___________ 。
(3)晶态SiO2的晶胞如图。
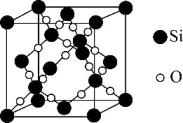
①硅原子的杂化方式为_________ ,氧原子的配位数为___________ 。
②已知 SiO2晶胞的棱长均为 apm,则 SiO2晶体的密度ρ=________ g·cm-3(列出计算式)。
(4)硅元素最高价氧化物对应的水化物为原硅酸(H4SiO4)。
资料:原硅酸(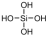 )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
①原硅酸钠(Na4SiO4)溶液吸收空气中的 CO2会生成 H4SiO4,写出生成 H4SiO4的离子方程式:___________ 。
②从结构的角度解释 H4SiO4脱水后溶解度降低的原因:_________________ 。
(1)基态硅原子的价电子排布式为
(2)硅、金刚石和碳化硅晶体的熔点从高到低依次是
(3)晶态SiO2的晶胞如图。

①硅原子的杂化方式为
②已知 SiO2晶胞的棱长均为 apm,则 SiO2晶体的密度ρ=
(4)硅元素最高价氧化物对应的水化物为原硅酸(H4SiO4)。
资料:原硅酸(
 )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。 ①原硅酸钠(Na4SiO4)溶液吸收空气中的 CO2会生成 H4SiO4,写出生成 H4SiO4的离子方程式:
②从结构的角度解释 H4SiO4脱水后溶解度降低的原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】红蓝宝石、祖母绿、金绿猫眼、钻石为举世公认的珍贵宝石。
(1)红宝石是刚玉的一种,主要成分为氧化铝( ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为___________ 。
(2)祖母绿主要成分的化学式为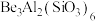 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)___________ I(Al)。Be和Al一样,能与NaOH溶液反应,请简单说明判断依据:___________ 。
(3)金绿猫眼主要成分的化学式为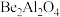 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为___________ 。 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式:
的结构式:___________ 。 分子中铝的杂化类型
分子中铝的杂化类型___________ 。
(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为___________ 。金刚石晶胞结构如图所示,与晶胞面心处碳原子距离最近且等距离的碳原子数为___________ 。
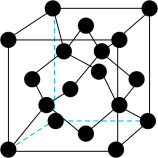
(5)该晶胞空间利用率___________ (用含的π式子表示)。
(1)红宝石是刚玉的一种,主要成分为氧化铝(
 ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为(2)祖母绿主要成分的化学式为
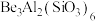 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)(3)金绿猫眼主要成分的化学式为
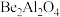 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式:
的结构式: 分子中铝的杂化类型
分子中铝的杂化类型(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为

(5)该晶胞空间利用率
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素A、B、C、D的原子序数依次增大,基态A原子核外电子占据3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,C的双原子单质分子中σ键和π键数目之比为1∶2,D的最高化合价和最低化合价代数和等于4。
(1)基态B原子的价电子排布图为_______ ;基态D原子核外电子占据最高能级的电子云轮廓图为_______ 形。
(2)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp2杂化、空间结构为平面三角形的是_______ (填分子式,下同),属于极性分子的是_______ ,键角由大到小的顺序为_______ 。
(3)(DC)4为热色性固体,且有色温效应,其颜色在低于30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色,(DC)4属于_______ 晶体,在淡黄色→橙黄色→深红色的转化中,破坏的作用力是_______ ;在常压下,(DC)4高于130℃分解为相应的单质,这一变化中破坏的作用力是_______ 。
(4)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子)。已知:该晶体边长为anm,NA代表阿伏加德罗常数的值。
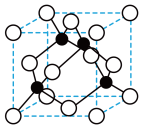
①该晶体的化学式为_______ 。
②该晶体的密度为_______ g/cm3。
(1)基态B原子的价电子排布图为
(2)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp2杂化、空间结构为平面三角形的是
(3)(DC)4为热色性固体,且有色温效应,其颜色在低于30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色,(DC)4属于
(4)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子)。已知:该晶体边长为anm,NA代表阿伏加德罗常数的值。

①该晶体的化学式为
②该晶体的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子和基态E原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)E的元素名称为_______ 。它位于元素周期表的_______ 区。
(2)元素A、B、C中,电负性最大的是_______ (填元素符号,下同),元素B、C、D第一电离能由大到小的顺序为_______ 。
(3)与同族其他元素X形成的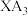 相比,
相比, 易液化的原因是
易液化的原因是_______ ; 分子中键角
分子中键角_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4) 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ , 离子的空间结构为
离子的空间结构为_______ 。
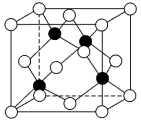
(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为_______  (用
(用 表示阿伏加德罗常数)。(已知:
表示阿伏加德罗常数)。(已知: )
)
(1)E的元素名称为
(2)元素A、B、C中,电负性最大的是
(3)与同族其他元素X形成的
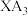 相比,
相比, 易液化的原因是
易液化的原因是 分子中键角
分子中键角 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 离子的空间结构为
离子的空间结构为(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为
 (用
(用 表示阿伏加德罗常数)。(已知:
表示阿伏加德罗常数)。(已知: )
)
您最近一年使用:0次
【推荐1】按要求完成下列填空:
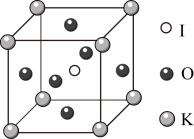
(1)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为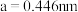 ,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。与K紧邻的I个数为
,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。与K紧邻的I个数为_______ 。
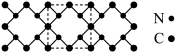
(2)某晶体结构如图,其硬度超过金刚石晶体,成为首屈一指的超硬新材料。该晶体属于_______ 晶体,化学式为_______ 。
(3)已知:
计算 的反应热为
的反应热为_______ kJ∙mol-1
(1)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为
 ,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。与K紧邻的I个数为
,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。与K紧邻的I个数为
(2)某晶体结构如图,其硬度超过金刚石晶体,成为首屈一指的超硬新材料。该晶体属于

(3)已知:
| 化学键 |  |  |  |  |
| 键能/( kJ∙mol-1) | 360 | 436 | 176 | 431 |
 的反应热为
的反应热为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】根据O、S、Cu、Zn四种元素及其化合物的结构与性质,回答有关问题。
(1)S原子的核外电子排布式为_______ ;在H2S分子中,S原子轨道的杂化类型是_______ 。
(2)H2O在乙醇中的溶解度大于H2S在乙醇中的溶解度,其原因是_______ 。
(3) 的空间构型为
的空间构型为_______ (用文字描述)。
(4)ZnCl2与氨水反应可形成配合物 [Zn(NH3)4]Cl2,1摩该配合物中含有σ键的数目为_______ mol。
(5)CuCl2加热至773K分解为CuCl和另一种物质,该物质的化学式为_______ 。
(6)Zn与Y所形成化合物晶体的晶胞如图所示。_______ 。
②该化合物的化学式为_______ 。(用符号Zn、Y表示)
(1)S原子的核外电子排布式为
(2)H2O在乙醇中的溶解度大于H2S在乙醇中的溶解度,其原因是
(3)
 的空间构型为
的空间构型为(4)ZnCl2与氨水反应可形成配合物 [Zn(NH3)4]Cl2,1摩该配合物中含有σ键的数目为
(5)CuCl2加热至773K分解为CuCl和另一种物质,该物质的化学式为
(6)Zn与Y所形成化合物晶体的晶胞如图所示。

②该化合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】金属晶体的原子堆积方式常有以下四种,请认真观察模型(见图),回答下列问题:
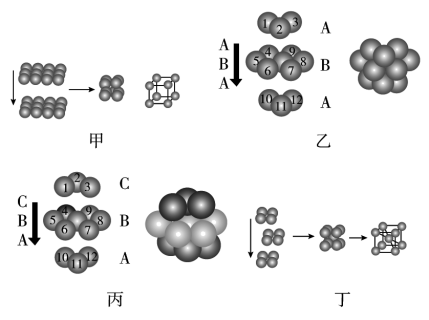
(1)四种堆积模型的堆积名称依次是________ 、________ 、________ 、________ 。
(2)甲堆积方式中的空间利用率为________ ,只有金属________ 采用这种堆积方式。
(3)乙与丙中两种堆积方式中金属原子的配位数________ (填“相同”或“不相同”);乙中的空间利用率为________ 。
(4)采取丁中堆积方式的金属通常有________ (任写三种金属元素的符号),每个晶胞中所含有的原子数为________ 。

(1)四种堆积模型的堆积名称依次是
(2)甲堆积方式中的空间利用率为
(3)乙与丙中两种堆积方式中金属原子的配位数
(4)采取丁中堆积方式的金属通常有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】金属在能源、环境、材料、生命科学等领域发挥着重要作用。
(1)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,在光催化还原 制备
制备 反应中,带状纳米
反应中,带状纳米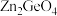 是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_______ 。
(2) 常用于检验二价亚铁离子,该晶体中所含化学键类型有
常用于检验二价亚铁离子,该晶体中所含化学键类型有_______
A.极性键 B.非极性键 C.氢键 D.配位键 E.离子键 F.金属键
(3)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电,CuF的熔点比CuCl的高,原因是_______ 。
(4)化学式为 的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色,已知
的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色,已知 的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量
的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量 溶液,所得AgCl沉淀的物质的量之比为3∶2∶1,则呈暗绿色的配合物内界的化学式为
溶液,所得AgCl沉淀的物质的量之比为3∶2∶1,则呈暗绿色的配合物内界的化学式为_______ 。
(5)某种铁镁合金储氢效率很高,其晶胞如图所示,

①该化合物的化学式为_______
②在该晶胞中与铁原子最近且等距离的镁原子有_______ 个。已知该晶胞密度为 ,NA为阿伏加德罗常数的值。则该晶胞中Fe原子与Mg原子的最近距离是
,NA为阿伏加德罗常数的值。则该晶胞中Fe原子与Mg原子的最近距离是_______ pm(用含NA、ρ的代数式表示)
(1)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,在光催化还原
 制备
制备 反应中,带状纳米
反应中,带状纳米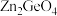 是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是(2)
 常用于检验二价亚铁离子,该晶体中所含化学键类型有
常用于检验二价亚铁离子,该晶体中所含化学键类型有A.极性键 B.非极性键 C.氢键 D.配位键 E.离子键 F.金属键
(3)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电,CuF的熔点比CuCl的高,原因是
(4)化学式为
 的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色,已知
的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色,已知 的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量
的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量 溶液,所得AgCl沉淀的物质的量之比为3∶2∶1,则呈暗绿色的配合物内界的化学式为
溶液,所得AgCl沉淀的物质的量之比为3∶2∶1,则呈暗绿色的配合物内界的化学式为(5)某种铁镁合金储氢效率很高,其晶胞如图所示,

①该化合物的化学式为
②在该晶胞中与铁原子最近且等距离的镁原子有
 ,NA为阿伏加德罗常数的值。则该晶胞中Fe原子与Mg原子的最近距离是
,NA为阿伏加德罗常数的值。则该晶胞中Fe原子与Mg原子的最近距离是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、R为原子序数依次增大的六种元素,位于元素周期表的前四周期。B元素原子含有3个能级,且每个能级所含的电子数相同;D的原子核外有8种运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子3d轨道上有4个未成对电子。请回答下列问题:
(1)写出C基态原子的价层电子排布____________ ,F基态原子的外围电子排布式_____________ 。
(2)下列说法正确的是____________ (填序号)。
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点:SiO2>CO2
B.第一电离能由小到大的顺序:B<C<D
C.N2与CO为等电子体,结构相似
D.稳定性:H2O>H2S,水分子更稳定的原因是水分子间存在氢键
(3)F元素位于周期表中_________ 区,其离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点。向F的硫酸盐溶液中通入过量的C与A形成的气体X可生成[F(X)4]2+,该离子的结构式为__________ (用元素符号表示)。
(4)某化合物与F(I)(I表示化合价为+ 1)结合形成下图所示的离子,该离子中碳原子的杂化方式为____________________ 。
(5)B单质的一种同素异形体的晶胞如下图所示,则一个晶胞中所含B原子的个数为____________ 。
(6)D与F形成离子个数比为1:1的化合物,晶胞与NaCl类似,设D离子的半径为apm, F离子的半径bpm,则该晶胞的空间利用率为_______________ 。
(1)写出C基态原子的价层电子排布
(2)下列说法正确的是
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点:SiO2>CO2
B.第一电离能由小到大的顺序:B<C<D
C.N2与CO为等电子体,结构相似
D.稳定性:H2O>H2S,水分子更稳定的原因是水分子间存在氢键
(3)F元素位于周期表中
(4)某化合物与F(I)(I表示化合价为+ 1)结合形成下图所示的离子,该离子中碳原子的杂化方式为

(5)B单质的一种同素异形体的晶胞如下图所示,则一个晶胞中所含B原子的个数为
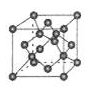
(6)D与F形成离子个数比为1:1的化合物,晶胞与NaCl类似,设D离子的半径为apm, F离子的半径bpm,则该晶胞的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用。回答下列问题:
(1)钠、铁、铝、铁、铜属于_______ 晶体, 铁熔化破坏的化学键为_______ 。
(2)NaCl的熔点为801 °C而AlCl3的熔点为194 °C,试分析其原因:_______ 。
(3)AlCl3分子中最多_______ 个原子共面,该晶体中存在的作用有_______ (填序号)。
A.范德华力 B.氢键 C.共价键 D.离子键
(4)铜的化合物种类很多。如图是氯化亚铜的晶胞结构,已知晶胞的棱长为a nm。

①Cu+与Cl-最短的距离是_______ nm,Cl-的配位数为_______ 。
②氯化亚铜密度的计算式为ρ=_______ g·cm-3 (用NA表示阿伏加德罗常数)。
(1)钠、铁、铝、铁、铜属于
(2)NaCl的熔点为801 °C而AlCl3的熔点为194 °C,试分析其原因:
(3)AlCl3分子中最多
A.范德华力 B.氢键 C.共价键 D.离子键
(4)铜的化合物种类很多。如图是氯化亚铜的晶胞结构,已知晶胞的棱长为a nm。

①Cu+与Cl-最短的距离是
②氯化亚铜密度的计算式为ρ=
您最近一年使用:0次



