下列事实中,不能用勒夏特列原理来解释的是
| A.向新制氯水中加入小苏打固体后漂白性明显增强 |
| B.氢气、碘蒸气、碘化氢气体组成的平衡体系,压缩体积后气体颜色变深 |
| C.合成氨时将氨液化分离,可提高原料的利用率。 |
| D.可乐等碳酸饮料突然打开后泛起大量泡沫 |
更新时间:2022-11-08 18:58:32
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定条件下, 与
与 发生反应:
发生反应: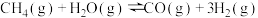 。设起始
。设起始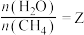 ,在恒压下,平衡时
,在恒压下,平衡时 体积分数
体积分数 与Z和T(温度)的关系如下图所示。下列说法
与Z和T(温度)的关系如下图所示。下列说法不正确 的是

 与
与 发生反应:
发生反应: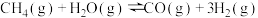 。设起始
。设起始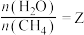 ,在恒压下,平衡时
,在恒压下,平衡时 体积分数
体积分数 与Z和T(温度)的关系如下图所示。下列说法
与Z和T(温度)的关系如下图所示。下列说法
A.该反应的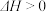 |
B.图中Z的大小关系: |
C.图中X点对应的平衡混合物中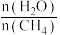 >3 >3 |
| D.温度不变时,图中X点对应的平衡在加压后ψ(CH4)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
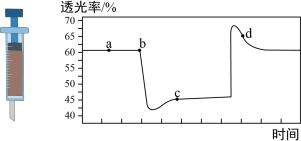
【推荐2】已知反应:2NO2(红棕色) N2O4(无色) ΔH<0,将一定量的NO2充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确的是
N2O4(无色) ΔH<0,将一定量的NO2充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确的是
 N2O4(无色) ΔH<0,将一定量的NO2充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确的是
N2O4(无色) ΔH<0,将一定量的NO2充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确的是
| A.b点的操作为拉伸注射器 |
| B.c点与a点相比,c(NO2)增大,c(N2O4)减小 |
C.d点 正< 正< 逆 逆 |
| D.若不忽略体系温度变化,且没有能量损失,则T(b)>T(c) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知苯酚(C6H5OH)与Fe3+反应生成[Fe(C6H5O)6]3-(紫色)。将6mL0. 1mol·L-1KI溶液和1mL 0.1 mol·L-1FeCl3溶液混合,发生反应:2Fe3+(aq) +2I-( aq)  2Fe2+ (aq) +I2(aq) ,下列有关该反应的说法错误的是
2Fe2+ (aq) +I2(aq) ,下列有关该反应的说法错误的是
 2Fe2+ (aq) +I2(aq) ,下列有关该反应的说法错误的是
2Fe2+ (aq) +I2(aq) ,下列有关该反应的说法错误的是| A.加入2 mL四氯化碳,振荡,平衡向右移动 |
| B.经四氯化碳多次萃取,在分离后的水溶液中滴加苯酚溶液,若溶液呈紫色,说明该反应是可逆反应 |
| C.加入少量I2固体,平衡向左移动 |
D.平衡常数的表达式为K=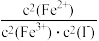 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实不能用化学平衡移动原理解释的是
| A.实验室收集氯气时,常用排饱和食盐水的方法 |
| B.用浓氨水和氢氧化钠固体快速制取氨气 |
C.工业合成氨N2(g) + 3H2(g) 2NH3(g) ΔH<0,采用400 ℃~ 500 ℃的高温条件 2NH3(g) ΔH<0,采用400 ℃~ 500 ℃的高温条件 |
| D.红棕色NO2加压后颜色先变深后变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】密闭容器中发生反应:2X(g)+Y(s) 2Z(g) ΔH<0,达到平衡时,下列说法正确的( )
2Z(g) ΔH<0,达到平衡时,下列说法正确的( )
 2Z(g) ΔH<0,达到平衡时,下列说法正确的( )
2Z(g) ΔH<0,达到平衡时,下列说法正确的( )| A.减小容器体积,平衡正向移动 | B.再加入Z,达平衡时Z的体积分数增大 |
| C.再加入X,X的转化率减小 | D.降低温度,Y的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在一定温度下,将等量的气体分别通入起始容积相同的密闭容器Ⅰ(恒容)和Ⅱ(恒压)中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是
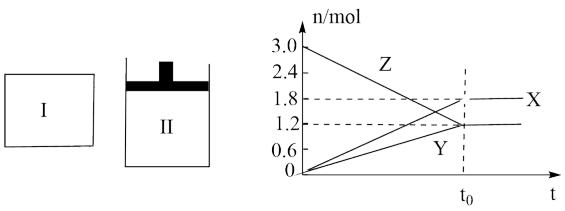
| A.当两容器中反应均达到平衡时,若两容器中Z的物质的量分数相同,则Y为固体或液体 |
| B.若Y为固体,则当容器Ⅰ中气体密度不变时,不能判断反应达到了平衡状态 |
| C.当两容器中反应均达到平衡时,若两容器的体积V(I)﹤V(II),则容器Ⅱ达到平衡所需的时间小于t0 |
| D.若达平衡后,对容器Ⅱ降低温度时,其体积减小,说明Z发生的反应为吸热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】氢气可通过下列反应制得:CO(g)+H2O(g) CO2(g)+H2(g) H<0,为了提高CO的平衡转化率,可采取的措施是
CO2(g)+H2(g) H<0,为了提高CO的平衡转化率,可采取的措施是
 CO2(g)+H2(g) H<0,为了提高CO的平衡转化率,可采取的措施是
CO2(g)+H2(g) H<0,为了提高CO的平衡转化率,可采取的措施是| A.增大压强 | B.降低温度 |
| C.更换催化剂 | D.增大CO的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实不能用勒夏特列原理解释的是
A.反应ClO-+H2O HClO+OH-,通入二氧化碳气体,溶液的漂白性增强 HClO+OH-,通入二氧化碳气体,溶液的漂白性增强 |
| B.合成氨工业上采用高温条件下反应 |
| C.为了增大汽水中二氧化碳的溶解量,采用加压方式 |
D.对于反应H2(g)+Br2(g)  2HBr(g)△H<0,达到平衡后,升温使气体颜色变深 2HBr(g)△H<0,达到平衡后,升温使气体颜色变深 |
您最近一年使用:0次



