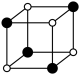
含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种原子序数为48的Cd2+配合物的结构如图所示,则下列说法正确的是
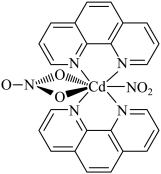

| A.该螯合物中N的杂化方式有2种 |
| B.1mol该配合物中通过螯合作用形成的配位键有6mol |
| C.Cd属于d区元素 |
| D.Cd的价电子排布式为4d85s2 |
更新时间:2022-11-07 22:50:02
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】W、X、Y、Z均为短周期元素且原子序数依次增大,元素X和Z同族。Z的单质为黄绿色气体,此气体同冷烧碱溶液作用,可得到含YZW的溶液,具有漂白性。下列说法正确的是
| A.原子半径大小为W<X<Y<Z |
| B.X的氢化物水溶液酸性强于Z的 |
| C.Y的氢化物为离子化合物 |
| D.X与Z具有相同的最高化合价 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】W、X、Y、Z为元素周期表中的主族元素,且原子序数均不大于20,W的原子序数最大,X位于第二周期且原子的最外层电子数是内层电子数的3倍,Y的单质在空气中易形成一层致密氧化膜,且Y原子的最外层电子数为奇数,Z与Y同周期且相邻,W、Y原子的最外层电子数之和等于Z原子的最外层电子数。下列说法正确的是( )
| A.最简单离子的半径:Y>W>X |
| B.气态氢化物的稳定性:X>Z |
| C.最高价氧化物对应水化物的碱性:Y>W |
| D.Y、Z的氧化物均不能溶解于水中,且均为碱性氧化物 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
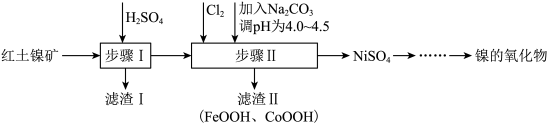
【推荐1】砷(As)是氮的同族元素,且比氮多2个电子层,镓(Ga)与铝同主族,砷化镓是当代国际公认的继硅之后最成熟的化合物半导体材料。某含砷(As)的有毒工业废水经如图流程转化为粗As2O3。已知:亚砷酸钙微溶于水,砷酸钙难溶于水。下列说法正确的是
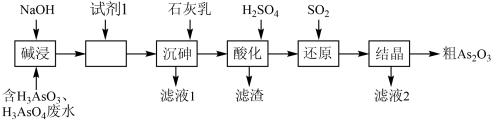

| A.As基态原子的价电子排布式为4s24p5 |
| B.“碱浸”的目的是将废水中的H3AsO3和H3AsO4转化为盐,H3AsO4转化为Na3AsO4的离子方程式为H++OH-=H2O |
| C.加入试剂1的目的是除杂 |
| D.每生成1molAs2O3,理论上需要标况下SO244.8L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在室温或接近室温时呈液态的自由离子构成的物质称为室温离子液体。某离子液体的制备原理如下:
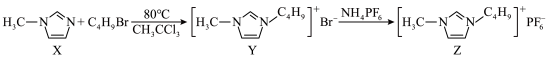
A.基态原子未成对电子数: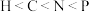 |
B.第二周期的主族元素中,第一电离能大于 的仅有一种 的仅有一种 |
| C.Z的阴离子中所有原子均满足8电子稳定结构 |
D.熔点: |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】下列有关说法不正确的是
A.咪唑为平面结构,结构为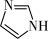 ,N的杂化方式为sp2杂化 ,N的杂化方式为sp2杂化 |
| B.H3AsO4、H3AsO3、H3AsO2三种酸中酸性最强的是H3AsO4 |
| C.某含钛配合物,化学式为[TiCl(H2O)5]Cl2,1mol该配合物中σ键的数目为16NA |
| D.SrCO3和CaCO3受热均可分解,且分解温度:SrCO3< CaCO3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】除少数卤化物外,大部分非金属卤化物都易水解,且反应不可逆。卤化物的水解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原子具有 和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受
和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受 的
的 进攻。其中
进攻。其中 的亲核水解机理如图。下列说法正确的是
的亲核水解机理如图。下列说法正确的是
 和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受
和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受 的
的 进攻。其中
进攻。其中 的亲核水解机理如图。下列说法正确的是
的亲核水解机理如图。下列说法正确的是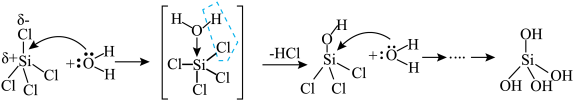
A.整个过程 的杂化方式不变 的杂化方式不变 |
B. 的水解历程与上述过程类似 的水解历程与上述过程类似 |
C. 水解会生成 水解会生成 和 和 |
D.由上述理论知 不能发生水解 不能发生水解 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】碳铂(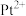 ,结构如图所示)是应用于临床的第二代铂类抗癌药物,下列说法错误的是
,结构如图所示)是应用于临床的第二代铂类抗癌药物,下列说法错误的是
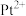 ,结构如图所示)是应用于临床的第二代铂类抗癌药物,下列说法错误的是
,结构如图所示)是应用于临床的第二代铂类抗癌药物,下列说法错误的是
| A.第一电离能:O>N>C>H | B. 是由极性键构成的极性分子 是由极性键构成的极性分子 |
C.碳原子的轨道杂化方式有 、 、 两种 两种 | D.1 mol该配合物含有4 mol配位键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】金属 溶于液氨中形成蓝色溶液,
溶于液氨中形成蓝色溶液, ,蓝色是生成了氨合电子
,蓝色是生成了氨合电子 (强还原剂)的缘故,向该溶液中加入穴醚类配体
(强还原剂)的缘故,向该溶液中加入穴醚类配体 ,得到首个含碱金属阴离子的金黄色化合物
,得到首个含碱金属阴离子的金黄色化合物 。下列说法正确的是
。下列说法正确的是
 溶于液氨中形成蓝色溶液,
溶于液氨中形成蓝色溶液, ,蓝色是生成了氨合电子
,蓝色是生成了氨合电子 (强还原剂)的缘故,向该溶液中加入穴醚类配体
(强还原剂)的缘故,向该溶液中加入穴醚类配体 ,得到首个含碱金属阴离子的金黄色化合物
,得到首个含碱金属阴离子的金黄色化合物 。下列说法正确的是
。下列说法正确的是| A.蓝色溶液具有强氧化性 | B. 中存在配位键 中存在配位键 |
C.粒子半径: | D.第一电离能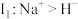 |
您最近一年使用:0次

 、
、 、
、 、
、


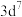
 和
和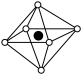


 胶体具有吸附性,可用于除去水中的悬浮颗粒物
胶体具有吸附性,可用于除去水中的悬浮颗粒物 分子的极性大于CH4
分子的极性大于CH4 存在3d、4s、4p等多个空轨道,可形成多种配位化合物
存在3d、4s、4p等多个空轨道,可形成多种配位化合物

