红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的化工原料,工业上用铬铁矿(主要成分是FeO·Cr2O3)制备红矾钠的过程中会发生如下反应:4FeO(s)+Cr2O3(s)+8Na2CO3(s)+7O2(g)⇌8Na2CrO4(s)+2Fe2O3(s)+8CO2(g)
请回答下列问题:
(1)请写出上述反应的化学平衡常数表达式:K=_______ 。
(2)此反应的lnK随着 的增大而增大,则反应的ΔH
的增大而增大,则反应的ΔH_______ 0(填“>”或“<”)。
(3)在一容积固定的密闭容器中加入一定量的反应物发生上述反应。该反应的逆反应速率与时间的关系如图所示:
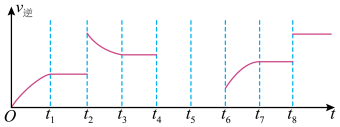
①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了条件,试判断t8时改变的条件可能是:_______ 。
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线。_________
(4)Cr2O3为重要铬系产品,我国科学家采用Cr2O3(SG)和H-SAPO-34复合催化剂极大提高短链烯烃选择性。CO2和H2在催化剂Cr2O3(SG)表面转化为甲醇的各步骤所需要克服的能垒及甲醇在H-SAPO-34作用下产生乙烯、丙烯示意图如图。
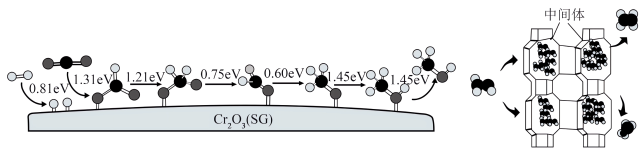
①吸附态用*表示,CO2→甲氧基(H3CO∗)过程中,_______ 的生成是决速步骤(填化学式)。
②H-SAPO-34具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。从结构角度推测、短链烯烃选择性提高的原因是_______ 。
请回答下列问题:
(1)请写出上述反应的化学平衡常数表达式:K=
(2)此反应的lnK随着
 的增大而增大,则反应的ΔH
的增大而增大,则反应的ΔH(3)在一容积固定的密闭容器中加入一定量的反应物发生上述反应。该反应的逆反应速率与时间的关系如图所示:

①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了条件,试判断t8时改变的条件可能是:
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线。
(4)Cr2O3为重要铬系产品,我国科学家采用Cr2O3(SG)和H-SAPO-34复合催化剂极大提高短链烯烃选择性。CO2和H2在催化剂Cr2O3(SG)表面转化为甲醇的各步骤所需要克服的能垒及甲醇在H-SAPO-34作用下产生乙烯、丙烯示意图如图。

①吸附态用*表示,CO2→甲氧基(H3CO∗)过程中,
②H-SAPO-34具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。从结构角度推测、短链烯烃选择性提高的原因是
更新时间:2022-11-10 22:39:20
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】甲醇蒸气转化为氢气的一种原理是 和
和 反应生成
反应生成 和
和 。
。
图是该过程中的能量变化示意图。若在反应体系中加入催化剂,反应速率增大,正反应活化能 的变化是
的变化是______ (填“增大”“减小”或“不变”),反应热 的变化是
的变化是______ (填“增大”“减小”或“不变”)。请写出 和
和 反应的热化学方程式:
反应的热化学方程式:______ 。
 和
和 反应生成
反应生成 和
和 。
。
图是该过程中的能量变化示意图。若在反应体系中加入催化剂,反应速率增大,正反应活化能
 的变化是
的变化是 的变化是
的变化是 和
和 反应的热化学方程式:
反应的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在下列事实中,什么因素影响了化学反应的速率?
(1)黄铁矿煅烧时要粉碎成细小颗粒___ ;
(2)夏天的食品变霉,在冬天不易发生该现象___ ;
(3)熔化的KClO3放出气泡很慢,撒入MnO2少量很快产生气体___ ;
(4)卤化银要保存在棕色试剂瓶中___ 。
(1)黄铁矿煅烧时要粉碎成细小颗粒
(2)夏天的食品变霉,在冬天不易发生该现象
(3)熔化的KClO3放出气泡很慢,撒入MnO2少量很快产生气体
(4)卤化银要保存在棕色试剂瓶中
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
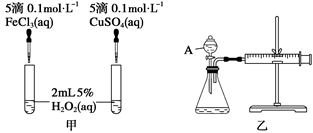
(1)定性分析:
①如图甲可通过观察_____________________________________ ,定性比较得出结论。
②有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是__________________ ,
③若H2O2在二氧化锰催化作用下发生反应,曾检测出有物质MnO3出现,写出整个反应过程的两个化学方程式:___________________________ ,________________________ 。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为________ ,实验中需要测量的数据是_________________ 。

(1)定性分析:
①如图甲可通过观察
②有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
③若H2O2在二氧化锰催化作用下发生反应,曾检测出有物质MnO3出现,写出整个反应过程的两个化学方程式:
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学平衡
(1)化学平衡状态的概念:
在一定条件下,当反应进行到一定程度时,_______ 与_______ 相等,反应物的_______ 和生成物的_______ 都不再改变,达到一种表面静止的状态,称之为_______ 状态。
(2)化学反应的限度是指可逆反应在一定条件下所能达到或完成的_______ 程度,即该反应进行的限度。化学反应的限度决定了反应物在该条件下转化为生成物的最大_______ 。
(3)转化率=_______ 。
(4)影响因素:改变反应条件,可以在一定程度上改变该反应的化学_______ 状态。
(1)化学平衡状态的概念:
在一定条件下,当反应进行到一定程度时,
(2)化学反应的限度是指可逆反应在一定条件下所能达到或完成的
(3)转化率=
(4)影响因素:改变反应条件,可以在一定程度上改变该反应的化学
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】合成氨反应的限度
(1)合成氨反应的特点
(2)影响因素
①外界条件:_______ 温度、_______ 压强,有利于化学平衡向合成氨的方向移动。
②投料比:温度压强一定时, 、
、 的体积比为
的体积比为_______ 时平衡混合物中氨的百分含量最高。
(1)合成氨反应的特点
| 合成氨反应 | ——可逆性:反应为 |
| ——体积变化:正反应是气体体积 | |
——焓变:  | |
——常温下自发性: , , |
(2)影响因素
①外界条件:
②投料比:温度压强一定时,
 、
、 的体积比为
的体积比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在密闭容器中进行如下反应: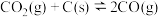
 ,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
(1)增加 的量,则平衡
的量,则平衡___________ (填“逆移”“正移”或“不移”,下同),
___________ (填“增大”“减小”或“不变”,下同)。
(2)恒温条件,增大反应容器的容积,则平衡___________ ,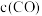
___________ (填“增大”“减小”或“不变”,下同)
(3)保持反应容器的容积和温度不变,通入He气,则平衡___________ ,
___________ 。
(4)保持反应容器的压强不变,通入Ar气,则平衡___________ ,
___________ 。
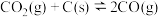
 ,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度、速率、平衡如何变化。(1)增加
 的量,则平衡
的量,则平衡
(2)恒温条件,增大反应容器的容积,则平衡
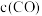
(3)保持反应容器的容积和温度不变,通入He气,则平衡

(4)保持反应容器的压强不变,通入Ar气,则平衡

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】 可用FeO吸收获得
可用FeO吸收获得 .有关反应:
.有关反应:
①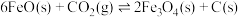
②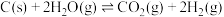
(1)反应①的化学平衡常数表达式为________ 。
(2)若 时反应①达到平衡,此时
时反应①达到平衡,此时 的浓度为
的浓度为 ,保持其他条件不变,再加入一定量的
,保持其他条件不变,再加入一定量的 ,再次达到平衡后
,再次达到平衡后 的浓度为
的浓度为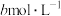 ,则a
,则a________ b(选填“>”、“<”或“=”)。请说明理由________ 。
 可用FeO吸收获得
可用FeO吸收获得 .有关反应:
.有关反应:①
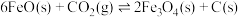
②
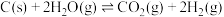
(1)反应①的化学平衡常数表达式为
(2)若
 时反应①达到平衡,此时
时反应①达到平衡,此时 的浓度为
的浓度为 ,保持其他条件不变,再加入一定量的
,保持其他条件不变,再加入一定量的 ,再次达到平衡后
,再次达到平衡后 的浓度为
的浓度为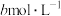 ,则a
,则a
您最近一年使用:0次
【推荐2】氨的合成是最重要的化工生产之一。
已知: N2(g)+ 3H2(g) 2NH3(g) △H =-92.4 kJ/mol
2NH3(g) △H =-92.4 kJ/mol
在甲、乙、丙三个不同密闭容器中,按不同方式投料,起始温度和容积相同,相关数据如下表所示:
则平衡时容器的体积V甲_____ V丙, 平衡常数K丙_______ K乙(填>、<或=)。
已知: N2(g)+ 3H2(g)
 2NH3(g) △H =-92.4 kJ/mol
2NH3(g) △H =-92.4 kJ/mol在甲、乙、丙三个不同密闭容器中,按不同方式投料,起始温度和容积相同,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1 mol N2、3 molH2 | 2 mol NH3 | 2 mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
则平衡时容器的体积V甲
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】在一个容积不变的密闭容器中发生反应CO2(g)+H2(g)  CO(g)+H2O(g)其平衡常数K和温度的关系如下表所示:
CO(g)+H2O(g)其平衡常数K和温度的关系如下表所示:
请填写下列空白。
(1)该反应的平衡常数表达式K=___________ ,该反应为___________ 反应(填“吸热”或“放热”)
(2)在830℃时,向容器中充入1molCO、5molH2O,保持温度不变,反应达到平衡后,其平衡常数___________ 1.0(填“大于”或“等于”或“小于”)
(3)在1200℃时,在某时刻反应混合物中CO2、H2、CO、H2O浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时平衡移动方向为___________ (填“正反应方向”或“逆反应方向”或“不移动”)
 CO(g)+H2O(g)其平衡常数K和温度的关系如下表所示:
CO(g)+H2O(g)其平衡常数K和温度的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的平衡常数表达式K=
(2)在830℃时,向容器中充入1molCO、5molH2O,保持温度不变,反应达到平衡后,其平衡常数
(3)在1200℃时,在某时刻反应混合物中CO2、H2、CO、H2O浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时平衡移动方向为
您最近一年使用:0次



