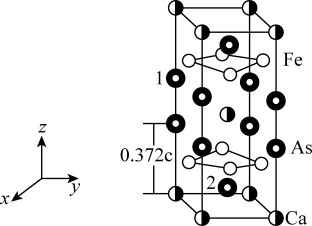
最近合成的一种铁基超导材料 ,在低温高压下能显示出独特的电子性质,晶胞结构如图所示,回答下列问题:
,在低温高压下能显示出独特的电子性质,晶胞结构如图所示,回答下列问题:
(1)Fe的基态原子共有_______ 种不同能级的电子。
(2) 的沸点(1935℃)高于
的沸点(1935℃)高于 的沸点(130.2℃)原因是
的沸点(130.2℃)原因是_______ 。
(3)Fe可以与CO、NO、 等多种微粒形成配合物。
等多种微粒形成配合物。
①C、N、O的第一电离能由大到小的顺序为_______ 。
②写出 的一种等电子体分子
的一种等电子体分子_______ 。
(4) 溶液中含有的微粒内部及微粒间作用力除共价键外还有
溶液中含有的微粒内部及微粒间作用力除共价键外还有_______ ,溶质阴离子的中心原子杂化轨道类型为_______ 。
(5)该材料的化学式为_______ ,已知:体心的Ca原子与顶点的Ca原子有着相同的化学环境(化学环境受周围粒子的数目与距离所影响),该晶胞的晶胞参数为a pm、a pm、c pm,晶胞中As原子1分数坐标为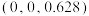 ,则As原子2的分数坐标为
,则As原子2的分数坐标为_______ 。
 ,在低温高压下能显示出独特的电子性质,晶胞结构如图所示,回答下列问题:
,在低温高压下能显示出独特的电子性质,晶胞结构如图所示,回答下列问题:
(1)Fe的基态原子共有
(2)
 的沸点(1935℃)高于
的沸点(1935℃)高于 的沸点(130.2℃)原因是
的沸点(130.2℃)原因是(3)Fe可以与CO、NO、
 等多种微粒形成配合物。
等多种微粒形成配合物。①C、N、O的第一电离能由大到小的顺序为
②写出
 的一种等电子体分子
的一种等电子体分子(4)
 溶液中含有的微粒内部及微粒间作用力除共价键外还有
溶液中含有的微粒内部及微粒间作用力除共价键外还有(5)该材料的化学式为
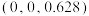 ,则As原子2的分数坐标为
,则As原子2的分数坐标为
更新时间:2022-11-13 19:13:04
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
【推荐1】铊(Tl)本身是一种剧毒物质,为毒性最大的金属元素之一,但是铊在工业中的用途非常广泛,主要存在于一些矿物和工业废水中,也可以从含铊的合金中提取.从某铅锌厂的富铊灰(主要成分为 、
、 、
、 、
、 、
、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示:
①在氯化物-硫酸水溶液中,铊元素以 形式存在;
形式存在;
(2)萃取过程的反应原理为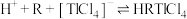 .
.
请回答下列问题:
(1)基态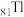 原子核外电子的运动状态有
原子核外电子的运动状态有________ 种.
(2)“浸取I”过程中为提高铊的浸取速率,可采取的措施有________________ (写出两条).
(3)写出“浸取I”中 发生反应的化学方程式:
发生反应的化学方程式:________________ ,“滤渣”的主要成分是________ (填化学式).
(4)请从化学平衡的角度解释“反萃取”过程中加入 溶液的原因:
溶液的原因:________________ .
(5)写出“还原氯化沉淀”中反应的离子方程式:________________ .
(6)通过沉淀法也可以去除工业废水中的 和
和 .
.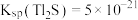 ,某地区规定工业污水中铊的污染物排放限值为
,某地区规定工业污水中铊的污染物排放限值为 ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中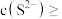
________  (假设污水中铊全部以
(假设污水中铊全部以 形式存在).
形式存在).
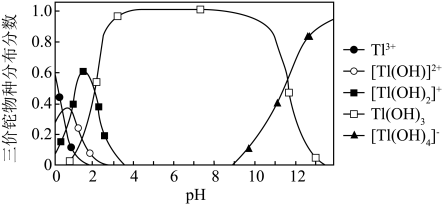
②向含铊废水中加入溴水,使 充分氧化成
充分氧化成 ,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是________________ .
 、
、 、
、 、
、 、
、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示: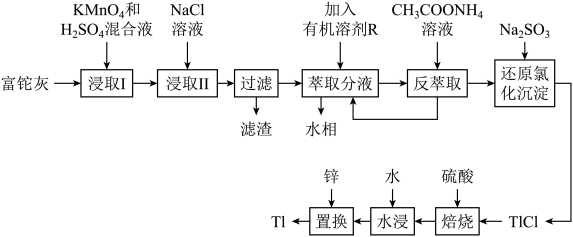
①在氯化物-硫酸水溶液中,铊元素以
 形式存在;
形式存在;(2)萃取过程的反应原理为
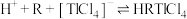 .
.请回答下列问题:
(1)基态
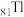 原子核外电子的运动状态有
原子核外电子的运动状态有(2)“浸取I”过程中为提高铊的浸取速率,可采取的措施有
(3)写出“浸取I”中
 发生反应的化学方程式:
发生反应的化学方程式:(4)请从化学平衡的角度解释“反萃取”过程中加入
 溶液的原因:
溶液的原因:(5)写出“还原氯化沉淀”中反应的离子方程式:
(6)通过沉淀法也可以去除工业废水中的
 和
和 .
.
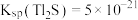 ,某地区规定工业污水中铊的污染物排放限值为
,某地区规定工业污水中铊的污染物排放限值为 ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中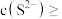
 (假设污水中铊全部以
(假设污水中铊全部以 形式存在).
形式存在).②向含铊废水中加入溴水,使
 充分氧化成
充分氧化成 ,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】AGS(Ag、Ga、S)可构成一种红外非线性晶体。回答下列问题:
(1)基态时Ga原子核外电子排布式为[Ar]____ ,Ag与铜同族,Ag形成Ag+时失去的是____ 轨道上的一个电子。
(2)硫与碳能形成多种化合物,如CS2、硫花(分子式为C16S8,结构如图所示)。
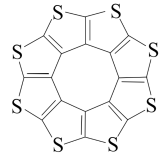
①CS2分子的空间构型为____ 。
②CS2、硫花中碳原子的杂化方式分别是____ 。
③每个硫花分子中含____ 个σ键。
(3)噻吩、呋喃及吡咯(结构如图)均是常见的杂环化合物。

在水中溶解度最大的是____ 填名称);沸点从高到低的顺序是____ (用名称表示),其理由是____ 。
(4)AGS的晶胞结构如图所示(晶胞参数为a、b、c,单位为pm,其中a=b);

用NA表示阿伏加德罗常数的值,该晶体的密度为____ g•cm-3(用含a、c、NA的代数式表示)。
(1)基态时Ga原子核外电子排布式为[Ar]
(2)硫与碳能形成多种化合物,如CS2、硫花(分子式为C16S8,结构如图所示)。

①CS2分子的空间构型为
②CS2、硫花中碳原子的杂化方式分别是
③每个硫花分子中含
(3)噻吩、呋喃及吡咯(结构如图)均是常见的杂环化合物。

在水中溶解度最大的是
(4)AGS的晶胞结构如图所示(晶胞参数为a、b、c,单位为pm,其中a=b);

用NA表示阿伏加德罗常数的值,该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】ZnS、CdSe均为重要的半导体材料,可应用于生物标记和荧光显示领域,并在光电器件、生物传感和激光材料等方面也得到了广泛的应用。
(1)基态Zn原子的价层电子排布式为______ 。
(2)S与P在周期表中是相邻元素,两者的第一电离能:S_____ P(填“>”、“<”或“=”),解释其原因_____ 。
(3)CdSe的一种晶体为闪锌矿型结构,晶胞结构如图所示。

①晶胞中,与Cd原子距离最近且相等的Se原子有_____ 个。
②已知,晶胞边长anm,阿伏加德罗常数为NA,CdSe的摩尔质量为191g•mol-1。则CdSe晶体的密度是_____ g•cm-3。(1nm=10-7cm)
(4)电化学沉积法可用于制备CdSe,其装置示意图如图。

电解过程中阳极有无色气泡产生,CdSe在阴极生成,纯度及颗粒大小会影响CdSe性能,沉积速率过快容易团聚。
①已知H2SeO3是弱酸。控制合适的电压,可以使Cd2+转化为纯净的CdSe,写出阴极的电极反应式:_____ 。
②研究表明,为得到更致密均匀的CdSe薄膜,可用二甲基甲酰胺( )做溶剂降低Cd2+浓度,从结构的角度分析原因:
)做溶剂降低Cd2+浓度,从结构的角度分析原因:_____ 。
(1)基态Zn原子的价层电子排布式为
(2)S与P在周期表中是相邻元素,两者的第一电离能:S
(3)CdSe的一种晶体为闪锌矿型结构,晶胞结构如图所示。

①晶胞中,与Cd原子距离最近且相等的Se原子有
②已知,晶胞边长anm,阿伏加德罗常数为NA,CdSe的摩尔质量为191g•mol-1。则CdSe晶体的密度是
(4)电化学沉积法可用于制备CdSe,其装置示意图如图。

电解过程中阳极有无色气泡产生,CdSe在阴极生成,纯度及颗粒大小会影响CdSe性能,沉积速率过快容易团聚。
①已知H2SeO3是弱酸。控制合适的电压,可以使Cd2+转化为纯净的CdSe,写出阴极的电极反应式:
②研究表明,为得到更致密均匀的CdSe薄膜,可用二甲基甲酰胺(
 )做溶剂降低Cd2+浓度,从结构的角度分析原因:
)做溶剂降低Cd2+浓度,从结构的角度分析原因:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)元素p为26号元素,请写出其基态原子外围电子排布式:____ 。
(2)c与a形成6个原子组成分子结构简式:__________ ,该分子是:_______ (填“极性”或“非极性”)分子。
(3)表中O、P两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态O2+再失去一个电子比气态P2+再失去一个电子难。对此,你的解释是__________________________ ;
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
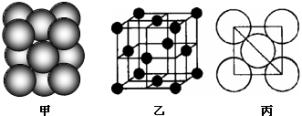
晶胞中i原子的配位数为___________ ,一个晶胞中i原子的数目为____________ 。
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p | |||||||||||||||
试回答下列问题:
(1)元素p为26号元素,请写出其基态原子外围电子排布式:
(2)c与a形成6个原子组成分子结构简式:
(3)表中O、P两元素的部分电离能数据列于下表:
| 元 素 | O | P | |
| 电离能kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态O2+再失去一个电子比气态P2+再失去一个电子难。对此,你的解释是
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

晶胞中i原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】自然界中存在大量的金属元素,在工农业生产中有着广泛的应用。回答下列问题:
(1)下列有关微粒性质的排列顺序错误的是___________。
(2)基态Cu原子核外电子运动状态有___________ 种,其核外电子排布式中未成对电子数为___________ 个。
(3)钌(Ru)一多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(Ⅱ)的配位数是___________ ,N原子的杂化类型为___________ 。 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点103℃,则
为浅黄色液体,沸点103℃,则 中含有的化学键类型包括___________(填字母)。
中含有的化学键类型包括___________(填字母)。
(5) 比
比 更稳定的原因是
更稳定的原因是___________ 。
(1)下列有关微粒性质的排列顺序错误的是___________。
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
C.离子半径: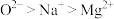 | D.原子的未成对电子数:Mn>Si>Cl |
(2)基态Cu原子核外电子运动状态有
(3)钌(Ru)一多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(Ⅱ)的配位数是

 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点103℃,则
为浅黄色液体,沸点103℃,则 中含有的化学键类型包括___________(填字母)。
中含有的化学键类型包括___________(填字母)。| A.极性共价键 | B.离子键 | C.配位键 | D.金属键 |
(5)
 比
比 更稳定的原因是
更稳定的原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D、E、F是前四周期的六种元素,原子序数依次增大。A、B、D三种元素分别位于不同短周期的不同主族。C、D对应的简单离子核外电子排布相同,A、B、C、D元素可形成一种新型漂白剂(结构如图),E元素正三价阳离子的3d轨道为半充满状态,F元素最外层只有一个电子,焰色反应为蓝绿色。

回答下列问题:
(1)基态A原子电子占据最高能级的电子云轮廓图为___________ 形。D元素基态原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。基态原子与F同周期且最外层电子数相等的元素还有___________ (填元素符号)。E元素位于元素周期表___________ 区。
(2)B元素名称是___________ 。新型漂白剂中C元素的化合价为___________ 。C元素能形成两种常见单质,其中沸点高的是___________ (填分子式),原因是___________ 。
(3)元素E与F的第二电离能 I2(F)>I2(E)的原因是___________ 。
(4)E的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是___________ (填字母序号) 。
。
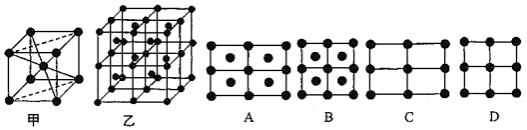

回答下列问题:
(1)基态A原子电子占据最高能级的电子云轮廓图为
(2)B元素名称是
(3)元素E与F的第二电离能 I2(F)>I2(E)的原因是
(4)E的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的截面图是
 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】卤族元素可以与很多元素形成多种具有不同组成、结构、性质的物质。请回答下列问题:
(1)基态氟原子价电子的轨道表示式为_______ 。
(2)亚硝酰氯(NOCl)是有机合成中的重要试剂,其中中心原子的杂化形式为_______ 。等电子体是指价电子数和原子数相同的分子、离子或原子团,写出与(NOCl)互为等电子体的一种分子_______ (填化学式)。
(3)东南大学某课题组合成了一种新型具有平面分子结构的醌类聚合物PPPA,PPPA可作为有机锌离子电池的正极材料。_______ 。
②NaCl溶液中存在水合钠离子,其示意图如图1所示。从电负性角度来解释这一现象_______ 。
(4)磷和硫均能形成多种卤化物。下列说法正确的是_______ (填标号)。
A.SCl2、PCl5均属于非极性分子
B.PCl3、S2Cl2的空间构型分别为三角锥形、直线形
C.NF3、S2Br2分子中各原子最外层均满足8电子稳定结构
(5)γ-AgI晶胞为立方结构,晶胞中I-采取面心立方堆积方式(如图3);γ-AgI晶胞沿x、y、z轴方向的投影均如图4所示。_______ (填“正四面体”或“正八面体”)空隙,其填充率为_______ 。
②γ-AgI晶胞的密度为ρg•cm-3,则晶胞中两个最近的Ag+之间的距离为_______ nm(NA表示阿伏加德罗常数的值)。
(1)基态氟原子价电子的轨道表示式为
(2)亚硝酰氯(NOCl)是有机合成中的重要试剂,其中中心原子的杂化形式为
(3)东南大学某课题组合成了一种新型具有平面分子结构的醌类聚合物PPPA,PPPA可作为有机锌离子电池的正极材料。

②NaCl溶液中存在水合钠离子,其示意图如图1所示。从电负性角度来解释这一现象
(4)磷和硫均能形成多种卤化物。下列说法正确的是
A.SCl2、PCl5均属于非极性分子
B.PCl3、S2Cl2的空间构型分别为三角锥形、直线形
C.NF3、S2Br2分子中各原子最外层均满足8电子稳定结构
(5)γ-AgI晶胞为立方结构,晶胞中I-采取面心立方堆积方式(如图3);γ-AgI晶胞沿x、y、z轴方向的投影均如图4所示。

②γ-AgI晶胞的密度为ρg•cm-3,则晶胞中两个最近的Ag+之间的距离为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐2】3-氯靛红酸酐( )是重要的材料中间体,其制备流程图如下:
)是重要的材料中间体,其制备流程图如下:
(1)3-氯靛红酸酐的分子式为_____ ,苯环上碳原子的杂化方式为_____ ;
(2)有机物B的名称为_____ ,写出符合下列条件有机物B的所有同分异构体的结构简式_____ ;
a.苯环上只有两个取代基且互为邻位 b.既能发生银镜反应又能发生水解反应
(3)该流程未采用甲苯直接硝化的方法制备有机物B,而是经由①、②、③三步反应进行制取,其目的是_____ ;
(4)⑥的反应类型是_____ ,⑥的主要目的是_____ ;
(5)⑧的反应试剂和条件为_____ ;F中含氧官能团的名称为_____ ;
(6)以有机物C为原料,在一定条件下制备含酰胺基聚合物的化学方程式_____ 。
 )是重要的材料中间体,其制备流程图如下:
)是重要的材料中间体,其制备流程图如下:

(1)3-氯靛红酸酐的分子式为
(2)有机物B的名称为
a.苯环上只有两个取代基且互为邻位 b.既能发生银镜反应又能发生水解反应
(3)该流程未采用甲苯直接硝化的方法制备有机物B,而是经由①、②、③三步反应进行制取,其目的是
(4)⑥的反应类型是
(5)⑧的反应试剂和条件为
(6)以有机物C为原料,在一定条件下制备含酰胺基聚合物的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】(1)下列反应可用于检测司机是否酒后驾驶: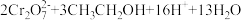
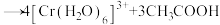 。
。
①配合物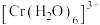 中,与
中,与 形成配位键的原子是
形成配位键的原子是__________ (填元素符号)。
② 中
中 原子的杂化轨道类型是
原子的杂化轨道类型是________ ;
 含有
含有 键的数目为
键的数目为_______ 。
(2) 分子中,
分子中, 原子的杂化轨道类型是
原子的杂化轨道类型是__________ ;写出由3个原子组成且与 具有相同空间构型的离子:
具有相同空间构型的离子:___________ (填一个即可)。
(3)石墨烯(结构如图1所示)是一种由单层碳原子构成的具有平面结构的新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(结构如图2所示)。
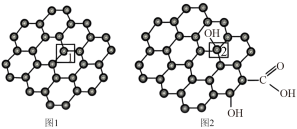
氧化石墨烯中2号 原子的杂化方式是
原子的杂化方式是_________ ,该 原子与相邻
原子与相邻 原子形成的键角
原子形成的键角______ (填“>”“<”或“=”)石墨烯中1号 与相邻
与相邻 形成的键角。
形成的键角。
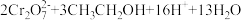
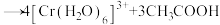 。
。①配合物
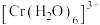 中,与
中,与 形成配位键的原子是
形成配位键的原子是②
 中
中 原子的杂化轨道类型是
原子的杂化轨道类型是
 含有
含有 键的数目为
键的数目为(2)
 分子中,
分子中, 原子的杂化轨道类型是
原子的杂化轨道类型是 具有相同空间构型的离子:
具有相同空间构型的离子:(3)石墨烯(结构如图1所示)是一种由单层碳原子构成的具有平面结构的新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(结构如图2所示)。

氧化石墨烯中2号
 原子的杂化方式是
原子的杂化方式是 原子与相邻
原子与相邻 原子形成的键角
原子形成的键角 与相邻
与相邻 形成的键角。
形成的键角。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】钴的化合物在磁性材料生产、电池制造、催化剂制备等方面应用十分广泛。
(1)基态Co原子的核外电子排布式为______ ,其中,3d能级上有_____ 个未成对电子。
(2)化合物四氨基钴酞菁分子的结构式如图。四氨基钴酞菁中N原子的杂化轨道类型为_____ 。

(3)纳米结构的氧化钴可以在室温下氧化甲醛(HCHO),甲醛各原子都达到最外层稳定结构,则甲醛分子的空间构型为______ 。
(4)某含钴配合物的组成为CoCl3•5NH3•H2O,该配合物中Co离子的配位数是6,1mol该配合物可以与足量的硝酸银反应生成3mol AgCl沉淀,则该配合物的配体是____ 。
(5)已知CoCl2的颜色变化情况如下:

则实验室中的可循环硅胶干燥剂掺杂CoCl2的意义是____ 。
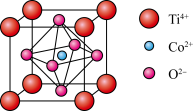
(6)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如下图所示,则晶体中与每个O2-相邻的O2-有_________ 个,该钴的化合物的化学式是_____ 。
(1)基态Co原子的核外电子排布式为
(2)化合物四氨基钴酞菁分子的结构式如图。四氨基钴酞菁中N原子的杂化轨道类型为

(3)纳米结构的氧化钴可以在室温下氧化甲醛(HCHO),甲醛各原子都达到最外层稳定结构,则甲醛分子的空间构型为
(4)某含钴配合物的组成为CoCl3•5NH3•H2O,该配合物中Co离子的配位数是6,1mol该配合物可以与足量的硝酸银反应生成3mol AgCl沉淀,则该配合物的配体是
(5)已知CoCl2的颜色变化情况如下:

则实验室中的可循环硅胶干燥剂掺杂CoCl2的意义是
(6)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如下图所示,则晶体中与每个O2-相邻的O2-有

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】钙钛矿型材料是一种具有独特物理性质的无机材料,因最早被发现存在于钙钛矿石中的钛酸钙( )而得名,其通式为
)而得名,其通式为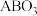 。请回答下列问题:
。请回答下列问题:
(1)钙钛矿( )的晶胞结构如图所示(原子半径未区分),其中位于晶胞面上的原子为
)的晶胞结构如图所示(原子半径未区分),其中位于晶胞面上的原子为___________ (填“Ca”“Ti”或“O”,下同),位于顶点的原子为___________ 。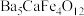 ),该物质表现出优异的氧气吸收和释放性能,这一发现有望成为通过化学循环进行空气分离。该新型钙钛矿的结构如图所示:
),该物质表现出优异的氧气吸收和释放性能,这一发现有望成为通过化学循环进行空气分离。该新型钙钛矿的结构如图所示:___________ 。
②Ba、Ca、Fe、O四种元素的第一电离能由大到小的顺序是___________ 。
③该新型钙钛矿结构中,Ca原子位于6个O原子形成的八面体中,而Fe原子位于4个O原子形成的四面体中,解释Ca为什么不位于O原子形成的四面体中:___________ 。
(3)钙钛矿型材料应用广泛,如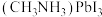 可作为太阳能电池材料而被应用,有人提出了水降解该物质的反应机理如图所示。
可作为太阳能电池材料而被应用,有人提出了水降解该物质的反应机理如图所示。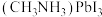 的晶体类型是
的晶体类型是___________ 。
②存在反应: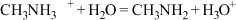 ,
,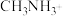 和
和 的化学键类别的不同之处是
的化学键类别的不同之处是___________ ;键角: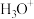
___________ (填“>”“=”或“<”) 。
。
 )而得名,其通式为
)而得名,其通式为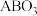 。请回答下列问题:
。请回答下列问题:(1)钙钛矿(
 )的晶胞结构如图所示(原子半径未区分),其中位于晶胞面上的原子为
)的晶胞结构如图所示(原子半径未区分),其中位于晶胞面上的原子为
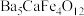 ),该物质表现出优异的氧气吸收和释放性能,这一发现有望成为通过化学循环进行空气分离。该新型钙钛矿的结构如图所示:
),该物质表现出优异的氧气吸收和释放性能,这一发现有望成为通过化学循环进行空气分离。该新型钙钛矿的结构如图所示:
②Ba、Ca、Fe、O四种元素的第一电离能由大到小的顺序是
③该新型钙钛矿结构中,Ca原子位于6个O原子形成的八面体中,而Fe原子位于4个O原子形成的四面体中,解释Ca为什么不位于O原子形成的四面体中:
(3)钙钛矿型材料应用广泛,如
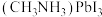 可作为太阳能电池材料而被应用,有人提出了水降解该物质的反应机理如图所示。
可作为太阳能电池材料而被应用,有人提出了水降解该物质的反应机理如图所示。
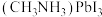 的晶体类型是
的晶体类型是②存在反应:
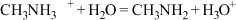 ,
,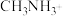 和
和 的化学键类别的不同之处是
的化学键类别的不同之处是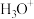
 。
。
您最近一年使用:0次
【推荐3】铜元素是人体所必须的一种微量元素,铜也是人类最早发现和使用的金属。
回答下列问题:
(1)金属铜晶体的原子堆积模型属于________ (填堆积模型名称),其原子的空间利用率为_______ 。
(2)简单金属离子在水溶液中有颜色的原因,是其价层电子中含有的未成对电子发生跃迁,如:Fe3+呈黄色、Fe2+呈绿色、Cu2+呈蓝色等;预测Cu+为_____ 色,原因是_____ 。
(3)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中Cu原子处于面心,Au原子处于顶点,则该合金中Cu原子与Au原子数目之比为________ ,该晶体中原子之间的作用力是________ 。
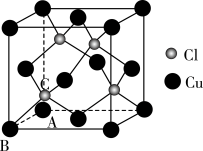
(4)某种铜的氯化物晶体结构如图所示。此晶体中铜原子的配位数是________ ;若A的原子坐标是(0,0,0),B的原子坐标是(0,1,0),则C的原子坐标是________ ;设晶胞参数为a pm,则该铜的氯化物晶体的密度为________ g·cm-3。(用含a和NA的式子表示,NA为阿伏加 德罗常数)
回答下列问题:
(1)金属铜晶体的原子堆积模型属于
(2)简单金属离子在水溶液中有颜色的原因,是其价层电子中含有的未成对电子发生跃迁,如:Fe3+呈黄色、Fe2+呈绿色、Cu2+呈蓝色等;预测Cu+为
(3)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中Cu原子处于面心,Au原子处于顶点,则该合金中Cu原子与Au原子数目之比为
(4)某种铜的氯化物晶体结构如图所示。此晶体中铜原子的配位数是

您最近一年使用:0次



