用图示方法表示你对电离平衡、水解平衡、沉淀溶解平衡的认识________ 。
更新时间:2022-11-26 17:22:16
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】判断正误
1.温度一定时,水的电离常数与水的离子积常数相等_______ ;
2.100 ℃的纯水中c(H+)=1×10—6 mol·L—1,此时水呈酸性_______ ;
3.在蒸馏水中滴加浓H2SO4,Kw不变_______ ;
4.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同_______ ;
5.室温下,0.1 mol·L—1的HCl溶液与0.1 mol·L—1的NaOH溶液中水的电离程度相等_______ ;
6.任何水溶液中均存在H+和OH—,且水电离出的c(H+)和c(OH—)相等_______ ;
7.25 ℃时,0.1 mol·L—1的NaOH溶液中KW=1×10—13 mol2·L—2_______ ;
8.某温度下,纯水中的c(H+)=2×10—7mol·L—1,则c(OH—)=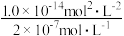
_______ ;
9.25 ℃时,0.01 mol·L—1的盐酸中,c(OH—)=1.0×10—12mol·L—1_______ 。
1.温度一定时,水的电离常数与水的离子积常数相等
2.100 ℃的纯水中c(H+)=1×10—6 mol·L—1,此时水呈酸性
3.在蒸馏水中滴加浓H2SO4,Kw不变
4.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
5.室温下,0.1 mol·L—1的HCl溶液与0.1 mol·L—1的NaOH溶液中水的电离程度相等
6.任何水溶液中均存在H+和OH—,且水电离出的c(H+)和c(OH—)相等
7.25 ℃时,0.1 mol·L—1的NaOH溶液中KW=1×10—13 mol2·L—2
8.某温度下,纯水中的c(H+)=2×10—7mol·L—1,则c(OH—)=
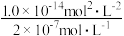
9.25 ℃时,0.01 mol·L—1的盐酸中,c(OH—)=1.0×10—12mol·L—1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)常温下,物质的量浓度均为0.1 mol/L的下列溶液:①NH4HCO3 ②NH4Cl ③(NH4)2SO4 ④NH4HSO4 ⑤(NH4)2Fe(SO4)2 ⑥氨水,溶液中c(NH )最大的是
)最大的是___________ (填序号)。
(2)在溶液③中___________ (填离子符号)的浓度为0.1 mol/L;NH3·H2O和___________ 的浓度之和为0.2 mol/L。
(3)将体积相等的稀NaOH溶液和CH3COOH溶液混合,若溶液中c(Na+)=c(CH3COO-),则混合前c(NaOH)___________ (填“>”“<”或“=”)c(CH3COOH)。
(1)常温下,物质的量浓度均为0.1 mol/L的下列溶液:①NH4HCO3 ②NH4Cl ③(NH4)2SO4 ④NH4HSO4 ⑤(NH4)2Fe(SO4)2 ⑥氨水,溶液中c(NH
 )最大的是
)最大的是(2)在溶液③中
(3)将体积相等的稀NaOH溶液和CH3COOH溶液混合,若溶液中c(Na+)=c(CH3COO-),则混合前c(NaOH)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图所示三个烧瓶中分别装入含酚酞的0.01 mol·L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质。
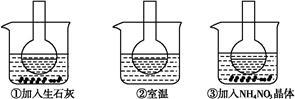
(1)含酚酞的0.01 mol·L-1 CH3COONa溶液显浅红色的原因为_______
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是_______ 。
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01 mol·L-1 CH3COONa溶液中分别加入少量浓盐酸、NaOH固体、Na2CO3固体、FeSO4固体,使CH3COO-水解平衡移动的方向分别为_______ 、_______ 、_______ 、_______ (填“左”、“右”或“不移动”)。

(1)含酚酞的0.01 mol·L-1 CH3COONa溶液显浅红色的原因为
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01 mol·L-1 CH3COONa溶液中分别加入少量浓盐酸、NaOH固体、Na2CO3固体、FeSO4固体,使CH3COO-水解平衡移动的方向分别为
您最近一年使用:0次
【推荐1】按要求完成下列问题:
(1)请用系统命名法给下列有机物命名:
①
___________
②
___________
(2)相对分子质量为72且沸点最低的烷烃的结构简式___________
(3)为抑制水解,实验室中配制FeCl3溶液时常加入___________ (填名称)。将FeCl3溶液和NaHCO3溶液混合,产生红褐色沉淀和无色气体,反应的离子方程式为___________ 。
(4)25℃时,pH均为5的醋酸和硫酸铝两种溶液中,由水电离出的c(H+)之比为___________ 。
(5)25℃时,Ksp(AgCl)=1.8×10-10.现将足量氯化银固体放入100 mL 0.2 mol·L-1 AgNO3溶液中,则溶液中氯离子的浓度为___________ mol·L-1(忽略溶液体积的变化)。
(1)请用系统命名法给下列有机物命名:
①

②

(2)相对分子质量为72且沸点最低的烷烃的结构简式
(3)为抑制水解,实验室中配制FeCl3溶液时常加入
(4)25℃时,pH均为5的醋酸和硫酸铝两种溶液中,由水电离出的c(H+)之比为
(5)25℃时,Ksp(AgCl)=1.8×10-10.现将足量氯化银固体放入100 mL 0.2 mol·L-1 AgNO3溶液中,则溶液中氯离子的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定温度下,在氯化银悬浊液中,存在如下平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),判断下表中加入不同物质的平衡移动情况及溶液中各项的变化。
| 外界条件 | 移动方向 | c(Ag+) | Ksp |
| 升高温度 | |||
| 加入少量AgNO3 | |||
| 加入Na2S | |||
| 通入HCl |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】电解质水溶液中存在各种行为,如电离、水解、沉淀溶解等,据所学知识回答下列问题:
(1)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中,a点对应的酸为___________ ;(填名称),该醋酸溶液稀释过程中,下列各量一定变小的是___________ 。(填序号)
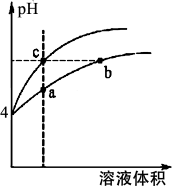
a.c(H+) b.c(OH-) c. d.
d.
(2)在t℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,则在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH=___________ 。
(3)25℃时,将 a mol·L-1的醋酸和 b mol·L-1的氢氧化钠溶液等体积混合后,溶液的pH=7,则a___________ b(填“>”、“<”或“=”),此时溶液中c(CH3COO-)+c(CH3COOH)=___________ mol·L-1(用字母表示)
(4)将AgCl分别放入:①5 mL水 ②10 mL 0.1 mol·L-1 MgCl2溶液 ③20 mL 0.5 mol·L-1 NaCl溶液 ④40 mL 0.3mol·L-1盐酸溶液中溶解至溶液饱和,各溶液中Ag+的浓度分别为a、b、 c、d,它们由大到小的排列顺序___________ (用字母表示)。
(1)某温度下,pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中,a点对应的酸为

a.c(H+) b.c(OH-) c.
 d.
d.
(2)在t℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,则在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH=
(3)25℃时,将 a mol·L-1的醋酸和 b mol·L-1的氢氧化钠溶液等体积混合后,溶液的pH=7,则a
(4)将AgCl分别放入:①5 mL水 ②10 mL 0.1 mol·L-1 MgCl2溶液 ③20 mL 0.5 mol·L-1 NaCl溶液 ④40 mL 0.3mol·L-1盐酸溶液中溶解至溶液饱和,各溶液中Ag+的浓度分别为a、b、 c、d,它们由大到小的排列顺序
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】沉淀溶解平衡在生活生产中有着重要应用.
(1)粗制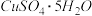 晶体中常含有杂质
晶体中常含有杂质 .
.
①在提纯时为了除去 ,常加入合适氧化剂,使
,常加入合适氧化剂,使 氧化为
氧化为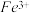 ,下列物质最好选用的是
,下列物质最好选用的是______ .
A.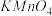
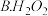
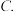 氯水
氯水 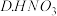
 然后再加入适当物质调整溶液至
然后再加入适当物质调整溶液至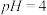 ,使
,使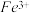 转化为
转化为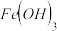 ,调整溶液pH可选用下列中的
,调整溶液pH可选用下列中的______ .
A.NaOH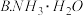


(2)在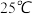 下,向浓度均为
下,向浓度均为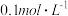 的
的 和
和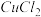 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成______ 沉淀 填化学式
填化学式 ,生成该沉淀的离子方程式为
,生成该沉淀的离子方程式为______  已知
已知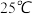 时
时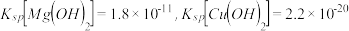 .
.
(3)向 溶液中加入
溶液中加入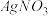 和KBr,当两种沉淀共存时,
和KBr,当两种沉淀共存时,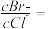
______ 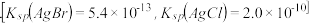
(4)向盛有1mL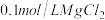 溶液的试管中滴加2滴
溶液的试管中滴加2滴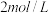 NaOH溶液,有白色沉淀生成,再滴加2滴
NaOH溶液,有白色沉淀生成,再滴加2滴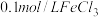 溶液,静置
溶液,静置 可以观察到的现象是
可以观察到的现象是______ ,产生该现象的原因是 用离子方程式表示
用离子方程式表示
______ 已知:Ksp[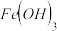 ]=4.0x10-38。
]=4.0x10-38。
(1)粗制
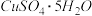 晶体中常含有杂质
晶体中常含有杂质 .
.①在提纯时为了除去
 ,常加入合适氧化剂,使
,常加入合适氧化剂,使 氧化为
氧化为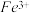 ,下列物质最好选用的是
,下列物质最好选用的是A.
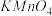
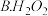
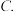 氯水
氯水 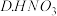
 然后再加入适当物质调整溶液至
然后再加入适当物质调整溶液至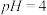 ,使
,使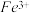 转化为
转化为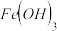 ,调整溶液pH可选用下列中的
,调整溶液pH可选用下列中的A.NaOH
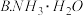


(2)在
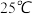 下,向浓度均为
下,向浓度均为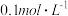 的
的 和
和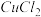 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成 填化学式
填化学式 ,生成该沉淀的离子方程式为
,生成该沉淀的离子方程式为 已知
已知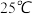 时
时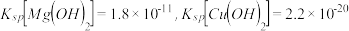 .
.(3)向
 溶液中加入
溶液中加入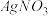 和KBr,当两种沉淀共存时,
和KBr,当两种沉淀共存时,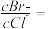
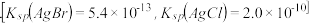
(4)向盛有1mL
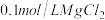 溶液的试管中滴加2滴
溶液的试管中滴加2滴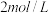 NaOH溶液,有白色沉淀生成,再滴加2滴
NaOH溶液,有白色沉淀生成,再滴加2滴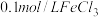 溶液,静置
溶液,静置 可以观察到的现象是
可以观察到的现象是 用离子方程式表示
用离子方程式表示
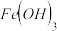 ]=4.0x10-38。
]=4.0x10-38。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空。
(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
为除去溶液中的Fe2+,可先加入_______ ,(从下面四个选项选择)将Fe2+氧化为Fe3+,反应的离子方程式为_______ ,然后加入适量的_______ (写化学式)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。
A.KMnO4 B.Cl2 C.浓硫酸 D.H2O2
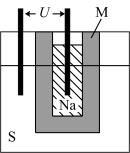
(2)如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS=Na2Sx,正极的电极反应式为_______ 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的_______ 倍。
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,当溶液pH=7时,溶液中各离子浓度由大到小的排列顺序是_______ 。
(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
为除去溶液中的Fe2+,可先加入
A.KMnO4 B.Cl2 C.浓硫酸 D.H2O2
(2)如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS=Na2Sx,正极的电极反应式为

(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,当溶液pH=7时,溶液中各离子浓度由大到小的排列顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组为探究沉淀溶解平衡的原理并测定某温度下PbI2溶度积常数,设计如下实验。
I.取100mL蒸馏水,加入过量的PbI2固体(黄色),搅拌,静置,过滤到洁净的烧杯中,得到滤液。
(1)搅拌的目的是___________________ 。
(2)取少量滤液于试管中,向其中滴加几滴0.1mol/LKI溶液,观察到的现象是________ ,溶液中c(Pb2+)_________ (填“增大”、“减小”或“不变”)。
Ⅱ.准确量取10.00mL滤液,与离子交换树脂(RH) 发生反应:2RH+Pb2+=R2Pb+2H+,交换完成后,流出溶液用中和滴定法测得n(H+)=3.000×10-5mol。
(3)在此实验温度下,PbI2的溶度积常数Ksp=_________ 。
(4)若步骤I盛装滤液的烧杯中有少量水,Ksp测定结果将会________ (填“偏大”、“偏小”或“无影响”)。
I.取100mL蒸馏水,加入过量的PbI2固体(黄色),搅拌,静置,过滤到洁净的烧杯中,得到滤液。
(1)搅拌的目的是
(2)取少量滤液于试管中,向其中滴加几滴0.1mol/LKI溶液,观察到的现象是
Ⅱ.准确量取10.00mL滤液,与离子交换树脂(RH) 发生反应:2RH+Pb2+=R2Pb+2H+,交换完成后,流出溶液用中和滴定法测得n(H+)=3.000×10-5mol。
(3)在此实验温度下,PbI2的溶度积常数Ksp=
(4)若步骤I盛装滤液的烧杯中有少量水,Ksp测定结果将会
您最近一年使用:0次



