水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。
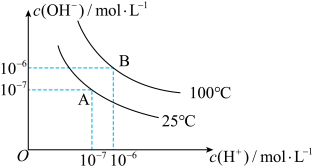
(1)100℃时1mol·L-1NaOH溶液中,由水电离出的c(H+)=_______ mol·L-1,Kw(25 ℃)_______ (填“>”“<”或“=”)Kw100℃。25 ℃时,向水的电离平衡体系中加入少量氢氧化钠固体,对水的电离平衡的影响是_______ (填“促进”“抑制”或“不影响”)。
(2)①已知室温下HA的电离平衡常数Ka=1×10-5,则100ml 0.1mol·L-1HA溶液中,HA的电离度为_______ 。
②若向该溶液中加入少量NaOH 固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,HA的电离平衡_______ (填“向左”、“向右”或“不”)移动。
③另取 10mL 的 HA 溶液,加入少量 NaA周体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(HA)的值将_______ (填“增大”“减小”或“无法确定”)。
(3)已知25 ℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0 mol·L-1,溶液中的c(OH-)=_______ mol·L-1。将SO2通入该氨水中,当c(OH-)降至1.0×10-7 mol·L-1时,溶液中的c(SO )/c(HSO
)/c(HSO )=
)=_______ 。

(1)100℃时1mol·L-1NaOH溶液中,由水电离出的c(H+)=
(2)①已知室温下HA的电离平衡常数Ka=1×10-5,则100ml 0.1mol·L-1HA溶液中,HA的电离度为
②若向该溶液中加入少量NaOH 固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,HA的电离平衡
③另取 10mL 的 HA 溶液,加入少量 NaA周体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(HA)的值将
(3)已知25 ℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0 mol·L-1,溶液中的c(OH-)=
 )/c(HSO
)/c(HSO )=
)=
更新时间:2022-12-02 13:31:11
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】I.已知水的电离平衡曲线如图所示:
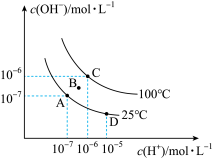
回答下列问题:
(1)图中C点水的离子积常数为___________ (mol·L-1)2。
(2)A、B、C、D四点KW的关系是___________ 。
(3)从A点到D点,可采取的措施是___________ 。
a.升温b.加入少量盐酸c.降温d.加入少量NaOH
Ⅱ.下表是不同温度下水的离子积数据:
试回答以下问题:
(4)若25<t1<t2,则a___________ (填“>”“<”或“=”)1×10-14。
(5)在t2℃,pH=10的NaOH溶液中,水电离产生的OH-浓度为___________ 。
(6)在t2℃下,其溶液的pH=7,则该溶液___________ (填字母)。
a.呈中性b.呈碱性c.呈酸性d.c(OH-)=100c(H+)
(7)25℃时,某Na2SO4溶液中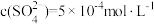 ,取该溶液1mL加水稀至10mL,则稀释后溶液中c(Na+):c(OH-)=
,取该溶液1mL加水稀至10mL,则稀释后溶液中c(Na+):c(OH-)=___________ 。

回答下列问题:
(1)图中C点水的离子积常数为
(2)A、B、C、D四点KW的关系是
(3)从A点到D点,可采取的措施是
a.升温b.加入少量盐酸c.降温d.加入少量NaOH
Ⅱ.下表是不同温度下水的离子积数据:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积KW | 1×10-14 | a | 1×10-12 |
(4)若25<t1<t2,则a
(5)在t2℃,pH=10的NaOH溶液中,水电离产生的OH-浓度为
(6)在t2℃下,其溶液的pH=7,则该溶液
a.呈中性b.呈碱性c.呈酸性d.c(OH-)=100c(H+)
(7)25℃时,某Na2SO4溶液中
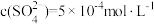 ,取该溶液1mL加水稀至10mL,则稀释后溶液中c(Na+):c(OH-)=
,取该溶液1mL加水稀至10mL,则稀释后溶液中c(Na+):c(OH-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】常温下,向100mL0.1molL-1H2S溶液中滴加0.1mol·L-1NaOH溶液。实验过程中,H2S溶液的pH与所滴加的NaOH溶液体积的关系如下图。
已知:H2S Ka1=1.3×10-7;Ka2=7.1×10-15
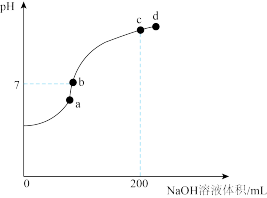
(1)b点所对应的NaOH溶液体积___________ 100mL(填“大于”、“等于”或“小于”)。
(2)a、b、c、d中,水的电离程度最大的是___________ (填字母代号)。
已知:H2S Ka1=1.3×10-7;Ka2=7.1×10-15

(1)b点所对应的NaOH溶液体积
(2)a、b、c、d中,水的电离程度最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。
甲:取纯度相同,质量、大小相等的锌粒放入两支试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按图装好,观察现象。
乙:用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH。
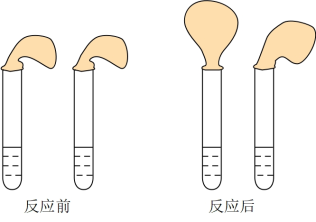
(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L﹣1的HA溶液的pH_______ 1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是_______ 。
A.装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol·L﹣1的HA溶液中,选择加入_______试剂。
(3)pH=2的盐酸和CH3COOH溶液各1mL,加入等体积的水稀释后HCl溶液中水电离出来的c(H+)_______ 醋酸溶液水电离出来的c(H+)(填“>”、“<”或“=”)。
(4)如表是不同温度下水的离子积数据:
试回答以下问题:
①25℃时,某Na2SO4溶液中c( )=5×10﹣4mol·L-1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+)∶c(OH﹣)=
)=5×10﹣4mol·L-1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+)∶c(OH﹣)=_______ 。
②在t1℃下,pH=8的NaOH溶液中,水电离产生的OH﹣浓度c(OH﹣)水=_______ ;pH=8的CH3COONa溶液中,水电离出来的c(OH﹣)水=_______ 。
(5)t1℃下,将pH=11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=_______ 。
甲:取纯度相同,质量、大小相等的锌粒放入两支试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按图装好,观察现象。
乙:用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH。

(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L﹣1的HA溶液的pH
A.装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol·L﹣1的HA溶液中,选择加入_______试剂。
| A.NaA固体(可完全溶于水) | B.1mol·L﹣1NaOH溶液 |
| C.1mol·L﹣1H2SO4 | D.2mol·L﹣1HA |
(4)如表是不同温度下水的离子积数据:
| 温度/℃ | 25 | t1 |
| 水的离子积Kw | 1×10﹣14 | 1×10﹣12 |
①25℃时,某Na2SO4溶液中c(
 )=5×10﹣4mol·L-1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+)∶c(OH﹣)=
)=5×10﹣4mol·L-1,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+)∶c(OH﹣)=②在t1℃下,pH=8的NaOH溶液中,水电离产生的OH﹣浓度c(OH﹣)水=
(5)t1℃下,将pH=11的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】水溶液中的离子平衡是中学学习的一个重要内容。
(1)下列溶液①0.10mol•L-1盐酸②0.10mol•L-1H2SO4溶液③0.10mol•L-1CH3COONa溶液④0.10mol•L-1NH4Cl溶液⑤0.10mol•L-1NaOH溶液,按pH由小到大顺序为____ (填序号)。
(2)在一定温度下,将一定质量冰醋酸加水稀释过程中溶液的导电能力变化如图所示。
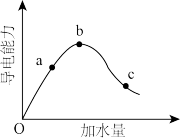
a、b、c三点对应的溶液中,CH3COOH电离程度最大的是____ ;a、b、c三点溶液用1mol•L-1NaOH溶液中和,消耗NaOH溶液体积大小关系____ 。
(3)已知25℃时,CO 水解反应的一级平衡常数Kh=2×10-4mol•L-1,写出此Kh的表达式
水解反应的一级平衡常数Kh=2×10-4mol•L-1,写出此Kh的表达式____ ;当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=___ 。
(4)SOCl2是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有雾形成,并有带刺激性气味气体溢出,该气体可使品红溶液褪色,请根据实验现象写出SOCl2和H2O反应的化学方程式:____ 。
(5)等浓度的盐酸、氨水中,由水电离出的H+浓度c盐酸(H+)____ c氨水(H+)(填“>”“<”或“=”)。在25℃下,将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合充分反应后溶液呈中性。则反应后溶液存在的离子浓度由大到小顺序为____ ,用含a的代数式表示NH3•H2O的电离常数Kb=____ 。
(1)下列溶液①0.10mol•L-1盐酸②0.10mol•L-1H2SO4溶液③0.10mol•L-1CH3COONa溶液④0.10mol•L-1NH4Cl溶液⑤0.10mol•L-1NaOH溶液,按pH由小到大顺序为
(2)在一定温度下,将一定质量冰醋酸加水稀释过程中溶液的导电能力变化如图所示。

a、b、c三点对应的溶液中,CH3COOH电离程度最大的是
(3)已知25℃时,CO
 水解反应的一级平衡常数Kh=2×10-4mol•L-1,写出此Kh的表达式
水解反应的一级平衡常数Kh=2×10-4mol•L-1,写出此Kh的表达式 ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=(4)SOCl2是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有雾形成,并有带刺激性气味气体溢出,该气体可使品红溶液褪色,请根据实验现象写出SOCl2和H2O反应的化学方程式:
(5)等浓度的盐酸、氨水中,由水电离出的H+浓度c盐酸(H+)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)25℃时,pH=3的盐酸中由水电离出的c(H+)为_______ 。
(2)99℃时,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。此时水的离子积Kw=_____ ,溶液中c(OH-)为_____ 。
(3)25℃时,a mol·L-1CH3COOH溶液的pH=b,用含a和b的代数式表示CH3COOH的电离平衡常数Ka=________ 。
(4)25℃时,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液呈___ (填“酸”、“中”或“碱”)性。
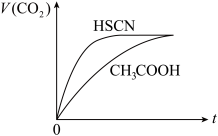
(5)25℃时,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13。该温度下将20mL 0.1mol·L-1CH3COOH溶液和20mL 0.1mol·L-1HSCN溶液分别与20mL 0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是_____________________________________________ 。
(1)25℃时,pH=3的盐酸中由水电离出的c(H+)为
(2)99℃时,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。此时水的离子积Kw=
(3)25℃时,a mol·L-1CH3COOH溶液的pH=b,用含a和b的代数式表示CH3COOH的电离平衡常数Ka=
(4)25℃时,pH=3的醋酸和pH=11的NaOH溶液等体积混合后,溶液呈
(5)25℃时,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13。该温度下将20mL 0.1mol·L-1CH3COOH溶液和20mL 0.1mol·L-1HSCN溶液分别与20mL 0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)常温下,将1mLpH=1的H2SO4溶液加水稀释到100ml,稀释后的溶液中 =
=______ 。
(2)某温度时,测得0.01mol/L的NaOH溶液的pH为11,则该温度下水的离子积常数KW=____ ,该温度______ (填“高于”或“低于”)25℃。
(3)在(2)所述温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸Vb L混合。
①若所得混合液为中性,且a =12,b=2,则Va :Vb=____________ 。
②若所得混合溶液的pH=l0,且a=12,b=2,则Va :Vb=____________ 。
(4)常温下,设pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5是Al2(SO4)3溶液中由水电离出的H+浓度为c2,则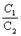 =
=________ 。
 =
=(2)某温度时,测得0.01mol/L的NaOH溶液的pH为11,则该温度下水的离子积常数KW=
(3)在(2)所述温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸Vb L混合。
①若所得混合液为中性,且a =12,b=2,则Va :Vb=
②若所得混合溶液的pH=l0,且a=12,b=2,则Va :Vb=
(4)常温下,设pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5是Al2(SO4)3溶液中由水电离出的H+浓度为c2,则
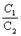 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】测得某温度下0.5mol·L-1 HNO2(亚硝酸)溶液的pH约为2。
(1)写出HNO2的电离方程式___ 。
(2)将溶液加水稀释至10倍后,c(NO2-)___ (填“增大”、“减小”或“不变”),n(H+)___ (填“增大”、“减小”或“不变”),pH区间范围是___ 。
A.1~2 B.2~3 C.3~4 D.4~5
(3)分别取同浓度同体积的盐酸与亚硝酸,以同样的操作与足量NaOH溶液反应,测得反应溶液的最高温度盐酸要高于亚硝酸,说明可能的原因___ 。
(4)0.1mol·L-1 NaNO2溶液pH___ 7(填“>”、“<”或“=”),溶液中含有___ 种分子,溶液中c(Na+)___ c(NO2-)(填“>”、“<”或“=”),下列措施能提高溶液中c(OH-)的是___ 。
A.适当升高温度 B.增加压强 C.加水 D.加入NH4Cl固体 E.加入Na2CO3固体
(1)写出HNO2的电离方程式
(2)将溶液加水稀释至10倍后,c(NO2-)
A.1~2 B.2~3 C.3~4 D.4~5
(3)分别取同浓度同体积的盐酸与亚硝酸,以同样的操作与足量NaOH溶液反应,测得反应溶液的最高温度盐酸要高于亚硝酸,说明可能的原因
(4)0.1mol·L-1 NaNO2溶液pH
A.适当升高温度 B.增加压强 C.加水 D.加入NH4Cl固体 E.加入Na2CO3固体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷能形成次磷酸(H3PO2)、亚磷酸(H3PO3)等多种含氧酸。
(1)次磷酸(H3PO2)属于元酸,是一种精细化工产品。设计一种实验方案,证明H3PO2是弱酸:____ 。(可选择的试剂为:0.1mol·L-1NaH2PO2溶液、0.1mol·L-1的H3PO2溶液、0.1ml·L-1的盐酸)
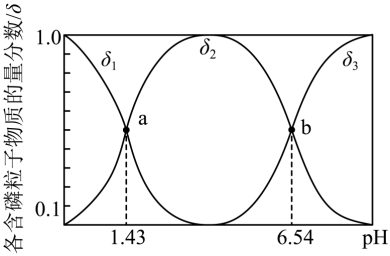
(2)亚磷酸(H3PO3)是二元弱酸,常温下向1L0.5mol·LH3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示:
①当溶液pH从6.54变为7时发生反应的离子方程式为____ 。
②Na2HPO3溶液显碱性,原因是(用离子方程式表示)____ 。
③室温下,H3PO3的电离平衡常数为Ka1和Ka2,则pKa2=____ (pKa2=lgKa2)。
④0.1mol·L-1NaH2PO3溶液中各离子浓度由大到小顺序为____ 。
(1)次磷酸(H3PO2)属于元酸,是一种精细化工产品。设计一种实验方案,证明H3PO2是弱酸:
(2)亚磷酸(H3PO3)是二元弱酸,常温下向1L0.5mol·LH3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示:

①当溶液pH从6.54变为7时发生反应的离子方程式为
②Na2HPO3溶液显碱性,原因是(用离子方程式表示)
③室温下,H3PO3的电离平衡常数为Ka1和Ka2,则pKa2=
④0.1mol·L-1NaH2PO3溶液中各离子浓度由大到小顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在氨水中存在下列电离平衡:NH3·H2O
 +OH-。
+OH-。
(1)下列情况能引起电离平衡正向移动的有___________ (填字母,下同)。
①加NH4Cl固体;②加NaOH溶液;③通入HCl;④加CH3COOH溶液;⑤加水;⑥加热至沸腾
(2)向含有酚酞的0.1 mol·L-1氨水中加入少量的NH4Cl晶体,则溶液颜色___________ 。
a.变蓝色 b.变深 c.变浅 d.不变
(3)向0.1 mol·L-1醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度(I)随加入氨水的体积(V)变化的曲线关系是下图中的___________。

 +OH-。
+OH-。(1)下列情况能引起电离平衡正向移动的有
①加NH4Cl固体;②加NaOH溶液;③通入HCl;④加CH3COOH溶液;⑤加水;⑥加热至沸腾
(2)向含有酚酞的0.1 mol·L-1氨水中加入少量的NH4Cl晶体,则溶液颜色
a.变蓝色 b.变深 c.变浅 d.不变
(3)向0.1 mol·L-1醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度(I)随加入氨水的体积(V)变化的曲线关系是下图中的___________。
A.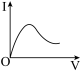 | B. | C.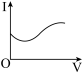 | D. |
您最近一年使用:0次



