H与O可以形成H2O和H2O2两种化合物。请回答:
(1)H+可与H2O形成H3O+,H3O+的空间构型名称为_____ 。
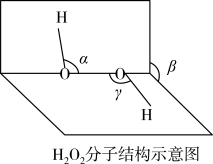
(2)H2O2分子结构如图所示,α、β、γ中相等的角是_____ ,H2O2是_____ 分子(填“极性”或“非极性”)。H2O2晶体中有4种作用力:①O-O键、②O-H键、③范德华力、④氢键,这4种作用力由强到弱依次为:_____ (用序号表示)。
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是_____ 。
A.Al3+ B.Mg2+ C.Cu2+ D.Mn2+ E.Fe2+
(4)实验测得,25℃时H2O2的pKa1小于H2O的pKa(pKa=-lgKa),原因是_____ (运用物质结构原理解释)。
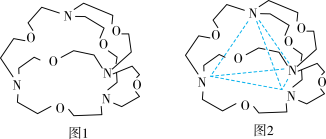
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是_____ (填标号)。
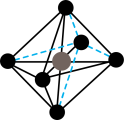
(6)SF6分子的空间结构为正八面体形,如图所示。1molSF6中含有_____ molS-F键,它的二氯代物SF4Cl2有_____ 种。
(1)H+可与H2O形成H3O+,H3O+的空间构型名称为
(2)H2O2分子结构如图所示,α、β、γ中相等的角是

(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是
A.Al3+ B.Mg2+ C.Cu2+ D.Mn2+ E.Fe2+
(4)实验测得,25℃时H2O2的pKa1小于H2O的pKa(pKa=-lgKa),原因是
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是

| A.CCl4 | B.CH4 | C.NH | D.H2O |

更新时间:2023-01-08 09:49:56
|
相似题推荐
【推荐1】X、Y、Z、W、Q、R均为元素周期表前4周期元素,原子序数依次增大,其相关信息如下:
请回答下列问题:
(1)元素X、Y、Z中:电负性由大到小的顺序为___________ (填元素符号,下同),第一电离能最大的为___________ 。
(2)基态W原子的价电子轨道表示式为___________ ,基态Q原子核外电子占据最高能级的电子云轮廓图为___________ 形。
(3)R在元素周期表中的位置是___________ ,属于___________ 区,基态R原子的电子排布式为___________ 。
| X元素的基态原子中,电子分布在三个不同的能级,且每个能级的电子总数相等 |
Y原子的 轨道有3个未成对电子 轨道有3个未成对电子 |
| Z元素的族序数是其周期数的3倍 |
W原子的第一至第六电离能分别为:      |
| Q为前4周期中电负性最小的元素 |
| R元素位于元素周期表的第11列 |
(1)元素X、Y、Z中:电负性由大到小的顺序为
(2)基态W原子的价电子轨道表示式为
(3)R在元素周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。
请回答下列问题:
(1)X、Y的元素符号依次是__ 、__ 。
(2)XZ2与YZ2分子的立体构型分别是_________ 和_________ ,相同条件下两者在水中的溶解度较大的是___ (写分子式)。
(3)Q的元素符号是__ ,它属于第___ 周期,它的核外电子排布式为___ ,在形成化合物时它的最高化合价为__ 。
(4)Y、Z、E三种元素原子的第一电离能由大到小的顺序是_________ 。(用元素符号表示)
请回答下列问题:
(1)X、Y的元素符号依次是
(2)XZ2与YZ2分子的立体构型分别是
(3)Q的元素符号是
(4)Y、Z、E三种元素原子的第一电离能由大到小的顺序是
您最近一年使用:0次
【推荐3】W、X、Y、Z四种短周期元素的原子序数W>X>Z>Y。X原子的最外层没有p电子,Y原子最外层s电子与p电子数之比为1∶1,W与Z原子核外s电子与p电子数之比均为1∶1。则:
(1)写出各元素的元素符号:W:________ 、X:________ 、Y:________ 、Z:________ 。
(2)四种元素原子半径大小顺序依次为____________________________________ 。
(3)W、X元素最高价氧化物对应水化物的碱性强弱为________________________ (用化学式表示)。
(1)写出各元素的元素符号:W:
(2)四种元素原子半径大小顺序依次为
(3)W、X元素最高价氧化物对应水化物的碱性强弱为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】构成物质的微粒种类及相互间的作用力是影响物质性质的主要因素。
(1)已知:H与O可以形成H2O和H2O2两种化合物。
①H2O内O-H(a)、水分子间的范德华力(b)和氢键(c),从强到弱的顺序为______ 。(用a、b、c表示)。H+可与H2O形成H3O+,H3O+中H-O-H的键角比H2O中的大,原因是______ 。
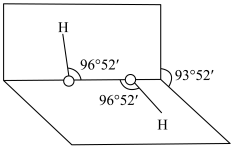
②H2O2是常用的氧化剂,分子结构如图所示。
i.H2O2的电子式是______ 。
ii.下列关于H2O2的说法中正确的是______ (填序号)。。
a.分子中含有极性键和非极性键
b.氧原子的轨道发生了sp3杂化
c.分子是非极性分子
iii.H2O2易溶于水,难溶于CC14,主要原因是______ 。
(2)已知:在一定条件下,十八胺具有一定的还原性,不同的金属盐与十八胺体系反应可以得到不同的产物,产物的差异与金属离子获得电子的能力有关。
表1部分金属元素的电负性
表2单一金属盐与十八胺体系反应得到的产物
①请结合上述信息,分析不同的金属盐与十八胺体系反应得到不同类型产物的原因:Zn、Co、Ni元素电负性相对较小,获得电子的能力相对较弱,在反应中未发生元素化合价的变化,得到金属氧化物:______ 。
②Co2+和Pd2+盐混合后再与十八胺体系反应得到金属间化合物CoPd2.该化合物中Co原子与Pd原子间的作用力是______ (填“离子键”或“共价键”),依据表1信息写出判断理由______ 。
③Pt4+盐与十八胺体系的反应与上述反应类似。请推测单一Pt4+盐与十八胺体系的反应的产物是______ 。
(1)已知:H与O可以形成H2O和H2O2两种化合物。
①H2O内O-H(a)、水分子间的范德华力(b)和氢键(c),从强到弱的顺序为
②H2O2是常用的氧化剂,分子结构如图所示。

i.H2O2的电子式是
ii.下列关于H2O2的说法中正确的是
a.分子中含有极性键和非极性键
b.氧原子的轨道发生了sp3杂化
c.分子是非极性分子
iii.H2O2易溶于水,难溶于CC14,主要原因是
(2)已知:在一定条件下,十八胺具有一定的还原性,不同的金属盐与十八胺体系反应可以得到不同的产物,产物的差异与金属离子获得电子的能力有关。
表1部分金属元素的电负性
| 金属元素 | Zn | Co | Ni | Ag | Pd | Pt |
| 电负性 | 1.65 | 1.88 | 1.91 | 1.93 | 2.2 | 2.2 |
| 金属盐中的金属离子 | Zn2+ | Co2+ | Ni2+ | Ag+ | Pd2+ |
| 反应产物 | ZnO | CoO | NiO | Ag | Pd |
②Co2+和Pd2+盐混合后再与十八胺体系反应得到金属间化合物CoPd2.该化合物中Co原子与Pd原子间的作用力是
③Pt4+盐与十八胺体系的反应与上述反应类似。请推测单一Pt4+盐与十八胺体系的反应的产物是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】Mn是元素周期表中第25号元素,它的氧化物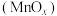 可用于催化醇的氧化氰化,反应如下:
可用于催化醇的氧化氰化,反应如下:
(1)组成物质Ⅰ的元素中,电负性最大是_____ (填元素符号)。
(2)物质Ⅱ中C原子的杂化轨道类型有_____ ; 该分子中含有
该分子中含有 键
键_____ mol。
(3) 的VSEPR模型为
的VSEPR模型为_____ ;已知 ,但该反应不及Na与
,但该反应不及Na与 的反应剧烈,从共价键的角度分析,可能的原因是
的反应剧烈,从共价键的角度分析,可能的原因是_____ 。
(4)Mn元素在周期表中的位置是_____ ;基态Mn原子的核外电子有_____ 种空间运动状态。
(5)某种 晶体的晶胞如下图所示,该晶体中Mn元素的化合价为
晶体的晶胞如下图所示,该晶体中Mn元素的化合价为_____ 。已知该晶胞底面是边长为 的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为
的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为 、
、 、
、 ,则Mn与O形成化学键的键长为
,则Mn与O形成化学键的键长为_____ cm(用含a、m、n的代数式表示)。
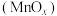 可用于催化醇的氧化氰化,反应如下:
可用于催化醇的氧化氰化,反应如下: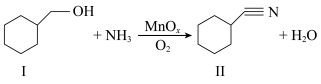
(1)组成物质Ⅰ的元素中,电负性最大是
(2)物质Ⅱ中C原子的杂化轨道类型有
 该分子中含有
该分子中含有 键
键(3)
 的VSEPR模型为
的VSEPR模型为 ,但该反应不及Na与
,但该反应不及Na与 的反应剧烈,从共价键的角度分析,可能的原因是
的反应剧烈,从共价键的角度分析,可能的原因是(4)Mn元素在周期表中的位置是
(5)某种
 晶体的晶胞如下图所示,该晶体中Mn元素的化合价为
晶体的晶胞如下图所示,该晶体中Mn元素的化合价为 的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为
的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为 、
、 、
、 ,则Mn与O形成化学键的键长为
,则Mn与O形成化学键的键长为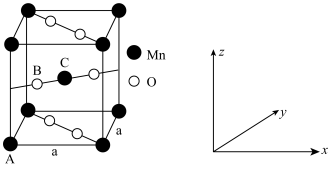
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】工业上以氯化钾和钛白厂的副产品硫酸亚铁为原料可得到硫酸钾、过二硫酸钠和铁红颜料等产品,该方法原料的综合利用率较高。
(1)原子序数为22基态钛原子的核外电子排布式为___________________________ 。
(2)TiCl4在常温下是一种无色液体,而FeCl3可用升华法提纯,则两种氯化物均属于__________ 晶体。
(3)SO42-和 S2O82-(过二硫酸根)结构中,硫原子均位于由氧原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。下列说法正确的是________________ 。
A. SO42-中存在σ键和π键且与PO43-离子互为等电子体
B.S2O82-中存在非极性键且有强氧化性
C.S2O82-比SO42-稳定且两者的氧元素的化合价相同
(4)KCl与MgO的晶体结构跟NaCl的晶体结构相似,则KCl与MgO两者中熔点高的是_________ ,原因是___________________________________________________ 。
(5)硫与氯可形成化合物SCl2,则该分子中硫原子的杂化方式为_____ ,分子的空间构型为__________________________________ 。
(6)在一定条件下铁形成的晶体的基本结构单元如下图1和图2所示,则图1和图2的结构中铁原子的配位数之比为____________ 。

(1)原子序数为22基态钛原子的核外电子排布式为
(2)TiCl4在常温下是一种无色液体,而FeCl3可用升华法提纯,则两种氯化物均属于
(3)SO42-和 S2O82-(过二硫酸根)结构中,硫原子均位于由氧原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。下列说法正确的是
A. SO42-中存在σ键和π键且与PO43-离子互为等电子体
B.S2O82-中存在非极性键且有强氧化性
C.S2O82-比SO42-稳定且两者的氧元素的化合价相同
(4)KCl与MgO的晶体结构跟NaCl的晶体结构相似,则KCl与MgO两者中熔点高的是
(5)硫与氯可形成化合物SCl2,则该分子中硫原子的杂化方式为
(6)在一定条件下铁形成的晶体的基本结构单元如下图1和图2所示,则图1和图2的结构中铁原子的配位数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】现有①SO2②SO3③SO32-④SO42-四种粒子,回答下列问题:
(1)其中中心原子S的杂化方式为sp2的是__ (填序号,下同);中心原子S的杂化方式为sp3的是_________ .
(2)SO2在水中的溶解度比较大,原因是_____________ 。
(3)下列对H2SO3和H2SO4的说法正确的是_____ (填字母)。
A.H2SO4比H2SO3易电离出H+是因为H2SO4分子中的非羟基氧多
B.H2SO4比H2SO3易电离出H+是因为H2SO4分子中中心原子S的孤电子对少
C.在H2SO4溶液中存在的粒子的空间构型有V形和正四面体形
(4)若丁二烯CH2=CH-CH=CH2中除含σ键外,还含有一个Π44键(Πmn键表示n个原子、m个电子组成的大п键),SO2含有大п键,可表示为___________ 。
(1)其中中心原子S的杂化方式为sp2的是
(2)SO2在水中的溶解度比较大,原因是
(3)下列对H2SO3和H2SO4的说法正确的是
A.H2SO4比H2SO3易电离出H+是因为H2SO4分子中的非羟基氧多
B.H2SO4比H2SO3易电离出H+是因为H2SO4分子中中心原子S的孤电子对少
C.在H2SO4溶液中存在的粒子的空间构型有V形和正四面体形
(4)若丁二烯CH2=CH-CH=CH2中除含σ键外,还含有一个Π44键(Πmn键表示n个原子、m个电子组成的大п键),SO2含有大п键,可表示为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
(1)写出B原子的电子排布式__________
(2)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为__________ ,简要描述该配合物中化学键的成键情况:__________
(3)“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。
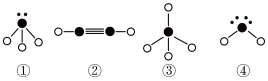
则在以上分子中,中心原子采用sp3杂化形成化学键的是__________ (填序号);在②的分子中有__________ 个σ键和__________ 个π键
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:
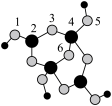
在Xm-中,硼原子轨道的杂化类型有__________ ;配位键存在于__________ 原子之间(填原子的数字标号);m=__________ (填数字)
(5)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的化学式为__________ ,第二种配合物的化学式为_________ .
| 元素 | A | B | C | D |
| 性质结构信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(2)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为
(3)“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。

则在以上分子中,中心原子采用sp3杂化形成化学键的是
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:

在Xm-中,硼原子轨道的杂化类型有
(5)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铬锆铜(CuCrZr)合金广泛应用于机械制造工业的焊接。已知锆(40Zr)位于第IVB族,根据要求回答下列问题:
(1)铜元素在元素周期表的分区为___________ 。基态Cr原子的价电子排布图(即轨道排布式)为___________ 。
(2)将硫酸铜固体溶于水中,呈天蓝色,该天蓝色离子的结构式为___________ , 的空间构型为
的空间构型为___________ (用文字描述)。
(3)K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________ 。
(4)晶体具有自范性及各向异性等特点,造成某些物理性质的各向异性最本质原因是___________ ,铜与氯形成晶体的晶胞如图所示,该晶体的化学式为___________ 已知晶胞边长为anm,NA为阿伏加德罗常数的值,该晶体的密度为___________ g·cm-3。
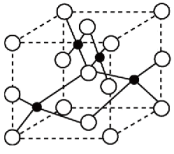
(5)火法炼铜中, ,
,___________ 元素被氧化。(填元素符号)
(1)铜元素在元素周期表的分区为
(2)将硫酸铜固体溶于水中,呈天蓝色,该天蓝色离子的结构式为
 的空间构型为
的空间构型为(3)K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是
(4)晶体具有自范性及各向异性等特点,造成某些物理性质的各向异性最本质原因是

(5)火法炼铜中,
 ,
,
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】A为短周期元素,A-F6种元素在元素周期表中的位置如图所示,其中A的基态原子的能层序数与最外基电子数相等。回答下列问题(请用元素符号表示相关化学式):
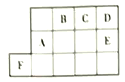
(1)F的价电于排布式为_______________ 。
(2)B、C、D原子的电负性由大到小的顺序是_______________ 。
(3)化合物BE2微溶于水,为______ (填“极性“成“非极性”)分子,BE2______ (填“能”或“不能”)分离常见的B的单质和正的单质的混合物。
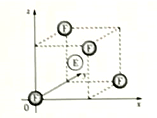
(4)下图为FE晶胞的一部分,F原子的周围最近的E原子有__ 个;若FE晶胞参数为a,作为数轴单位,在坐标原点的F原于坐标参数记为(0,0,0),则图中E原子的坐标参数为____ 。

(1)F的价电于排布式为
(2)B、C、D原子的电负性由大到小的顺序是
(3)化合物BE2微溶于水,为
(4)下图为FE晶胞的一部分,F原子的周围最近的E原子有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硒(Se)是一种有重要作用的元素,可以形成多种化合物。
(1)基态硒原子的简化电子排布式为
(2)H2SeO3的中心原子杂化类型是
 的空间结构是
的空间结构是(3)H2Se属于
(4)H2O中的H-O-H键角比H2Se中H-Se-H键角
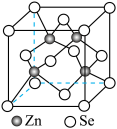
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A、B、C、D、E、F为前4周期的6种元素,原子序数依次增大,其中A位于周期表中s区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层电子数的3倍;F元素位于元素周期表的第4行、第11列。试回答下列问题:
(1)基态F原子的核外电子排布式为____ 。
(2)下列关于B2A2的说法中正确的是____ (填选项序号)
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是含极性键和非极性键的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序为___ (用元素符号表示),写出元素C基态原子的价电子排布图:____ 。
(4)C的简单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有___ (填选项符号)。
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为___ ;B和E的最高价氧化物中,熔沸点较高的是___ (写化学式)。
(1)基态F原子的核外电子排布式为
(2)下列关于B2A2的说法中正确的是
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是含极性键和非极性键的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序为
(4)C的简单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为
您最近一年使用:0次



