设NA为阿伏加德罗常数的值,下列关于常温下pH=2的H2C2O4溶液的说法错误的是
| A.1L该溶液中的H+数目为0.01NA |
B.c(H+)=c( )+ 2c( )+ 2c( )+c(OH-) )+c(OH-) |
| C.加水稀释,溶液pH增大 |
| D.加入NaHC2O4固体,溶液酸性增强 |
更新时间:2021/01/31 16:36:31
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.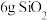 中含有O原子的数目为 中含有O原子的数目为 |
B.标准状况下,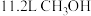 中含有的原子总数为 中含有的原子总数为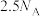 |
C.常温下,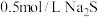 溶液中 溶液中 数目小于 数目小于 |
D.一定条件下,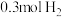 和 和 充分反应后转移电子总数为 充分反应后转移电子总数为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于0.1 mol/L KNO3溶液的叙述中,正确的是
| A.1 L该溶液中含KNO3 101 g |
| B.100 mL该溶液中含KNO3 0.01 mol |
| C.从1 L该溶液中取出500 mL后,剩余溶液的浓度为0.05 mol/L |
| D.1 L水中溶解0.1mol KNO3,即可配得0.1mol/L KNO3溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】紫罗兰含色素HZ在水溶液中存在平衡:HZ(红) H+ +Z- (蓝色)。将HZ溶液滴入稀硫酸中,溶液的颜色为
H+ +Z- (蓝色)。将HZ溶液滴入稀硫酸中,溶液的颜色为
 H+ +Z- (蓝色)。将HZ溶液滴入稀硫酸中,溶液的颜色为
H+ +Z- (蓝色)。将HZ溶液滴入稀硫酸中,溶液的颜色为| A.紫色 | B.红色 | C.蓝色 | D.无色 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】25℃,相同pH、相同体积的盐酸和醋酸溶液分别加水稀释,pH随溶液体积的变化如图所示。下列判断正确的是
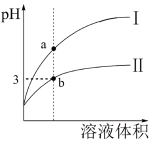

| A.Ⅰ为醋酸稀释时的pH变化 | B.未稀释时两溶液的导电能力不同 |
| C.b点水电离的c(H+)=1×10-11mol/L | D.a、b两点酸溶液的浓度相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】向0.1 mol·L-1 CH3COOH溶液中加入少量的CH3COONa晶体时,会引起
| A.溶液的pH增大 | B.溶液中的c(H+)增大 |
| C.溶液的导电能力减弱 | D.溶液中的c(CH3COO-)减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】25℃时,下列有关电解质溶液的说法正确的是( )
A.加水稀释0.1mol/L氨水,溶液中c(H+)·c(OH-)和 均不变 均不变 |
| B.配制Fe(NO3)2溶液时,为了防止Fe2+水解可向溶液中加入适量的稀硝酸 |
C.向盐酸中滴加氨水至溶液呈中性,所得溶液中c(NH )=c(Cl-) )=c(Cl-) |
| D.向CH3COOH溶液中加入少量CH3COONa固体,溶液的pH降低 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】t℃时,向20.00mL 0.1 mol•L-1 H2X(H2X为二元弱酸)溶液中滴入0.1mol•L-1NaOH溶液,溶液中由水电离出的c水(OH-)的负对数[-lgc水(OH-)]与所加NaOH溶液体积的关系如图所示,下列说法中不正确的是
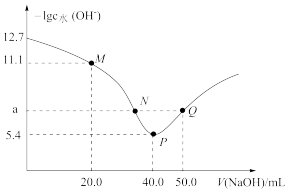

| A.水的电离程度:P>N=Q>M,且a=7 |
| B.图中M、P、Q三点对应溶液中c(HX-)/c(X2-)不相等 |
| C.M点溶液中:c(Na+)>c(HX-)>c(H2X) |
| D.P点溶液中c(OH-)=c(H+)+c(HX-)+2c(H2X) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法中正确的是
A.常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c( )、c(H+)均下降 )、c(H+)均下降 |
B.pH=8.3的NaHCO3溶液:c(Na+)>c( )>c( )>c( )>c(H2CO3) )>c(H2CO3) |
C.常温下,c( )相等的①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ )相等的①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
D.当溶液中存在的离子只有Cl-、OH-、 、H+时,该溶液中离子浓度大小关系可能为c(Cl-)>c( 、H+时,该溶液中离子浓度大小关系可能为c(Cl-)>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
您最近一年使用:0次

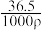
 H++Ac-的电离平衡中,要使电离平衡向左移动,应采取的措施是
H++Ac-的电离平衡中,要使电离平衡向左移动,应采取的措施是 稀溶液进行下列操作,一定可使
稀溶液进行下列操作,一定可使 增大的是
增大的是

 +H2O
+H2O )+c(OH-)
)+c(OH-)

