乙烯氢化的热化学方程式为C2H4(g) + H2(g) = C2H6(g) △H= akJ·mol-1,使用不同含Au催化剂的反应历程如图所示,下列说法正确的是
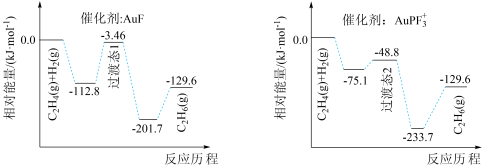

| A.1 mol C2H6(g)的能量大于 1 mol C2H4(g)与1 mol H2(g)具有的能量之和 |
| B.该反应的焓变:△H = -129.6 kJ·mol-1 |
| C.过渡态物质的稳定性:过渡态1大于过渡态2 |
D.相应的活化能:催化剂AuF小于催化剂AuPF |
22-23高三下·浙江·阶段练习 查看更多[4]
黑龙江省佳木斯市三校联考2023-2024学年高三上学期第三次调研考试化学试题浙江省杭州市等4地宁波市鄞州高级中学等2校2023届高三下学期二模考试化学试题(已下线)化学-2023年高考押题预测卷01(浙江卷)(含考试版、全解全析、参考答案、答题卡)浙江省浙里卷天下2022-2023学年高三百校联考3月测试化学试题
更新时间:2023-03-12 18:25:12
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.电解精炼铜时,阳极泥中含有 等金属 等金属 |
B. 通入足量水中,转移电子的数目为 通入足量水中,转移电子的数目为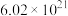 |
C.反应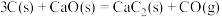 在常温下不能自发进行,说明该反应的 在常温下不能自发进行,说明该反应的 |
| D.等质量的硫蒸气和硫粉分别在空气中完全燃烧,前者放出热量多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:①101kPa时,C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH1=-1323kJ·mol-1②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3kJ·mol-1,下列说法正确的是
| A.1molC2H4(g)的能量比2molCO2(g)和2molH2O(g)的高 |
| B.表示C2H4燃烧热的热化学反应方程式中ΔH=-QkJ·mol-1,Q大于1323 |
| C.98%的浓硫酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |
| D.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH<ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】1,2-丙二醇(CH2OHCHOHCH3)单分子解离反应相对能量如图所示。路径包括碳碳键断裂解离和脱水过程。下列说法正确的是
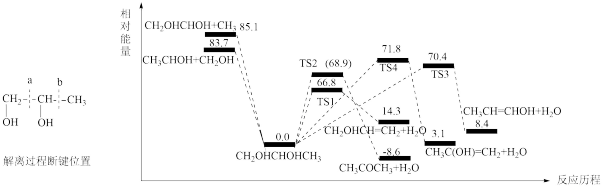

| A.解离过程中,断裂a处碳碳键比b处碳碳键所需能量高 |
| B.1,2-丙二醇单分子脱水过程均为吸热反应 |
| C.从能量的角度分析,TS1、TS2、TS3、TS4四种路径中TS4路径的速率最慢 |
| D.脱水生成的四种产物中,丙烯醇[CH3C(OH)=CH2]最稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知如下化学键的键能:
则下列热化学方程式不 正确的是
| 化学键 | H—H | Cl—Cl | H—Cl |
| 生成1 mol化学键时放出的能量 | 436kJ/mol | 243kJ/mol | 431kJ/mol |
A. H2(g)+ H2(g)+ Cl2(g)=HCl(g) ΔH=-91.5kJ/mol Cl2(g)=HCl(g) ΔH=-91.5kJ/mol |
| B.H2(g)+Cl2(g)=2HCl(g) ΔH=-183kJ/mol |
| C.2HCl(g)=H2(g)+Cl2(g) ΔH=+183kJ/mol |
D. H2(g)+ H2(g)+ Cl2(g)=HCl(g) ΔH=+91.5kJ/mol Cl2(g)=HCl(g) ΔH=+91.5kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】铁的配合物离子(用[L-Fe-H]+表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
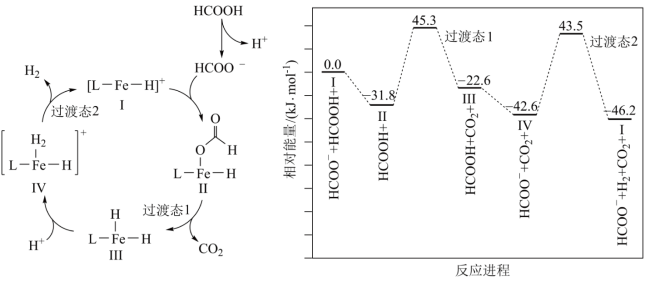
下列说法错误的是

下列说法错误的是
A.该过程总反应为 |
| B.H+浓度过大或者过小,均导致反应速率降低 |
C.该催化循环中 元素的化合价未发生变化 元素的化合价未发生变化 |
| D.该过程的总反应速率由IV→I步骤决定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用钛(Ru)基催化剂催化CO2(g)和H2(g)反应生成2mol液态HCOOH放出62.4kJ热量的图示如图,下列说法正确的是
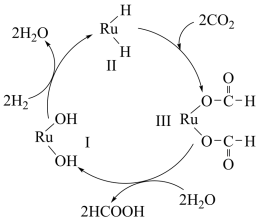

| A.图示中物质Ⅱ为该反应的催化剂 |
| B.图示中参与循环的物质只有CO2和H2 |
| C.该反应的活化能为62.4kJ•mol-1 |
| D.该反应的热化学方程式为H2(g)+CO2(g)=HCOOH(l) △H=-31.2kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验内容 | 实验结论 |
| A | 向两支试管中各加入2 mL 0.1 mol/L Na2S2O3溶液,分别放入盛有冷水和热水的两个烧杯中,再同时分别向两支试管中加入2 mL 0.1 mol/L H2SO4溶液,振荡,观察现象 | 探究温度对化学反应速率的影响 |
| B | 取两支试管,分别加入4 mL 0.01 mol/L KMnO4酸性溶液,然后向一支试管中加入0.01 mol/L H2C2O4溶液2 mL,向另一支试管中加入0.01 mol/L H2C2O4溶液4 mL,第一支试管中褪色时间长 | H2C2O4浓度越大,反应速率越快 |
| C | 取两支试管,分别加入等体积等浓度的双氧水,然后试管①中加入0.01 mol/L FeCl3溶液2 mL,向试管②中加入0.01 mol/L CuCl2溶液2 mL,试管①产生气泡快 | 加入FeCl3时,双氧水分解反应的活化能较大 |
| D | 检验FeCl2溶液中是否含有Fe2+时,将溶液滴入酸性KMnO4溶液,溶液紫红色褪去 | 能证明溶液中含有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国科技成就日新月异。下列对我国最新科技成就的化学解读正确的是
| 科技成就 | 化学解读 | |
| A | 利用足球烯(C60)合成亚晶态金刚石 | 足球烯和亚晶态金刚石互为同系物 |
| B | 合成介孔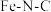 催化剂提升锌-空气电池性能 催化剂提升锌-空气电池性能 | 该电池放电时可将化学能100%转化成电能 |
| C | 构建新型催化剂高效、环保地将乙烷转化成乙烯 | 其他条件相同时,催化剂能加快反应的速率 |
| D | 发现能有效降解聚乙烯、聚苯乙烯等多种塑料的海洋真菌 | 在海洋真菌作用下,温度越高,聚乙烯、聚苯乙烯等塑料降解速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】氢能是一种极具发展潜能的清洁能源。对于可逆反应:
 ,在容积恒为2L的密闭容器中,将2.0molC0与8.0molH2混合加热到830℃发生上述反应,5min时达到平衡,CO的转化率是80%。实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以增大H2的体积分数。选用相同质量、不同粒径的CaO固体进行实验时,对比实验的结果如图所示。下列叙述中错误的是
,在容积恒为2L的密闭容器中,将2.0molC0与8.0molH2混合加热到830℃发生上述反应,5min时达到平衡,CO的转化率是80%。实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以增大H2的体积分数。选用相同质量、不同粒径的CaO固体进行实验时,对比实验的结果如图所示。下列叙述中错误的是

 ,在容积恒为2L的密闭容器中,将2.0molC0与8.0molH2混合加热到830℃发生上述反应,5min时达到平衡,CO的转化率是80%。实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以增大H2的体积分数。选用相同质量、不同粒径的CaO固体进行实验时,对比实验的结果如图所示。下列叙述中错误的是
,在容积恒为2L的密闭容器中,将2.0molC0与8.0molH2混合加热到830℃发生上述反应,5min时达到平衡,CO的转化率是80%。实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以增大H2的体积分数。选用相同质量、不同粒径的CaO固体进行实验时,对比实验的结果如图所示。下列叙述中错误的是
| A.微米CaO和纳米CaO对平衡影响不同主要是CaO作为催化剂表面积越大,反应的速率越快 |
B.在生产中,增大 的用量可同时提高CO的转化率和 的用量可同时提高CO的转化率和 的产率 的产率 |
C.5min内的平均反应速率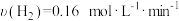 |
| D.平衡时间容器中通入He增大压强,平衡不移动 |
您最近一年使用:0次

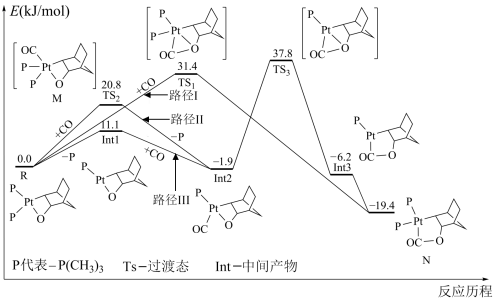
 的C-H键形成高氧化态过渡金属化合物的反应频繁出现在光分解作用、金属有机化学等领域,如图是
的C-H键形成高氧化态过渡金属化合物的反应频繁出现在光分解作用、金属有机化学等领域,如图是
 状态最稳定
状态最稳定
 活化能为
活化能为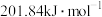
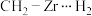 →状态2反应决定
→状态2反应决定