锂、铍等金属广泛应用于航空航天、核能和新能源汽车等高新产业。一种从萤石矿(主要含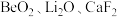 及少量
及少量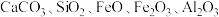 )中提取铍的工艺如图所示:
)中提取铍的工艺如图所示:
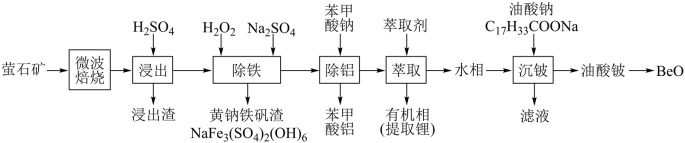
已知:苯甲酸是一元弱酸,白色片状晶体,常温下微溶于水,温度升高,溶解度增大。
回答下列问题:
(1)“微波焙烧”使矿物内部变得疏松多孔,目的是_______ 。
(2)由油酸铍制备 的方法是
的方法是_______ 。
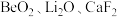 及少量
及少量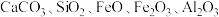 )中提取铍的工艺如图所示:
)中提取铍的工艺如图所示:
已知:苯甲酸是一元弱酸,白色片状晶体,常温下微溶于水,温度升高,溶解度增大。
回答下列问题:
(1)“微波焙烧”使矿物内部变得疏松多孔,目的是
(2)由油酸铍制备
 的方法是
的方法是
2023高三·全国·专题练习 查看更多[1]
(已下线)第二部分 工业生产流程 热点1 原料处理及操作目的
更新时间:2023-03-14 14:14:35
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某含镍 废料中有FeO、
废料中有FeO、 、MgO、
、MgO、 等杂质,用此废料提取
等杂质,用此废料提取 的工艺流程如图1:
的工艺流程如图1:

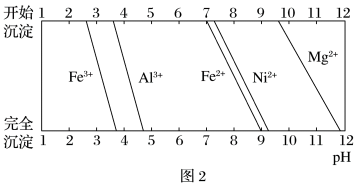
已知:①有关金属离子生成氢氧化物沉淀所需的pH如图.
② 时,
时,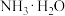 的电离常数
的电离常数 的电离常数
的电离常数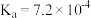 ,
,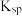
 .
.
(1)加 调节溶液的pH至5,得到废渣2的主要成分是
调节溶液的pH至5,得到废渣2的主要成分是______  填化学式
填化学式 .
.
(2)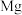 能与饱和
能与饱和 溶液反应产生
溶液反应产生 ,请用化学平衡移动原理解释
,请用化学平衡移动原理解释 用必要的文字和离子方程式回答
用必要的文字和离子方程式回答
______ .
(3) 时,
时,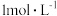 的NaF溶液中
的NaF溶液中
______ 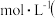 列出计算式即可
列出计算式即可 溶液呈
溶液呈______  填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” .
.
(4)已知沉淀前溶液中 ,当除镁率达到
,当除镁率达到 时,溶液中
时,溶液中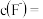
______  .
.
(5)在NaOH溶液中用NaClO与 反应可得
反应可得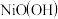 ,化学方程式为
,化学方程式为____________ ;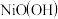 与贮氢的镧镍合金可组成镍氢碱性电池
与贮氢的镧镍合金可组成镍氢碱性电池 溶液
溶液 ,工作原理为:
,工作原理为: ,负极的电极反应式:
,负极的电极反应式:______ .
 废料中有FeO、
废料中有FeO、 、MgO、
、MgO、 等杂质,用此废料提取
等杂质,用此废料提取 的工艺流程如图1:
的工艺流程如图1:

已知:①有关金属离子生成氢氧化物沉淀所需的pH如图.
②
 时,
时,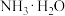 的电离常数
的电离常数 的电离常数
的电离常数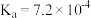 ,
,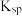
 .
.(1)加
 调节溶液的pH至5,得到废渣2的主要成分是
调节溶液的pH至5,得到废渣2的主要成分是 填化学式
填化学式 .
.(2)
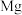 能与饱和
能与饱和 溶液反应产生
溶液反应产生 ,请用化学平衡移动原理解释
,请用化学平衡移动原理解释 用必要的文字和离子方程式回答
用必要的文字和离子方程式回答
(3)
 时,
时,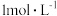 的NaF溶液中
的NaF溶液中
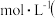 列出计算式即可
列出计算式即可 溶液呈
溶液呈 填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” .
.(4)已知沉淀前溶液中
 ,当除镁率达到
,当除镁率达到 时,溶液中
时,溶液中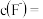
 .
.(5)在NaOH溶液中用NaClO与
 反应可得
反应可得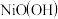 ,化学方程式为
,化学方程式为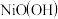 与贮氢的镧镍合金可组成镍氢碱性电池
与贮氢的镧镍合金可组成镍氢碱性电池 溶液
溶液 ,工作原理为:
,工作原理为: ,负极的电极反应式:
,负极的电极反应式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】废旧电池的回收利用既节约了资源,又可以减少污染。某型号锂电池的电池芯中含有LiCoO2及金属Al、Fe、Cu等,它的一种金属的回收工艺如图。

已知:高价钻离子在过程2被还原。
回答下列问题:
(1)LiCoO2中Co元素的化合价是_______ ,电池芯先要经过粉碎处理,目的是_______ 。
(2)过程3发生反应的离子方程式是_______ ,试从平衡的角度解释调节pH能产生Fe(OH)3沉淀的原因_______ (用离子方程式表达)
(3)过程5所用的分离方法是_______ 、_______ 。
(4)已知Co的活泼性在Fe、Sn之间,由CoC2O4到Co所发生的两步反应依次是CoC2O4 CoO+CO↑+CO2↑和
CoO+CO↑+CO2↑和_______ 。

已知:高价钻离子在过程2被还原。
回答下列问题:
(1)LiCoO2中Co元素的化合价是
(2)过程3发生反应的离子方程式是
(3)过程5所用的分离方法是
(4)已知Co的活泼性在Fe、Sn之间,由CoC2O4到Co所发生的两步反应依次是CoC2O4
 CoO+CO↑+CO2↑和
CoO+CO↑+CO2↑和
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钒铬还原渣是钠化提钒过程的固体废弃物,主要成分为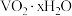 、
、 及少量
及少量 。用钒铬还原渣获得
。用钒铬还原渣获得 和
和 的工艺流程如图:
的工艺流程如图:
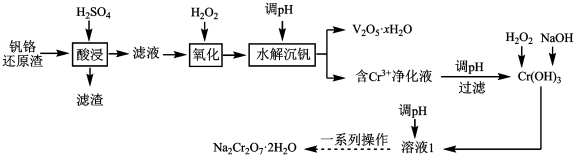
已知:“酸浸”初始温度为 ,
,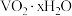 转化为
转化为 。
。
回答下列问题:
(1)“滤渣”的主要成分是___________ ,提高“酸浸”时的浸出率,可采用的措施有___________ (答出2条)。
(2)“氧化”时生成 ,发生反应离子方程式为
,发生反应离子方程式为___________ 。
(3) 可以与
可以与 和
和 反应生成
反应生成 ,写出该反应的化学反应方程式
,写出该反应的化学反应方程式___________ 。
(4)“一系列操作”包括蒸发浓缩、___________ 、干燥。
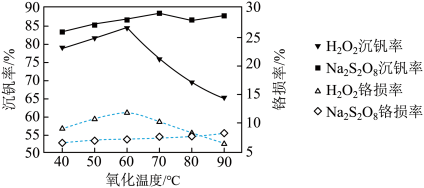
(5)查阅资料发现“氧化”时用 代替
代替 更好,温度对沉钒、铬损的影响如图所示,用
更好,温度对沉钒、铬损的影响如图所示,用 进行“氧化”时,应选择的适宜温度为
进行“氧化”时,应选择的适宜温度为________ ,选用 的原因是
的原因是________ 。
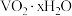 、
、 及少量
及少量 。用钒铬还原渣获得
。用钒铬还原渣获得 和
和 的工艺流程如图:
的工艺流程如图:
已知:“酸浸”初始温度为
 ,
,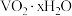 转化为
转化为 。
。回答下列问题:
(1)“滤渣”的主要成分是
(2)“氧化”时生成
 ,发生反应离子方程式为
,发生反应离子方程式为(3)
 可以与
可以与 和
和 反应生成
反应生成 ,写出该反应的化学反应方程式
,写出该反应的化学反应方程式(4)“一系列操作”包括蒸发浓缩、
(5)查阅资料发现“氧化”时用
 代替
代替 更好,温度对沉钒、铬损的影响如图所示,用
更好,温度对沉钒、铬损的影响如图所示,用 进行“氧化”时,应选择的适宜温度为
进行“氧化”时,应选择的适宜温度为 的原因是
的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钛酸钡( )可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是
)可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是 ,含少量
,含少量 、
、 、
、 等)为原料制备钛酸钡的流程如下:
等)为原料制备钛酸钡的流程如下: 如下表所示。
如下表所示。
注: 。
。
回答下列问题:
(1)浸渣的主要成分是_____ (填化学式)。
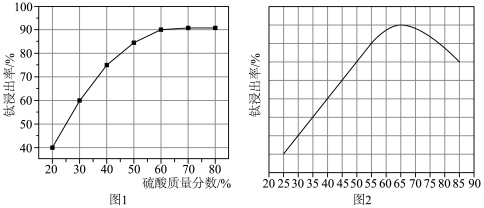
(2)“酸浸”中,其他条件相同,1h内钛浸出率与硫酸的质量分数、温度关系如图1所示。_____ 。图2中温度高于65℃,钛浸出率降低的原因可能是_____ 。
(3)“还原”时,主要反应的离子方程式为_____ ,检验“还原”后溶液中是否含 的试剂是
的试剂是_____ (填化学式)。
(4)“沉钛”中,先加入过量 溶液,后加入适量
溶液,后加入适量 溶液,如果加试剂顺序颠倒,会产生
溶液,如果加试剂顺序颠倒,会产生_____ (填化学式)杂质,影响产率。“调 ”范围为
”范围为_____ 。
(5)“氧化焙烧”发生反应的化学方程式为_____ 。工业上,还可以直接将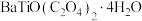 在1500℃、无氧环境下反应24h制备
在1500℃、无氧环境下反应24h制备 ,该方法的缺点是
,该方法的缺点是_____ 。
 )可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是
)可以作为防火涂料的添加剂,可提高涂层的防火性能和抗化学腐蚀性。以钛渣(主要成分是 ,含少量
,含少量 、
、 、
、 等)为原料制备钛酸钡的流程如下:
等)为原料制备钛酸钡的流程如下: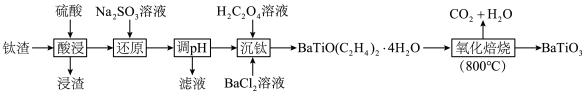
 如下表所示。
如下表所示。| 金属离子 |  |  |  |
开始沉淀/ | 1.5 | 6.3 | 0.5 |
完全沉淀/ | 2.8 | 8.3 | 2.5 |
 。
。回答下列问题:
(1)浸渣的主要成分是
(2)“酸浸”中,其他条件相同,1h内钛浸出率与硫酸的质量分数、温度关系如图1所示。
(3)“还原”时,主要反应的离子方程式为
 的试剂是
的试剂是(4)“沉钛”中,先加入过量
 溶液,后加入适量
溶液,后加入适量 溶液,如果加试剂顺序颠倒,会产生
溶液,如果加试剂顺序颠倒,会产生 ”范围为
”范围为(5)“氧化焙烧”发生反应的化学方程式为
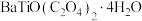 在1500℃、无氧环境下反应24h制备
在1500℃、无氧环境下反应24h制备 ,该方法的缺点是
,该方法的缺点是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】硫代硫酸钠晶体(Na2S2O3•5H2O,M=248g•mol﹣1)可用作还原剂。回答下列问题:
(1)已知:BaSO4,BaS2O3都是难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
(2)利用I2作为标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制;称取1.270 g纯净的I2,在盛有KI溶液的_____ (填仪器名称,下同)中溶解(反应为I2+KI=KI3,I2能够充分反应),完全溶解后,全部转移至100 mL的_____ 中,加蒸馏水至刻度线,此时KI3溶液的物质的量浓度为_____ mol•L﹣1;再取0.600gNa2S2O3•5H2O样品配制成溶液,备用。
②滴定:利用发生反应:I3﹣+2 ═
═ +3I﹣,对上述配制的Na2S2O3•5H2O溶液进行滴定,终点时消耗标准溶液20.00 mL,则样品纯度为
+3I﹣,对上述配制的Na2S2O3•5H2O溶液进行滴定,终点时消耗标准溶液20.00 mL,则样品纯度为_____ %(保留1位小数)。
(1)已知:BaSO4,BaS2O3都是难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
| 实验步骤 | 现象 |
| ①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
| ③取少量溶液溶于盐酸 | ④出现乳黄色浑浊, |
| ⑤静置, | ⑥ |
(2)利用I2作为标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制;称取1.270 g纯净的I2,在盛有KI溶液的
②滴定:利用发生反应:I3﹣+2
 ═
═ +3I﹣,对上述配制的Na2S2O3•5H2O溶液进行滴定,终点时消耗标准溶液20.00 mL,则样品纯度为
+3I﹣,对上述配制的Na2S2O3•5H2O溶液进行滴定,终点时消耗标准溶液20.00 mL,则样品纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
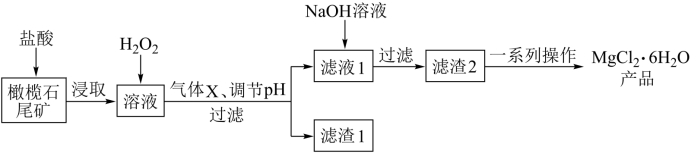
【推荐3】实验室利用橄榄石尾矿(主要成分为MgO及少量FeO、Fe2O3、Al2O3等)制备纯净氯化镁晶体(MgCl2·6H2O),实验流程如下:
已知几种金属阳离子形成氢氧化物沉淀时的pH如下表:
回答下列问题:
(1)“浸取”步骤中,能加快浸取速率的方法有___________ (任写两种)。
(2)气体X是___________ ,滤渣1溶于一定浓度硫酸溶液后,加热到70~80℃可以制得一种高效的无机高分子混凝剂、净水剂,其化学式为[Fe2(OH)n(SO4)(3-0.5n)]m,则该物质中铁元素的化合价为___________ 。溶液采用的加热方式为___________ ,控制温度70~80℃的原因是___________ 。
(3)加入H2O2的目的是___________ :若将上述过程中的“H2O2”用“NaClO”代替也能达到同样目的,则发生反应的离子方程式为___________ 。
(4)“一系列操作”主要包括加入足量盐酸,然后经过___________ 、过滤、洗涤,即得到氯化镁晶体。

已知几种金属阳离子形成氢氧化物沉淀时的pH如下表:
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时 | 7.6 | 2.7 | 4.2 | 9.6 |
| 沉淀完全时 | 9.6 | 3.7 | 5.4 | 11.1 |
(1)“浸取”步骤中,能加快浸取速率的方法有
(2)气体X是
(3)加入H2O2的目的是
(4)“一系列操作”主要包括加入足量盐酸,然后经过
您最近一年使用:0次
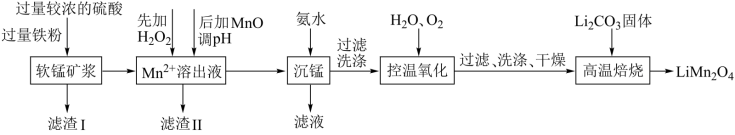
【推荐1】锰酸锂材料是新型锂电池的正极材料,具有容量高、成本低、安全性好、耐过充性好、易于合成等优异特性。工业上用某软锰矿(主要成分为MnO2,同时含有少量铁、铝及硅的氧化物)为原料制备锰酸锂(LiMn2O4)的流程如图:
室温下,有关物质的溶度积常数如表所示:
回答下列问题:
(1)滤渣I的主要成分除铁粉外还有___ (填化学式)。
(2)软锰矿浆加过量的硫酸和铁粉,铁的氧化过程及溶出Mn2+的主要途径如图所示。步骤II是从软锰矿浆中溶出Mn2+的主要反应,此反应中还原剂与氧化剂的物质的量之比为____ ;检验Mn2+溶出液中是否含有Fe3+常用的无机试剂为____ (填化学式)。

(3)实际生产中向Mn2+的溶出液中加入H2O2的量比理论值大,主要原因是__ 。
向Mn2+溶出液中先加H2O2,再加MnO调节pH的主要原因是___ ;当pH调节至6时,溶液中所含铝离子的浓度为____ 。
(4)“沉锰”得到Mn(OH)2和Mn2(OH)2SO4沉淀,均可被氧化为Mn3O4,若“控温氧化”过程中溶液的pH随时间变化如图所示,则t1~t2min内,沉淀中一定发生的氧化还原反应为___ (用离子方程式表示)。
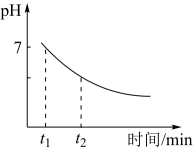
(5)写出高温焙烧生成锰酸锂的化学方程式:___ 。

室温下,有关物质的溶度积常数如表所示:
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 8.0×10-16 | 4.0×10-38 | 4.5×10-33 | 1.9×10-13 |
(1)滤渣I的主要成分除铁粉外还有
(2)软锰矿浆加过量的硫酸和铁粉,铁的氧化过程及溶出Mn2+的主要途径如图所示。步骤II是从软锰矿浆中溶出Mn2+的主要反应,此反应中还原剂与氧化剂的物质的量之比为

(3)实际生产中向Mn2+的溶出液中加入H2O2的量比理论值大,主要原因是
向Mn2+溶出液中先加H2O2,再加MnO调节pH的主要原因是
(4)“沉锰”得到Mn(OH)2和Mn2(OH)2SO4沉淀,均可被氧化为Mn3O4,若“控温氧化”过程中溶液的pH随时间变化如图所示,则t1~t2min内,沉淀中一定发生的氧化还原反应为

(5)写出高温焙烧生成锰酸锂的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
(1)上述流程中能加快反应速率的措施有__________ 、__________ 等。
(2)酸浸时发生反应:2MgO·SiO2 + 2H2SO4=2MgSO4 + SiO2 + 2H2O,2MgO·B2O3+ 2H2SO4 + H2O=2H3BO3 + 2MgSO4。
① 上述反应体现出酸性强弱:H2SO4__________ H3BO3(填“>”或“<”)。
② 酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:______ 、____ 。
③ 已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3 + OH-= BO2- + 2H2O,下列关于硼酸的说法正确的是___ (填序号)。(已知:H2CO3 Ka1=4.2×10-7,Ka2=5.6×10-11 H3BO3 Ka=5.8×10-10)
a. 硼酸是三元酸
b. 硼酸的电离方程式可表示为:H3BO3⇌ BO2- + H2O +H+
c. 向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
d.室温下同浓度的NaBO2溶液和Na2CO3 溶液,Na2CO3 溶液pH较大。
(3)褐色浸出液中加入H2O2目的是:________________ 。
(4)用MgO调节溶液的pH至________ 以上,使杂质离子转化为沉淀,过滤。
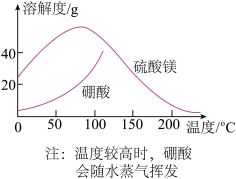
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合如图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,_________________ (将方法补充完整)。

已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(2)酸浸时发生反应:2MgO·SiO2 + 2H2SO4=2MgSO4 + SiO2 + 2H2O,2MgO·B2O3+ 2H2SO4 + H2O=2H3BO3 + 2MgSO4。
① 上述反应体现出酸性强弱:H2SO4
② 酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:
③ 已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3 + OH-= BO2- + 2H2O,下列关于硼酸的说法正确的是
a. 硼酸是三元酸
b. 硼酸的电离方程式可表示为:H3BO3⇌ BO2- + H2O +H+
c. 向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
d.室温下同浓度的NaBO2溶液和Na2CO3 溶液,Na2CO3 溶液pH较大。
(3)褐色浸出液中加入H2O2目的是:
(4)用MgO调节溶液的pH至
(5)获取晶体:ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;ⅱ.控制温度使两种晶体分别从溶液中结晶。结合如图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钴基合金中含少量镁、镍和铁元素,在化工、航空航天和机械工业应用广泛。现有钴基废合金需要回收再利用,设计流程如图:

已知:1)有关钴、镍、镁、铁化合物的性质见下表:
2)25℃ Ksp(MgF2)=7.4×10—11、Ksp(MgCO3)=3.5×10—3
请回答:
(1)“除镍”步骤必须控制在一定时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为________________ 。
(2)在“盐酸调pH=4”步骤中,加入盐酸的作用是______________________ 。
(3)“净化”步骤中加入H2O2的作用是_____________________ (请用离子方程式表示)。废渣的成分___________________ (请用化学式表示)。
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数K=
Fe(OH)3+3H+的平衡常数K=_________________________ 。
(5)二水合草酸钴晶体(CoC2O4·2H2O)中C元素的化合价为________ ,在空气中高温反应的化学方程式为_______________________ 。

已知:1)有关钴、镍、镁、铁化合物的性质见下表:
| 化学式 | 沉淀开始时的pH | 沉淀完全时的pH | 有关性质 |
| Co(OH)2 | 7.2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O  Co(OH)2+2H+ Co(OH)2+2H+Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
| Fe(OH)2 | 7.1 | 9.6 | |
| Fe(OH)3 | 2.3 | 3.7 | |
| Mg(OH)2 | 10.8 | 12.4 |
2)25℃ Ksp(MgF2)=7.4×10—11、Ksp(MgCO3)=3.5×10—3
请回答:
(1)“除镍”步骤必须控制在一定时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为
(2)在“盐酸调pH=4”步骤中,加入盐酸的作用是
(3)“净化”步骤中加入H2O2的作用是
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O
 Fe(OH)3+3H+的平衡常数K=
Fe(OH)3+3H+的平衡常数K=(5)二水合草酸钴晶体(CoC2O4·2H2O)中C元素的化合价为
您最近一年使用:0次



