N2、CO2 与 Fe+体系中存在如图 1 所示物质转变关系,已知 Fe+ (s)与中间产物 N2O(g) 反应过程中的能量变化如图 2 所示。下列说法错误的是
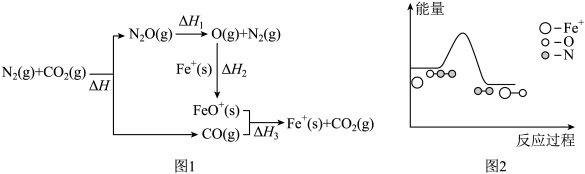
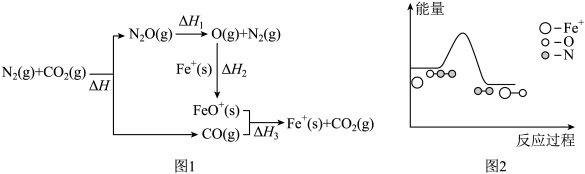
| A.∆H=-(∆H 1+∆H 2+∆H 3 ) |
| B.Fe+在反应中作催化剂,能降低反应的活化能 |
| C.∆H 1和∆H 2均小于 0 |
| D.由图 2 可知,反应 Fe+ (s)+N2O(g)=FeO+(s) +N2 (g) ∆H 4<0 |
22-23高三下·浙江杭州·阶段练习 查看更多[3]
更新时间:2023-03-17 10:12:20
|
相似题推荐
【推荐1】如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是( )


| A.热稳定性:MgF2 <MgCl2<MgBr2<MgI2 |
| B.22.4LF2(g)与足量的Mg充分反应,放热1124kJ |
| C.工业上可由电解MgCl2溶液冶炼金属Mg,该过程需要吸收热量 |
| D.由图可知:MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(l) ∆H<-117kJ/mol |
您最近一年使用:0次
【推荐2】已知N2O和CO反应进程的相对能量变化如图所示。已知CO(g)的燃烧热ΔH=-283kJ·mol-1。下列说法错误的是
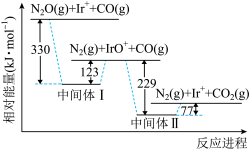

| A.中间体Ⅱ比中间体I稳定 |
| B.Ir+是上述反应的催化剂 |
| C.该反应过程中Ir元素的化合价发生了变化 |
D.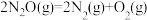 的反应热ΔH为-76kJ·mol-1 的反应热ΔH为-76kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】氨氮是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,相关反应如下:
①NH3+HClO=NH2Cl+H2O
②NH2Cl+HClO=NHCl2+H2O
③2NHCl2+H2O=N2+HClO+3HCl
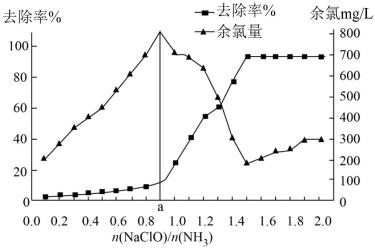
已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件一定的情况下,改变 (即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如图所示。则下列说法正确的是
(即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如图所示。则下列说法正确的是
①NH3+HClO=NH2Cl+H2O
②NH2Cl+HClO=NHCl2+H2O
③2NHCl2+H2O=N2+HClO+3HCl
已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件一定的情况下,改变
 (即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如图所示。则下列说法正确的是
(即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如图所示。则下列说法正确的是
| A.次氯酸与氨的总反应可表示为:2NH3+HClO=N2+3H2O+3HCl |
B.反应中氨氮去除效果最佳的 值约为1.5 值约为1.5 |
| C.a点之前溶液中发生的主要反应为:NH2Cl+HClO=NHCl2+H2O |
| D.次氯酸钠溶液pH较小时有O2生成,促使氨氮去除率提高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】氮肥保障了现代农业的丰收。根据下图的循环过程,有关硫酸铵和氯化铵的说法正确的是
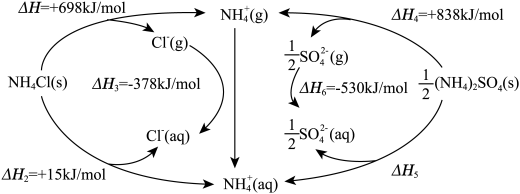

A.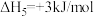 |
| B.硫酸铵晶体中只含离子键不含共价键 |
C.氯化铵晶体溶于水的过程: |
D.可以通过 的受热分解实验测得 的受热分解实验测得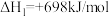 的数据 的数据 |
您最近一年使用:0次
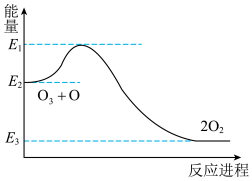
【推荐1】超音速飞机可排放NO,这是平流层中氮的氧化物的主要来源,它破坏臭氧层的机理为: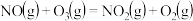
 ;
;
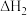 。总反应为:
。总反应为: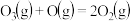
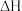 ,该反应的能量变化示意图如下:下列叙述中正确的是
,该反应的能量变化示意图如下:下列叙述中正确的是
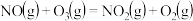
 ;
;
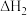 。总反应为:
。总反应为: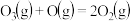
 ,该反应的能量变化示意图如下:下列叙述中正确的是
,该反应的能量变化示意图如下:下列叙述中正确的是
A. |
| B.该反应是吸热反应 |
C.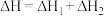 |
D.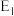 是反应 是反应 的活化能 的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某反应加入催化剂后,反应历程变成两个基元反应,相关能量变化如图所示为(E为正值,单位:kJ/mol)。下列有关说法正确的是


| A.此条件下,第一个基元反应的反应速率小于第二个 |
B.总反应的活化能 |
| C.对于Ea(活化能)>0的反应,必须加热才能进行 |
D.总反应的焓变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】水煤气变换反应为:CO(g)+H2O(g)=CO2(g)+H2(g)。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。下列说法正确的是




| A.水煤气变换反应的ΔH>0 |
| B.决定反应速率步骤(慢反应)的化学方程式为:H2O*=H*+OH* |
| C.反应物中的两个H2O同时吸附到金催化剂的表面 |
| D.该历程中最大能垒(活化能)E正=1.91eV |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向H2O2溶液中滴加少量Fe2(SO4)3溶液,反应原理如下图所示,下列说法不正确的是
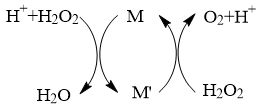

| A.该反应过程中,M是Fe3+, M’是Fe2+ |
B.该过程的总反应方程式为: 2H2O2 2H2O+O2↑ 2H2O+O2↑ |
| C.当反应中有1 mol O2生成时,转移电子数为2 mol |
| D.H2O2生产过程要严格避免混入Fe2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验过程可以达到实验目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 探究浓度对反应速率的影响 | 分别向2支盛有等体积、等浓度的FeCl3和CuCl2溶液的试管中同时加入2 mL5%H2O2溶液 |
| B | 制备无水Fe(OH)3 胶体 | 加热饱和FeCl3溶液至出现红褐色沉淀 |
| C | 探究温度对化学反应速率的影响 | 将等浓度的Na2S2O3和H2SO4等体积混合,平均分成两份,一份置于热水中,一份置于冷水中,记录出现浑浊的时间 |
| D | 比较金属的活泼性 | 向两只盛有稀硫酸的烧杯中分别投入铜丝和银丝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用如图所示装置进行实验,下列实验操作、现象及相应结论均正确的是
| 实验操作 | 实验现象 | 结论 | |
| A | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝不滴落 | 金属铝的熔点较高 |
| B | 将光亮的镁条放入盛有NH4Cl溶液的试管中 | 有大量气泡产生 | 生成的气体中含有NH3 |
| C | 向溶液X中加入Na2O2粉末 | 出现红褐色沉淀和无色气体 | X中一定含有Fe3+ |
| D | 在盛有少量HCl和H2O2混合溶液的试管中加入铁粉 | 试管中有大量无色气体产生 | 该反应中铁作催化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

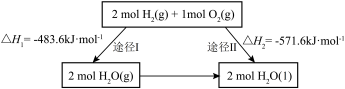
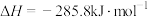
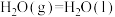 的过程中,
的过程中, ,
, ,只与反应体系的始态和终态有关,与反应途径无关
,只与反应体系的始态和终态有关,与反应途径无关 和1mol
和1mol 中化学键所需能量大于断裂2mol
中化学键所需能量大于断裂2mol 中化学键所需能量
中化学键所需能量

