I.工业上用丙烯加成法制备1,2-二氯丙烷(CH2ClCHClCH3),主要副产物为3-氯丙烯,反应原理为:
①CH2=CHCH3(g)+Cl2(g) CH2ClCHClCH3(g) ΔH1=-134 kJ·mol-1
CH2ClCHClCH3(g) ΔH1=-134 kJ·mol-1
②CH2=CHCH3(g)+Cl2(g) CH2=CHCH2Cl(g)+HCl(g) ΔH2=-102 kJ·mol-1
CH2=CHCH2Cl(g)+HCl(g) ΔH2=-102 kJ·mol-1
(1)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g),在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
用单位时间内气体分压的变化来表示反应速率,即v=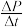 ,则反应①前180 min内平均反应速率v(CH2ClCHClCH3)=
,则反应①前180 min内平均反应速率v(CH2ClCHClCH3)=_______ kPa·min-1(保留小数点后2位)。
II.丙烯的制备方法
方法一:丙烷无氧脱氢法制备丙烯反应:C3H8(g) C3H6(g)+H2(g) ΔH=+124 kJ·mol-1
C3H6(g)+H2(g) ΔH=+124 kJ·mol-1
(2)①某温度下,在刚性容器中充入C3H8,起始压强为10 kPa,平衡时总压强为14 kPa,C3H8的平衡转化率为_______ 。该反应的平衡常数Kp=_______ kPa(保留小数点后2位)。
②总压分别为100 kPa和10 kPa时发生该反应,平衡体系中C3H8和C3H6的物质的量分数随温度变化关系如图1所示。_______ 、_______ 。
方法二:丙烷氧化脱氢法制备丙烯还生成CO、CO2等副产物,制备丙烯的反应: C3H8(g)+ O2(g)
O2(g)  C3H6(g)+H2O(g) ΔH=-118 kJ·mol-1,在催化剂的作用下C3H8的转化率和C3H6的产率随温度变化关系如图2所示。
C3H6(g)+H2O(g) ΔH=-118 kJ·mol-1,在催化剂的作用下C3H8的转化率和C3H6的产率随温度变化关系如图2所示。_______ ,观察图2,回答能提高C3H6选择性的措施是_______ 。(C3H6的选择性=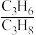 ×100%)
×100%)
①CH2=CHCH3(g)+Cl2(g)
 CH2ClCHClCH3(g) ΔH1=-134 kJ·mol-1
CH2ClCHClCH3(g) ΔH1=-134 kJ·mol-1②CH2=CHCH3(g)+Cl2(g)
 CH2=CHCH2Cl(g)+HCl(g) ΔH2=-102 kJ·mol-1
CH2=CHCH2Cl(g)+HCl(g) ΔH2=-102 kJ·mol-1(1)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g),在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
| 时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
| 压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
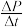 ,则反应①前180 min内平均反应速率v(CH2ClCHClCH3)=
,则反应①前180 min内平均反应速率v(CH2ClCHClCH3)=II.丙烯的制备方法
方法一:丙烷无氧脱氢法制备丙烯反应:C3H8(g)
 C3H6(g)+H2(g) ΔH=+124 kJ·mol-1
C3H6(g)+H2(g) ΔH=+124 kJ·mol-1(2)①某温度下,在刚性容器中充入C3H8,起始压强为10 kPa,平衡时总压强为14 kPa,C3H8的平衡转化率为
②总压分别为100 kPa和10 kPa时发生该反应,平衡体系中C3H8和C3H6的物质的量分数随温度变化关系如图1所示。
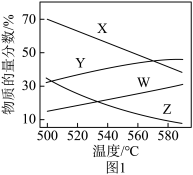
方法二:丙烷氧化脱氢法制备丙烯还生成CO、CO2等副产物,制备丙烯的反应: C3H8(g)+
 O2(g)
O2(g)  C3H6(g)+H2O(g) ΔH=-118 kJ·mol-1,在催化剂的作用下C3H8的转化率和C3H6的产率随温度变化关系如图2所示。
C3H6(g)+H2O(g) ΔH=-118 kJ·mol-1,在催化剂的作用下C3H8的转化率和C3H6的产率随温度变化关系如图2所示。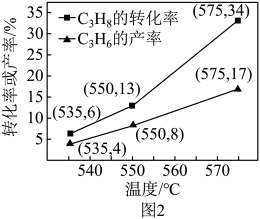
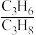 ×100%)
×100%)
更新时间:2023-03-24 16:30:05
|
相似题推荐
【推荐1】合成氨工业对国民经济和社会发展具有重要的意义。
其原理为:
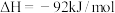 ;据此回答以下问题:
;据此回答以下问题:
实验室中模拟合成氨反应,在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:
(1)实验1中,50 min时向容器中充入一定量He,则正反应速率____ (域“增大”、“减小”或“不变”)
(2)实验2中,前20min内以 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为_____ 。
(3)比较实验1和2,说明实验2隐含的条件是______ 。
(4)上述三组实验的化学平衡常数分别为 、
、 、
、 ,三者大小关系是
,三者大小关系是______ 。
(5)某温度下,若把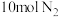 ,与
,与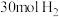 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体的压强弯为开始时的0.8,则平衡时氢气的转化率
置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体的压强弯为开始时的0.8,则平衡时氢气的转化率
_______ 。(用百分数表示)。能说明该反应达到化学平衡状态的是_____ (填字母)。
a.容器内压强保持不变。
b.容器内的密度保持不变
c.混合气体中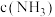 不变
不变
d.
(6)对于合成氨反应而言,下列有关图象一定正确的是_____ (选填序号)。
A、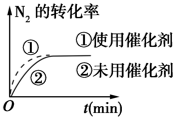 B、
B、 C、
C、 
其原理为:

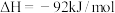 ;据此回答以下问题:
;据此回答以下问题:实验室中模拟合成氨反应,在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:
| 实验序号 | 温度(℃) |  浓度(mol/L) 浓度(mol/L) | ||||||
| 0 min | 10 min | 20 min | 30 min | 40min | 50min | 60 min | ||
| 1 | 300 | 2.00 | 1.70 | 1.50 | L36 | 1.25 | 1.20 | 1.20 |
| 2 | 300 | 2.00 | 1.50 | 1.28 | 1.20 | 1.20 | 1.20 | 1.20 |
| 3 | 200 | 2.00 | 1.60 | 1.39 | 1.29 | 1.27 | 1.27 | 1.27 |
(1)实验1中,50 min时向容器中充入一定量He,则正反应速率
(2)实验2中,前20min内以
 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为(3)比较实验1和2,说明实验2隐含的条件是
(4)上述三组实验的化学平衡常数分别为
 、
、 、
、 ,三者大小关系是
,三者大小关系是(5)某温度下,若把
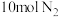 ,与
,与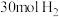 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体的压强弯为开始时的0.8,则平衡时氢气的转化率
置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体的压强弯为开始时的0.8,则平衡时氢气的转化率
a.容器内压强保持不变。
b.容器内的密度保持不变
c.混合气体中
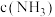 不变
不变d.

(6)对于合成氨反应而言,下列有关图象一定正确的是
A、
 B、
B、 C、
C、 
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研发CO2利用技术成为了研究热点,某科研团队采用一种类似“搭积木”的方式,在实验室中首次实现从二氧化碳到淀粉分子的全合成,“积木”中涉及如下两个反应:①CO2(g)+3H2(g) CH3OH(g)+H2O(g),②CH3OH(g)+O2(g)
CH3OH(g)+H2O(g),②CH3OH(g)+O2(g) HCHO(g)+H2O2(l)。一定温度下,往5L反应釜中充入1molCO2、3molH2,反应5min,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=
HCHO(g)+H2O2(l)。一定温度下,往5L反应釜中充入1molCO2、3molH2,反应5min,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=____ 。
 CH3OH(g)+H2O(g),②CH3OH(g)+O2(g)
CH3OH(g)+H2O(g),②CH3OH(g)+O2(g) HCHO(g)+H2O2(l)。一定温度下,往5L反应釜中充入1molCO2、3molH2,反应5min,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=
HCHO(g)+H2O2(l)。一定温度下,往5L反应釜中充入1molCO2、3molH2,反应5min,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某可逆反应:2A(g) B(g)+D(g)在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
B(g)+D(g)在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
(1)实验2中,在5~10 min内,以物质A表示的平均反应速率为______ mol·L-1·min-l,25 min时,v(正)______ (填“<”、“>”或“=”)v(逆)。
(2)0~10 min内,实验2比实验1的反应速率______ (填“快”或“慢”),其原因可能是______ 。
(3)实验3的探究目的是______ 。
 B(g)+D(g)在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
B(g)+D(g)在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:| 实验 序号 | 时间/min 浓度/mol•L-1 温度/℃ | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 950 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(2)0~10 min内,实验2比实验1的反应速率
(3)实验3的探究目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g)  pC(g)+qD(g)。已知:平均反应速率vC=
pC(g)+qD(g)。已知:平均反应速率vC= vA;反应2 min时,A的物质的量减少了
vA;反应2 min时,A的物质的量减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2 min内,vA=________ ,vB=________ 。
(2)化学方程式中,x=________ ,y=__________ ,p=__________ ,q=________ 。
(3)反应平衡时,D为2a mol,则B的转化率为________ 。
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,则该反应的ΔH________ 0。(填“>”“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:①反应速率________ (填“增大”“减小”或“不变”),理由是_____________________ 。
②平衡时反应物的转化率________ (填“增大”“减小”或“不变”),理由是__________________ 。
 pC(g)+qD(g)。已知:平均反应速率vC=
pC(g)+qD(g)。已知:平均反应速率vC= vA;反应2 min时,A的物质的量减少了
vA;反应2 min时,A的物质的量减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有a mol D生成。
mol,有a mol D生成。回答下列问题:
(1)反应2 min内,vA=
(2)化学方程式中,x=
(3)反应平衡时,D为2a mol,则B的转化率为
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,则该反应的ΔH
(5)如果其他条件不变,将容器的容积变为1 L,进行同样的实验,则与上述反应比较:①反应速率
②平衡时反应物的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一定条件下,在体积为5L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
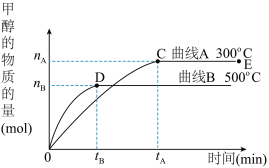
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=__________ ,升高温度,K值_______ (填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=_____________ 。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是___________ 。
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,该反应使用催化剂的目的是_____________________ 。已知反应Cu2O+CO 2Cu+CO2若原反应体系中含少量CO2
2Cu+CO2若原反应体系中含少量CO2________ (填“有利于”“不利于”)维持催化剂Cu2O的量不变。请标出反应Cu2O+CO 2Cu+CO2电子转移的方向和数目:
2Cu+CO2电子转移的方向和数目:___________________________ ,标准状况下2.24LCO2参与反应,电子转移数为___________ 个。
 CH3OH(g)
CH3OH(g)
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,该反应使用催化剂的目的是
 2Cu+CO2若原反应体系中含少量CO2
2Cu+CO2若原反应体系中含少量CO2 2Cu+CO2电子转移的方向和数目:
2Cu+CO2电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在某温度下合成氨:N2+3H2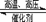 2NH3(△H<0),把N2和H2以1︰1的物质的量之比混匀后分成两等份,同时分别充入A体积和B体积两个装有催化剂的真空容器中(A、B两容器容积固定),在保持同温度下,A、B两个容器的合成氨反应先后达到平衡状态。请回答:
2NH3(△H<0),把N2和H2以1︰1的物质的量之比混匀后分成两等份,同时分别充入A体积和B体积两个装有催化剂的真空容器中(A、B两容器容积固定),在保持同温度下,A、B两个容器的合成氨反应先后达到平衡状态。请回答:
(1)写出该反应的平衡常数表达式:_____________ ,KA______ KB(填“>”、“<”或“=”)。
(2)平衡常数K值越大,表明建立平衡时__________ 。
A.N2的转化率越低 B.NH3的产量越小
C.正反应进行得越彻底
(3)欲增大该反应K值,可以采取的措施为__________ 。
A.升高温度 B.降低温度
C.增大N2、H2的浓度 D.使用高效的催化剂
(4)分析下表中数据后,完成下列问题[M(平)表示平衡时混合物的平均相对分子质量]:达平衡时,容器A中N2的转化率为___________ ,容器B中M(平)为__________ ,容器______ (填“A”或“B”)中,NH3的物质的量所占的比例较大。
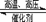 2NH3(△H<0),把N2和H2以1︰1的物质的量之比混匀后分成两等份,同时分别充入A体积和B体积两个装有催化剂的真空容器中(A、B两容器容积固定),在保持同温度下,A、B两个容器的合成氨反应先后达到平衡状态。请回答:
2NH3(△H<0),把N2和H2以1︰1的物质的量之比混匀后分成两等份,同时分别充入A体积和B体积两个装有催化剂的真空容器中(A、B两容器容积固定),在保持同温度下,A、B两个容器的合成氨反应先后达到平衡状态。请回答:(1)写出该反应的平衡常数表达式:
(2)平衡常数K值越大,表明建立平衡时
A.N2的转化率越低 B.NH3的产量越小
C.正反应进行得越彻底
(3)欲增大该反应K值,可以采取的措施为
A.升高温度 B.降低温度
C.增大N2、H2的浓度 D.使用高效的催化剂
(4)分析下表中数据后,完成下列问题[M(平)表示平衡时混合物的平均相对分子质量]:达平衡时,容器A中N2的转化率为
| 容器A | 容器B | |
| M(平) | 20 | |
| 平衡时N2的转化率 | 10% |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】“温室效应”是哥本哈根世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
(1)下列措施中,有利于降低大气中CO2浓度的是__________ (填字母编号)。
A 采用节能技术,减少化石燃料的用量
B 鼓励乘坐公交车出行,倡导“低碳”生活
C 利用太阳能、风能等新型能源替代化石燃料
(2)CH4是另一种主要的温室气体,lg甲烷完全燃烧生成液态水和二氧化碳,放出55.64kJ的热量,写出表示甲烷燃烧的热化学方程式_______________ 。
(3)酸雨的形成主要是由废气中的SOx和NOx造成的,某空气污染监测仪是根据SO2与Br2、H2O的定量反应来测定空气中SO2含量的,该反应的化学方程式为:____________ 。
(4)某硫酸工厂以黄铁矿为原料生产硫酸。第一阶段燃烧黄铁矿的化学方程式为4FeS2+11O2 2Fe2O3+8SO2:第二阶段的反应原理是2SO2(g)+O2(g)
2Fe2O3+8SO2:第二阶段的反应原理是2SO2(g)+O2(g) 2SO3(g),其生产设备的名称为接触室;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是
2SO3(g),其生产设备的名称为接触室;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是__________ (填字母编号)
A SO2为5mol·L-1,O2为3.5mol·L-1
B SO2为3mol·L-1
C SO2、SO3均为2.5mol·L-1
D SO3为5mol·L-1
(1)下列措施中,有利于降低大气中CO2浓度的是
A 采用节能技术,减少化石燃料的用量
B 鼓励乘坐公交车出行,倡导“低碳”生活
C 利用太阳能、风能等新型能源替代化石燃料
(2)CH4是另一种主要的温室气体,lg甲烷完全燃烧生成液态水和二氧化碳,放出55.64kJ的热量,写出表示甲烷燃烧的热化学方程式
(3)酸雨的形成主要是由废气中的SOx和NOx造成的,某空气污染监测仪是根据SO2与Br2、H2O的定量反应来测定空气中SO2含量的,该反应的化学方程式为:
(4)某硫酸工厂以黄铁矿为原料生产硫酸。第一阶段燃烧黄铁矿的化学方程式为4FeS2+11O2
 2Fe2O3+8SO2:第二阶段的反应原理是2SO2(g)+O2(g)
2Fe2O3+8SO2:第二阶段的反应原理是2SO2(g)+O2(g) 2SO3(g),其生产设备的名称为接触室;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是
2SO3(g),其生产设备的名称为接触室;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是A SO2为5mol·L-1,O2为3.5mol·L-1
B SO2为3mol·L-1
C SO2、SO3均为2.5mol·L-1
D SO3为5mol·L-1
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】CO用途广泛,工业应用时离不开平衡思想的指导。
I.在某一容积为5L的体积不变的密闭容器内,加入0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:
 ,反应中
,反应中 的浓度随时间变化情况如下图:
的浓度随时间变化情况如下图:
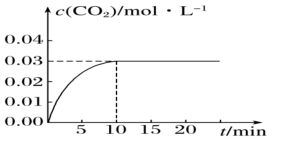
(1)根据图上数据,该温度(800℃)下的平衡常数
_______ 。
(2)在体积不变的条件下,改变下列条件能使平衡常数K增大的有_______ (填字母)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出一氧化碳气体
(3)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol的水蒸气,重新达到平衡后, 的转化率
的转化率_______ (填“升高”“降低”或“不变”)。
(4)在催化剂存在和800℃的条件下,在某一时刻测得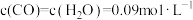 ;
; ,则此时正、逆反应速率的大小v正
,则此时正、逆反应速率的大小v正_______ (填“>”“<”或“=”)v逆
Ⅱ.在容积为1.00L的容器中,通入一定量的N2O4,发生反应 ,随温度升高,混合气体的颜色变深。回答下列问题:
,随温度升高,混合气体的颜色变深。回答下列问题:
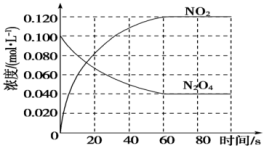
(5)反应的
_______ 0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率 为
为_______  ;反应的平衡常数
;反应的平衡常数 为
为_______ 。
I.在某一容积为5L的体积不变的密闭容器内,加入0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:

 ,反应中
,反应中 的浓度随时间变化情况如下图:
的浓度随时间变化情况如下图:
(1)根据图上数据,该温度(800℃)下的平衡常数

(2)在体积不变的条件下,改变下列条件能使平衡常数K增大的有
A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出一氧化碳气体
(3)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol的水蒸气,重新达到平衡后,
 的转化率
的转化率(4)在催化剂存在和800℃的条件下,在某一时刻测得
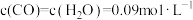 ;
; ,则此时正、逆反应速率的大小v正
,则此时正、逆反应速率的大小v正Ⅱ.在容积为1.00L的容器中,通入一定量的N2O4,发生反应
 ,随温度升高,混合气体的颜色变深。回答下列问题:
,随温度升高,混合气体的颜色变深。回答下列问题:
(5)反应的

 为
为 ;反应的平衡常数
;反应的平衡常数 为
为
您最近一年使用:0次
【推荐3】甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)一种新合成二甲醚的方法为一定条件下:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g),该反应的△H=
CH3OCH3(g)+3H2O(g),该反应的△H=_______ kJ·mol-1;在体积恒定的密闭容器中,下列能作为该反应达到化学平衡状态的依据是_______ (填序号)。
A.v(CO2):v(H2)=1:3
B.容器内CH3OCH3体积分数不变
C.容器内压强保持不变
D.单位时间内断裂6molH-H键,同时断裂3molH-O键
(2)可采用CO和二甲醚催化合成乙醇。
反应i:CH3OCH3(g)+CO(g) CH3COOCH3(g) △H1
CH3COOCH3(g) △H1
反应ii:CH3COOCH3(g)+2H2(g) CH3OH(g)+C2H5OH(g) △H2
CH3OH(g)+C2H5OH(g) △H2
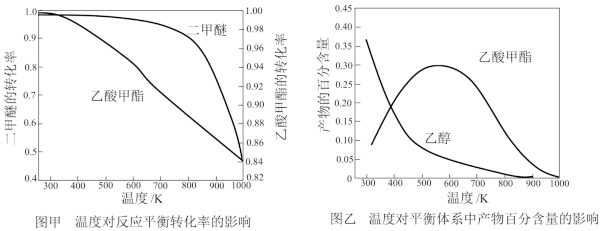
①压强为pkPa时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图甲所示,则△H1_______ (填“>”或“<”)0。
②温度对平衡体系中乙酸甲酯的含量和乙醇的影响图乙所示,在300~600K范围内,乙酸甲酯的含量逐渐增大,而乙醇的百分含量逐渐减小的原因是_______ 。
③若压强为pkPa、某温度时,向2L恒容密闭容器中充入1molCH3OCH3和1molCO只发生反应i,二甲醚的转化率为90%,2min时达到平衡,则前2min内CH3COOCH3的平均生成速率为_______ ,该条件下反应i的平衡常数K=_______ ,此时容器内的压强为_______ (用p表示)。
①CO(g)+2H2(g)
 CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1③CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1(1)一种新合成二甲醚的方法为一定条件下:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g),该反应的△H=
CH3OCH3(g)+3H2O(g),该反应的△H=A.v(CO2):v(H2)=1:3
B.容器内CH3OCH3体积分数不变
C.容器内压强保持不变
D.单位时间内断裂6molH-H键,同时断裂3molH-O键
(2)可采用CO和二甲醚催化合成乙醇。
反应i:CH3OCH3(g)+CO(g)
 CH3COOCH3(g) △H1
CH3COOCH3(g) △H1反应ii:CH3COOCH3(g)+2H2(g)
 CH3OH(g)+C2H5OH(g) △H2
CH3OH(g)+C2H5OH(g) △H2
①压强为pkPa时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图甲所示,则△H1
②温度对平衡体系中乙酸甲酯的含量和乙醇的影响图乙所示,在300~600K范围内,乙酸甲酯的含量逐渐增大,而乙醇的百分含量逐渐减小的原因是
③若压强为pkPa、某温度时,向2L恒容密闭容器中充入1molCH3OCH3和1molCO只发生反应i,二甲醚的转化率为90%,2min时达到平衡,则前2min内CH3COOCH3的平均生成速率为
您最近一年使用:0次



