2023年1月30日,中国科学院朱庆山团队研究六方相砷化镍(NiAs)型到正交相磷化锰(MnP)型结构转变,实现了对锂硫催化剂的精确设计。回答下列问题:
(1)Li、P、S三种元素中,电负性最小的是___________ 。第三周期元素中第一电离能比P大的元素有___________ 种。
(2)基态S原子核外有___________ 个电子自旋状态相同。基态As原子的电子排布式为___________ 。
(3)PH3、AsH3中沸点较高的是___________ ,其主要原因是___________ 。
(4)Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],该配合物中锰原子的配位数为___________ 。
(5)CH3CN中C原子的杂化类型为___________ 。
(6)等物质的量的CH3CN和CO中,π键数目之比___________ 。
(7)NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为NA,晶体的密度为ρ g/cm3,则该晶胞中最近的砷原子之间的距离为___________ pm。

(1)Li、P、S三种元素中,电负性最小的是
(2)基态S原子核外有
(3)PH3、AsH3中沸点较高的是
(4)Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],该配合物中锰原子的配位数为
(5)CH3CN中C原子的杂化类型为
(6)等物质的量的CH3CN和CO中,π键数目之比
(7)NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为NA,晶体的密度为ρ g/cm3,则该晶胞中最近的砷原子之间的距离为

2023·河南郑州·二模 查看更多[4]
河南省郑州市2023届高三下学期第二次质量预测理科综合化学试题(已下线)化学-2023年高考押题预测卷03(山东卷)(含考试版、全解全析、参考答案、答题卡)(已下线)考点43 晶体结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)甘肃省武威第一中学2023-2024学年高三上学期第三次月考化学试题
更新时间:2023-04-06 14:55:31
|
相似题推荐
【推荐1】科学工作者合成了含镁、镍、碳3种元素的超导材料,具有良好的应用前景。回答下列问题:
(1)Ni的基态原子价电子排布式为_____ 。元素Mg与C中,第一电离能较小的是_____ (填元素符号)。
(2)科学家研究发现Ni与CO在60~80℃时反应生成Ni(CO)4气体,在Ni(CO)4分子中与Ni形成配位键的原子是_____ (填元素符号),Ni(CO)4晶体类型是______ 。
(3)下列分子或离子与CO2具有相同类型化学键和立体构型的是_____ (填标号)。
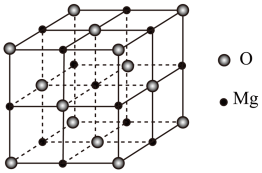
(4)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为anm,则r(O2-)为_____ nm(用含a的表达式表示)。
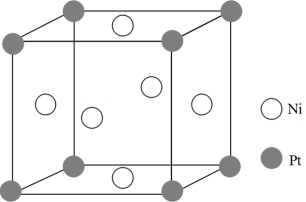
(5)铂镍合金在较低温度下形成一种超结构有序相,其立方晶胞结构如图所示,晶胞参数为apm。结构中有两种八面体空隙,一种完全由镍原子构成,另一种由铂原子和镍原子共同构成(如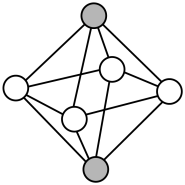 )。晶体中完全由镍原子构成的八面体空隙与由铂原子和镍原子共同构成的八面体空隙数目之比为
)。晶体中完全由镍原子构成的八面体空隙与由铂原子和镍原子共同构成的八面体空隙数目之比为_____ ,两种八面体空隙中心的最近距离为______ pm。
(1)Ni的基态原子价电子排布式为
(2)科学家研究发现Ni与CO在60~80℃时反应生成Ni(CO)4气体,在Ni(CO)4分子中与Ni形成配位键的原子是
(3)下列分子或离子与CO2具有相同类型化学键和立体构型的是
| A.SO2 | B.SCN- | C.NO | D.I |

(5)铂镍合金在较低温度下形成一种超结构有序相,其立方晶胞结构如图所示,晶胞参数为apm。结构中有两种八面体空隙,一种完全由镍原子构成,另一种由铂原子和镍原子共同构成(如
 )。晶体中完全由镍原子构成的八面体空隙与由铂原子和镍原子共同构成的八面体空隙数目之比为
)。晶体中完全由镍原子构成的八面体空隙与由铂原子和镍原子共同构成的八面体空隙数目之比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】锂离子电池是近年来的研究热点,常见的锂离子聚合物电池材料有石墨、LiAsF6、LiPF6、LiMn2O4等。回答下列问题:
(1)As的最高能级组的电子排布式为_______ ,Li、O、P、As四种元素电负性由大到小的顺序为_______ (填元素符号)。
(2)LiPF6的阴离子的空间构型为_______ 。
(3)一种类石墨的聚合物g—C3N4可由三聚氰胺( )制得。三聚氰胺分子中氮原子杂化类型是
)制得。三聚氰胺分子中氮原子杂化类型是_______ ;三聚氰胺分子不溶于冷水,溶于热水,主要原因是_______ 。
(4)尖晶石结构的LiMn2O4是一种常用的正极材料。已知一种LiMn2O4晶胞可看成由A、B单元按Ⅲ方式交替排布构成,“○”表示O2−。
 ①“●”表示的微粒是
①“●”表示的微粒是_______ (填元素符号)
②若该晶胞的晶胞参数为apm,设NA为阿伏加德罗常数的值,该晶体的密度为_______ g·cm-3(列出计算表达式,不必化简)
(1)As的最高能级组的电子排布式为
(2)LiPF6的阴离子的空间构型为
(3)一种类石墨的聚合物g—C3N4可由三聚氰胺(
 )制得。三聚氰胺分子中氮原子杂化类型是
)制得。三聚氰胺分子中氮原子杂化类型是(4)尖晶石结构的LiMn2O4是一种常用的正极材料。已知一种LiMn2O4晶胞可看成由A、B单元按Ⅲ方式交替排布构成,“○”表示O2−。
 ①“●”表示的微粒是
①“●”表示的微粒是②若该晶胞的晶胞参数为apm,设NA为阿伏加德罗常数的值,该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为__________ ,有______ 个未成对电子。写出磷及其同周期相邻元素第一电离能的大小顺序_________ 。
(2)磷的一种同素异形体——白磷(P4)的其键角为_________ ,推测其在CS2中的溶解度___________ (填“大于”或“小于”)在水中的溶解度
(3)两种三角锥形气态氢化物膦(PH3)和氮(NH3)的键角分别为93.6°和107°,试分析PH3、的键角小于NH3的原因_________ 。写出一种与互为等电子体的阳离子_________ 。
(4)PCl3中心原子杂化轨道类型为________ ,VSEPR 模型为_______ 。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,下图为其立方体晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点______ (填“高于”或“低于”)金刚石熔点。
已知其B-P键长均为x cm,则其密度为_____ g/cm3(列出计算式即可)
(1)基态P原子的核外电子排布式为
(2)磷的一种同素异形体——白磷(P4)的其键角为
(3)两种三角锥形气态氢化物膦(PH3)和氮(NH3)的键角分别为93.6°和107°,试分析PH3、的键角小于NH3的原因
(4)PCl3中心原子杂化轨道类型为
(5)磷化硼(BP)是一种超硬耐磨涂层材料,下图为其立方体晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点
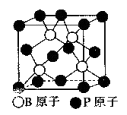
已知其B-P键长均为x cm,则其密度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】湿法炼锌综合回收系统产出的萃余液中含有Na2SO4、ZnSO4、H2SO4,还含有Mn2+、Co2+、Ni2+、Cd2+、Fe2+、A13+等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:

回答下列问题:
(1)“氧化”时,Mn2+、Fe2+均发生反应。后者发生反应时,氧化剂与还原剂的物质的量之比为___________ 。
(2)“调pH”时,所得滤渣1中除含有MnO2和Fe(OH)3外,还有___________ 。此时若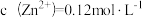 ,pH的范围应为
,pH的范围应为___________ 。{已知:常温下,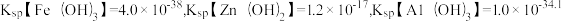 }
}
(3)“除镉”时,发生的反应属于四种基本反应类型的___________ 。
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物。其净化原理可表示为:
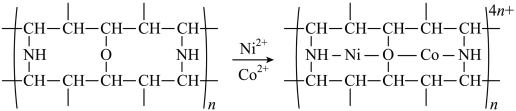
该有机净化剂所含元素的电负性由大到小的顺序为___________ 。上述反应时,接受电子对的一方是___________ 。
(5)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为___________ 。
(6)“沉锌”时,所得滤液经硫酸酸化后,用惰性电极电解可制备Na2S2O8,从而实现原料的循环利用,该电解过程中总反应的化学方程式为___________ 。

回答下列问题:
(1)“氧化”时,Mn2+、Fe2+均发生反应。后者发生反应时,氧化剂与还原剂的物质的量之比为
(2)“调pH”时,所得滤渣1中除含有MnO2和Fe(OH)3外,还有
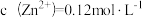 ,pH的范围应为
,pH的范围应为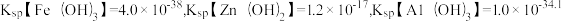 }
}(3)“除镉”时,发生的反应属于四种基本反应类型的
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物。其净化原理可表示为:

该有机净化剂所含元素的电负性由大到小的顺序为
(5)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为
(6)“沉锌”时,所得滤液经硫酸酸化后,用惰性电极电解可制备Na2S2O8,从而实现原料的循环利用,该电解过程中总反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】2018 年 11 月《Nature Energy》报道了中科院大连化学物理研究所科学家用 Ni-BaH2/Al2O3、Ni-LiH 等作催化剂,实现了在常压、100~300℃的条件下合成氨。
(1)在元素周期表中,Li、O、H 三种元素的电负性由大到小的顺序为___________ ;Al 原子核外电子空间运动状态有 8 种,则该原子处于____ (填“基态”或“激发态”)。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为 182℃,沸点为 233℃。
①硝酸溶液中 NO3‑的空间构型为__________ 。
②甘氨酸中 N 原子的杂化类型为________ ,分子中σ键与π键的个数比为_________ ;其熔点、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为 141℃)的主要原因:一是甘氨酸能形成内盐,二是______________ 。
(3)[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液,请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式___________________ 。
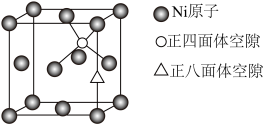
(4)X-射线衍射分析表明,由 Ni 元素形成的化合物 Mg2NiH4的立方晶胞如图所示,其面心和顶点均被 Ni 原子占据,所有 Mg 原子的 Ni 配位数都相等。则 Mg 原子填入由 Ni 原子形成的___ 空隙中(填“正四面体”或“正八面体”),填隙率是____ 。
(5)已知 Mg2NiH4晶体的晶胞参数为 646.5 pm,液氢的密度为0.0708 g•cm-3。若以材料中氢的密度与液氢密度之比定义为储氢材料的储氢能力,在 Mg2NiH4的储氢能力为____________ (列出计算式即可)。
(1)在元素周期表中,Li、O、H 三种元素的电负性由大到小的顺序为
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为 182℃,沸点为 233℃。
①硝酸溶液中 NO3‑的空间构型为
②甘氨酸中 N 原子的杂化类型为
(3)[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液,请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式
(4)X-射线衍射分析表明,由 Ni 元素形成的化合物 Mg2NiH4的立方晶胞如图所示,其面心和顶点均被 Ni 原子占据,所有 Mg 原子的 Ni 配位数都相等。则 Mg 原子填入由 Ni 原子形成的
(5)已知 Mg2NiH4晶体的晶胞参数为 646.5 pm,液氢的密度为0.0708 g•cm-3。若以材料中氢的密度与液氢密度之比定义为储氢材料的储氢能力,在 Mg2NiH4的储氢能力为

您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
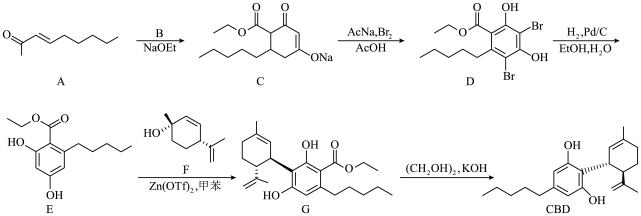
【推荐3】大麻二酚(CBD)具有降血糖、抗肿瘤、抗焦虑等多种生物活性。以下是CBD在医药工业上的一种合成路线,回答下列问题。___________ 。
(2)B的结构为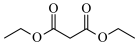 ,其化学名称是
,其化学名称是___________ ;D中含氧官能团的名称是___________ 。
(3)写出由E生成G的化学方程式___________ ,该反应类型为___________ 。
(4)已知X和A具有不同的官能团,其相对分子质量比A小14,同时满足如下条件的X的同分异构体Y共有___________ 种。(不考虑立体异构)
①1molY能与2mol[Ag(NH3)2]OH反应;②含有六元碳环。
满足上述条件的同分异构体中,只含有一个手性碳原子的Z是___________ (写出结构简式)。
(5)已知:R-CN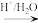 R-COOH.设计以Z与HCN为原料合成
R-COOH.设计以Z与HCN为原料合成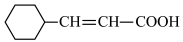 的路线(用流程图表示,其他无机试剂自选):
的路线(用流程图表示,其他无机试剂自选):___________ 。
(2)B的结构为
 ,其化学名称是
,其化学名称是(3)写出由E生成G的化学方程式
(4)已知X和A具有不同的官能团,其相对分子质量比A小14,同时满足如下条件的X的同分异构体Y共有
①1molY能与2mol[Ag(NH3)2]OH反应;②含有六元碳环。
满足上述条件的同分异构体中,只含有一个手性碳原子的Z是
(5)已知:R-CN
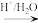 R-COOH.设计以Z与HCN为原料合成
R-COOH.设计以Z与HCN为原料合成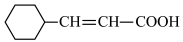 的路线(用流程图表示,其他无机试剂自选):
的路线(用流程图表示,其他无机试剂自选):
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】氮及其化合物应用广泛。回答下列问题:
(1)基态 原子处于最高能级的电子云轮廓图为
原子处于最高能级的电子云轮廓图为___________ 形,能量最低的激发态 的核外电子排布式为
的核外电子排布式为___________ 。
(2)胍( )为平面形分子,存在大
)为平面形分子,存在大 键
键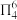 。胍属于
。胍属于___________ 分子(填“极性”或“非极性”), 原子的杂化轨道方式为
原子的杂化轨道方式为___________ ,①号 原子
原子 键角
键角___________ ②号 原子
原子 键角(填“>”“<”或“=”),胍易吸收空气中
键角(填“>”“<”或“=”),胍易吸收空气中 和
和 ,其原因是
,其原因是___________ 。
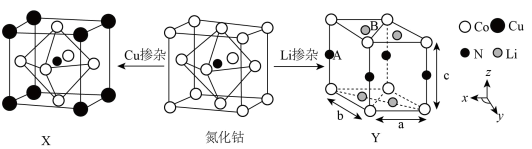
(3)氮化钴属于立方晶系,经 掺杂得催化剂
掺杂得催化剂 ,经
,经 掺杂得催化剂
掺杂得催化剂 。
。 属于立方晶系,晶胞参数为
属于立方晶系,晶胞参数为 ,距离最近
,距离最近 原子的核间距为
原子的核间距为___________  ,若
,若 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, 的密度为
的密度为___________  (用含
(用含 的代数式表示)。
的代数式表示)。 属于六方晶系,晶胞参数为
属于六方晶系,晶胞参数为 ,
, ,
,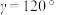 (
( 轴与
轴与 轴夹角),1个
轴夹角),1个 原子周围距离相等且最近的
原子周围距离相等且最近的 原子数目为
原子数目为___________ 。
(1)基态
 原子处于最高能级的电子云轮廓图为
原子处于最高能级的电子云轮廓图为 的核外电子排布式为
的核外电子排布式为(2)胍(
 )为平面形分子,存在大
)为平面形分子,存在大 键
键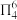 。胍属于
。胍属于 原子的杂化轨道方式为
原子的杂化轨道方式为 原子
原子 键角
键角 原子
原子 键角(填“>”“<”或“=”),胍易吸收空气中
键角(填“>”“<”或“=”),胍易吸收空气中 和
和 ,其原因是
,其原因是(3)氮化钴属于立方晶系,经
 掺杂得催化剂
掺杂得催化剂 ,经
,经 掺杂得催化剂
掺杂得催化剂 。
。
 属于立方晶系,晶胞参数为
属于立方晶系,晶胞参数为 ,距离最近
,距离最近 原子的核间距为
原子的核间距为 ,若
,若 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, 的密度为
的密度为 (用含
(用含 的代数式表示)。
的代数式表示)。 属于六方晶系,晶胞参数为
属于六方晶系,晶胞参数为 ,
, ,
,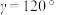 (
( 轴与
轴与 轴夹角),1个
轴夹角),1个 原子周围距离相等且最近的
原子周围距离相等且最近的 原子数目为
原子数目为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成C的含氧化合物。请回答下列问题:
(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为_____ 。
(2)在3d过渡金属中,基态原子未成对电子数最多的元素是_____ (填元素符号)。
(3)铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为_____ 。
(4)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力_____ (“减弱”或“不变”)。铁晶体中粒子之间作用力类型是_____ 。
(5)常温下,H2O2氧化CH4生成CH3OH、HCHO、HCOOH等。
①它们的沸点分别为64.7℃、-19.5℃、100.8℃,其主要原因是_____ ;
②CH4和HCHO比较,键角较大的是_____ ,主要原因是_____ 。
(6)钴晶胞和白铜(铜镍合金)晶胞分别如图1、2所示。
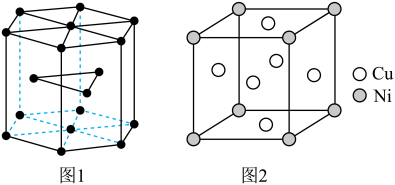
①钴晶胞堆积方式的名称为_____ ;
②已知白铜晶胞的密度为dg·cm-3,NA代表阿伏加 德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为_____ pm(列出计算式)。
(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为
(2)在3d过渡金属中,基态原子未成对电子数最多的元素是
(3)铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为
(4)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力
(5)常温下,H2O2氧化CH4生成CH3OH、HCHO、HCOOH等。
①它们的沸点分别为64.7℃、-19.5℃、100.8℃,其主要原因是
②CH4和HCHO比较,键角较大的是
(6)钴晶胞和白铜(铜镍合金)晶胞分别如图1、2所示。

①钴晶胞堆积方式的名称为
②已知白铜晶胞的密度为dg·cm-3,NA代表阿伏加 德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】Ag2[HgI4]是一种重要的无机热致变色示温材料。回答下列问题:
(1)Hg在元素周期表中位于第六周期,且与Zn同族,则基态Hg原子的价层电子排布式为_____ 。
(2)单质Hg在过量的Cl2中加热可生成HgCl2(熔点280℃,易升华,俗称升汞),则HgCl2的晶体类型为____ 。
(3)HIO3酸性强于HIO的原因是_____ ,IO 的立体构型为
的立体构型为_____ 。
(4)含有多个配位原子的配体与同一中心离子(或原子)通过鳌合配位成环而形成的配合物为螯合物。一种Ag+配合物的结构如图所示。

1mol该配合物中通过鳌合作用与Ag+形成的配位键有_____ mol,该配合物中处于同周期的三种非金属元素,电负性最小的是_____ (填元素符号),其原子的杂化类型为_____ 。
(5)Ag2[HgI4]在低温条件下为四方晶系结构,晶胞参数分别为apm、bpm,a=β=y=90,其晶胞结构如图所示。若Ag2[Hgl4]晶体的密度为ρg·cm-3,则NA=_____ mol-1。

(1)Hg在元素周期表中位于第六周期,且与Zn同族,则基态Hg原子的价层电子排布式为
(2)单质Hg在过量的Cl2中加热可生成HgCl2(熔点280℃,易升华,俗称升汞),则HgCl2的晶体类型为
(3)HIO3酸性强于HIO的原因是
 的立体构型为
的立体构型为(4)含有多个配位原子的配体与同一中心离子(或原子)通过鳌合配位成环而形成的配合物为螯合物。一种Ag+配合物的结构如图所示。

1mol该配合物中通过鳌合作用与Ag+形成的配位键有
(5)Ag2[HgI4]在低温条件下为四方晶系结构,晶胞参数分别为apm、bpm,a=β=y=90,其晶胞结构如图所示。若Ag2[Hgl4]晶体的密度为ρg·cm-3,则NA=

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】由废铁屑制得磷酸铁( ,一种难溶于水的米白色固体),然后获得锂离子正极材料
,一种难溶于水的米白色固体),然后获得锂离子正极材料 的流程如下:
的流程如下:

(1) 的晶胞结构如图1所示,其中
的晶胞结构如图1所示,其中 围绕
围绕 和
和 分别形成正八面体和正四面体,其余为
分别形成正八面体和正四面体,其余为 。每个晶胞中含有
。每个晶胞中含有 的数目为
的数目为_______ 。

(2)碱洗:废铁屑需碱洗的目的是_______ 。
(3)酸浸:酸浸时加入过量的 ,除了为确保废铁屑完全溶解、除去过量的
,除了为确保废铁屑完全溶解、除去过量的 外,还有的作用是
外,还有的作用是_______ 。
(4)合成:合成步骤中蔗糖的作用是_______ 。
(5)请补充完整由氧化后的溶液制备纯净的 的实验方案:
的实验方案:_______ (须选择的试剂有: 溶液、
溶液、 溶液、
溶液、 溶液).已知:
溶液).已知: 溶液中含磷微粒分布分数如图2所示。
溶液中含磷微粒分布分数如图2所示。

 ,一种难溶于水的米白色固体),然后获得锂离子正极材料
,一种难溶于水的米白色固体),然后获得锂离子正极材料 的流程如下:
的流程如下:
(1)
 的晶胞结构如图1所示,其中
的晶胞结构如图1所示,其中 围绕
围绕 和
和 分别形成正八面体和正四面体,其余为
分别形成正八面体和正四面体,其余为 。每个晶胞中含有
。每个晶胞中含有 的数目为
的数目为
(2)碱洗:废铁屑需碱洗的目的是
(3)酸浸:酸浸时加入过量的
 ,除了为确保废铁屑完全溶解、除去过量的
,除了为确保废铁屑完全溶解、除去过量的 外,还有的作用是
外,还有的作用是(4)合成:合成步骤中蔗糖的作用是
(5)请补充完整由氧化后的溶液制备纯净的
 的实验方案:
的实验方案: 溶液、
溶液、 溶液、
溶液、 溶液).已知:
溶液).已知: 溶液中含磷微粒分布分数如图2所示。
溶液中含磷微粒分布分数如图2所示。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中含有Fe、As、Ti等元素。回答下列问题:
(1)Fe转化为阳离子时首先失去__ 轨道电子,基态Fe3+核外电子排布式为__ 。
(2)AsH3中心原子杂化类型为__ 。
(3)与As同主族的短周期元素有N、P,一定压强下将AsH3、NH3和PH3的混合气体降温,首先液化的是__ ,理由是___ 。
(4)Ti金属晶体的堆积模型为__ ,配位数为__ ,基态Ti3+中未成对电子数有_ 个。
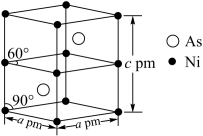
(5)某砷镍合金的晶胞结构如图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=__ g·cm-3。
(1)Fe转化为阳离子时首先失去
(2)AsH3中心原子杂化类型为
(3)与As同主族的短周期元素有N、P,一定压强下将AsH3、NH3和PH3的混合气体降温,首先液化的是
(4)Ti金属晶体的堆积模型为
(5)某砷镍合金的晶胞结构如图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】中国科学技术大学吴长征教授团队通过四烷基铵阳离子的插层及随后对合适氧化还原电位的选择,成功剥离制备出二维非范德华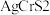 纳米片。
纳米片。
(1)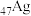 与铜元素同族,其基态原子价电子轨道表达式为
与铜元素同族,其基态原子价电子轨道表达式为___________ 。
(2)N、O、S的第一电离能由小到大的顺序为,___________ ,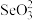 的空间结构为
的空间结构为___________ , 中碲的杂化轨道类型是
中碲的杂化轨道类型是___________ 。
(3)高氧化态 的过氧化物大多不稳定,容易分解,但
的过氧化物大多不稳定,容易分解,但 却是稳定的。这种配合物仍保持
却是稳定的。这种配合物仍保持 的过氧化物的结构特点,具体如图所示,
的过氧化物的结构特点,具体如图所示, 该配合物含有
该配合物含有___________  配位键;该结构中
配位键;该结构中 键角
键角___________  中的
中的 键角(填“大于”、“小于”或“等于”)。
键角(填“大于”、“小于”或“等于”)。 晶胞与
晶胞与 晶胞相似(如图),
晶胞相似(如图), 晶胞中部分原子的分数坐标为:A点
晶胞中部分原子的分数坐标为:A点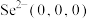 ,从该晶胞中找出距离B点
,从该晶胞中找出距离B点 最远的
最远的 的位置
的位置___________ (用分数坐标表示),晶胞中距离最近的两个 的距离为
的距离为 ,请计算
,请计算 晶胞的密度
晶胞的密度___________  。
。
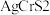 纳米片。
纳米片。(1)
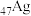 与铜元素同族,其基态原子价电子轨道表达式为
与铜元素同族,其基态原子价电子轨道表达式为(2)N、O、S的第一电离能由小到大的顺序为,
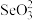 的空间结构为
的空间结构为 中碲的杂化轨道类型是
中碲的杂化轨道类型是(3)高氧化态
 的过氧化物大多不稳定,容易分解,但
的过氧化物大多不稳定,容易分解,但 却是稳定的。这种配合物仍保持
却是稳定的。这种配合物仍保持 的过氧化物的结构特点,具体如图所示,
的过氧化物的结构特点,具体如图所示, 该配合物含有
该配合物含有 配位键;该结构中
配位键;该结构中 键角
键角 中的
中的 键角(填“大于”、“小于”或“等于”)。
键角(填“大于”、“小于”或“等于”)。
 晶胞与
晶胞与 晶胞相似(如图),
晶胞相似(如图), 晶胞中部分原子的分数坐标为:A点
晶胞中部分原子的分数坐标为:A点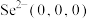 ,从该晶胞中找出距离B点
,从该晶胞中找出距离B点 最远的
最远的 的位置
的位置 的距离为
的距离为 ,请计算
,请计算 晶胞的密度
晶胞的密度 。
。
您最近一年使用:0次



