某同学进行了 与硫酸反应的有关实验,实验过程的数据记录如下(见表格)
与硫酸反应的有关实验,实验过程的数据记录如下(见表格)
(1)写出 溶液与稀硫酸反应的化学方程式为
溶液与稀硫酸反应的化学方程式为___________ 。
(2)A开始反应时硫代硫酸钠溶液的浓度为___________ mol/L (忽略不同溶液混合的体积变化);
(3)根据你所掌握的知识,在上述实验中,反应速率最快的可能是___________ (填实验序号);实验中,利用出现___________ (填现象)的快慢来比较反应速率的快慢;
(4)A和B的组合研究的是硫代硫酸钠浓度对反应速率的影响,表格中
___________ ;
(5)能说明温度对该反应速率影响的组合是___________ (填实验序号)。
 与硫酸反应的有关实验,实验过程的数据记录如下(见表格)
与硫酸反应的有关实验,实验过程的数据记录如下(见表格)| 实验序号 | 反应温度 | 硫代硫酸钠 | 硫酸 | 水 | ||
体积( ) ) | 浓度( ) ) | 体积( ) ) | 浓度( L L | )体积( ) ) | ||
| A |  | 10 | 0.1 | 10 | 0.1 | 0 |
| B |  | 5 | 0.1 | 10 | 0.1 | V |
| C |  | 10 | 0.1 | 5 | 0.1 | 5 |
| D |  | 10 | 0.1 | 10 | 0.1 | 0 |
 溶液与稀硫酸反应的化学方程式为
溶液与稀硫酸反应的化学方程式为(2)A开始反应时硫代硫酸钠溶液的浓度为
(3)根据你所掌握的知识,在上述实验中,反应速率最快的可能是
(4)A和B的组合研究的是硫代硫酸钠浓度对反应速率的影响,表格中

(5)能说明温度对该反应速率影响的组合是
更新时间:2023-05-15 20:43:16
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】碘在科研与生活中有重要作用,某兴趣小组用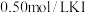 、0.2%淀粉溶液、
、0.2%淀粉溶液、 、
、 等试剂,探究反应条件对化学反应速率的影响。
等试剂,探究反应条件对化学反应速率的影响。
已知: (慢)
(慢)
 (快)
(快)
(1)向KI、 与淀粉的混合溶液中加入一定量的
与淀粉的混合溶液中加入一定量的 溶液,当溶液中的
溶液,当溶液中的___________ 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色, 与
与 初始的体积
初始的体积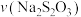 与
与 量需满足的关系为:
量需满足的关系为: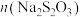
___________  (填“>”,“<”,“=”),出现蓝色之前,
(填“>”,“<”,“=”),出现蓝色之前, 在反应中起到的作用是
在反应中起到的作用是___________ 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
①表中
___________ ,
___________ ,
___________ 。
②用 表示实验序号④的速率为
表示实验序号④的速率为___________ 。
(3)已知某条件下,浓度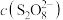 随反应时间t的变化曲线如图,若保持其它条件不变,图中分别画出降低反应温度和加入催化剂时
随反应时间t的变化曲线如图,若保持其它条件不变,图中分别画出降低反应温度和加入催化剂时 随反应时间t的变化曲线示意图(进行相应的标注)。
随反应时间t的变化曲线示意图(进行相应的标注)。_____

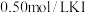 、0.2%淀粉溶液、
、0.2%淀粉溶液、 、
、 等试剂,探究反应条件对化学反应速率的影响。
等试剂,探究反应条件对化学反应速率的影响。已知:
 (慢)
(慢) (快)
(快)(1)向KI、
 与淀粉的混合溶液中加入一定量的
与淀粉的混合溶液中加入一定量的 溶液,当溶液中的
溶液,当溶液中的 与
与 初始的体积
初始的体积 与
与 量需满足的关系为:
量需满足的关系为:
 (填“>”,“<”,“=”),出现蓝色之前,
(填“>”,“<”,“=”),出现蓝色之前, 在反应中起到的作用是
在反应中起到的作用是(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | 出现蓝色的时间t/s | ||||
 溶液 溶液 | 水 | KI溶液 |  溶液 溶液 | 淀粉溶液 | ||
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 | 10 |
| ② | 5.0 |  | 4.0 | 4.0 | 2.0 | 20 |
| ③ | 10.0 |  | 2.0 | 4.0 | 2.0 | 20 |
| ④ | 10.0 | 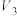 | 4.0 | 2.0 | 2.0 | 5 |



②用
 表示实验序号④的速率为
表示实验序号④的速率为(3)已知某条件下,浓度
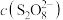 随反应时间t的变化曲线如图,若保持其它条件不变,图中分别画出降低反应温度和加入催化剂时
随反应时间t的变化曲线如图,若保持其它条件不变,图中分别画出降低反应温度和加入催化剂时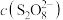 随反应时间t的变化曲线示意图(进行相应的标注)。
随反应时间t的变化曲线示意图(进行相应的标注)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】两套如图所示装置,分别为装置①和装置②,各盛有2g锌粒(颗粒大小相同)。
实验①:在装置①中加入40mL1mol/L的硫酸
实验②:在装置②中加入40mL4mol/L的硫酸。
比较二者收集10mLH2时所用的时间。
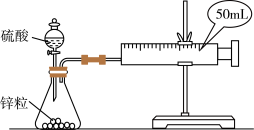
(1)当收集到10mLH2时,哪个实验所耗时间较长?__ (填写实验序号)为什么?__ 。
(2)活塞外移的情况是__ 。
A.均匀外移 B.先快后慢 C.先慢后快 D.先慢后快,然后又逐渐减慢
你选择的理由是__ 。
实验①:在装置①中加入40mL1mol/L的硫酸
实验②:在装置②中加入40mL4mol/L的硫酸。
比较二者收集10mLH2时所用的时间。

(1)当收集到10mLH2时,哪个实验所耗时间较长?
(2)活塞外移的情况是
A.均匀外移 B.先快后慢 C.先慢后快 D.先慢后快,然后又逐渐减慢
你选择的理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】I.某小组同学探究Br2与KI溶液发生置换反应的反应速率的影响因素。
【查阅资料】
a.溴水能将I2氧化为IO 。
。
b.分光光度计可用于测定溶液的吸光度。I2与淀粉的结合物能吸收波长为570 nm的光,其浓度越高,分光光度计测得的吸光度越高。
c.溴水、淀粉、K+、Br-、IO 、I-在波长为570 nm处的吸光度接近为0。
、I-在波长为570 nm处的吸光度接近为0。
【实验过程】
用图1所示装置进行实验。将分光光度计的测定波长调整到570 nm;先向比色皿中加入1.0 mL4.0 mmol·L-1KI溶液(含淀粉),再按照表中所示用量向比色皿中加入蒸馏水和溴水,立即测定溶液的吸光度变化。

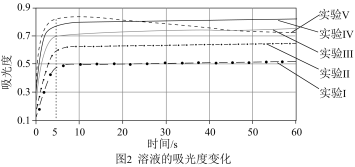
实验数据:
【分析与解释】
(1)Br2与KI溶液发生置换反应的离子方程式为_______ 。
(2)表格中x的数值为_______ 。
(3)能得出结论“随着Br2浓度的增大,Br2与KI溶液发生置换反应的反应速率增大”,依据的实验证据是_______ 。
(4)实验V中,吸光度达到最大值后又下降,可能的原因是_______ 。
II.向2L密闭容器中通入6mol气体A和5mol气体B,在一定条件下发生反应:xA(g)+yB(g) ⇌ pC(g)+qD(g)。已知:平均反应速率v(C)= v(A);反应2min时,A的物质的量减少2mol,B的物质的量减少3mol,有6molD生成。回答下列问题:
v(A);反应2min时,A的物质的量减少2mol,B的物质的量减少3mol,有6molD生成。回答下列问题:
(5)反应2min内,v(B)=_______ 。
(6)化学方程式中,x=_______ ,q=_______ 。
【查阅资料】
a.溴水能将I2氧化为IO
 。
。b.分光光度计可用于测定溶液的吸光度。I2与淀粉的结合物能吸收波长为570 nm的光,其浓度越高,分光光度计测得的吸光度越高。
c.溴水、淀粉、K+、Br-、IO
 、I-在波长为570 nm处的吸光度接近为0。
、I-在波长为570 nm处的吸光度接近为0。【实验过程】
用图1所示装置进行实验。将分光光度计的测定波长调整到570 nm;先向比色皿中加入1.0 mL4.0 mmol·L-1KI溶液(含淀粉),再按照表中所示用量向比色皿中加入蒸馏水和溴水,立即测定溶液的吸光度变化。


实验数据:
| 实验序号 | I | II | III | IV | V | |
| 蒸馏水体积/mL | 1.4 | 1.2 | x | 1.0 | 0.5 | |
| 溴水 | Br2浓度/mmol·L-1 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 |
| 溶液体积/mL | 0.6 | 0.8 | 0.9 | 1.0 | 1.5 | |
(1)Br2与KI溶液发生置换反应的离子方程式为
(2)表格中x的数值为
(3)能得出结论“随着Br2浓度的增大,Br2与KI溶液发生置换反应的反应速率增大”,依据的实验证据是
(4)实验V中,吸光度达到最大值后又下降,可能的原因是
II.向2L密闭容器中通入6mol气体A和5mol气体B,在一定条件下发生反应:xA(g)+yB(g) ⇌ pC(g)+qD(g)。已知:平均反应速率v(C)=
 v(A);反应2min时,A的物质的量减少2mol,B的物质的量减少3mol,有6molD生成。回答下列问题:
v(A);反应2min时,A的物质的量减少2mol,B的物质的量减少3mol,有6molD生成。回答下列问题:(5)反应2min内,v(B)=
(6)化学方程式中,x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】H2O2被称为绿色氧化剂,其性质的研究极其重要。某同学以H2O2分解为例,按照表中数据探究温度、浓度、催化剂、酸对反应速率的影响。
(1)在实验①和②中,H2O2分解速率较快的是_______ ,实验②和③的目的是_______ ;
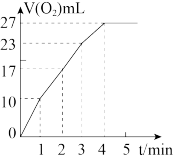
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出的实验结论是_______ 。

III.如图:另一个同学将状态不同的1gMnO2分别加入盛有30mL等浓度的H2O2溶液的锥形瓶中,产生气体进入注射器针筒中,记录结果如表:
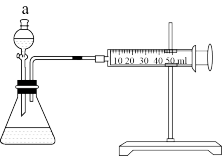
(3)锥形瓶中发生反应的化学方程式_______ ,该反应是_______ 反应(填“放热”或“吸热”),装置a的名称_______ ,实验结果表明,催化剂的催化效果与_______ 有关。
(4)实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因_______ 。
| 编号 | 反应物 | 催化剂 | 温度 |
| ① | 20mL2%H2O2溶液+2mLH2O | 无 | 20℃ |
| ② | 20mL5%H2O2溶液+2mLH2O | 无 | 20℃ |
| ③ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 20℃ |
| ④ | 20mL5%H2O2溶液+2mL1mol/LHCl溶液 | 1g粉末状MnO2 | 20℃ |
| ⑤ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 40℃ |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出的实验结论是

III.如图:另一个同学将状态不同的1gMnO2分别加入盛有30mL等浓度的H2O2溶液的锥形瓶中,产生气体进入注射器针筒中,记录结果如表:

| MnO2状态 | 触摸试管情况 | 该温度下针筒内收集到气体的体积 | 所需时间 |
| 粉末状 | 很烫 | 30mL | 3min |
| 块状 | 微热 | 30mL | 9min |
(4)实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸锌是一种重要的工业原料,ZnSO4∙H2O可用于制造印染用的媒染剂,木材及皮革保存剂等。以炼锌厂锌渣为原料,含ZnO、FeO、CuO、CdO等,生产ZnSO4∙H2O的流程如下:
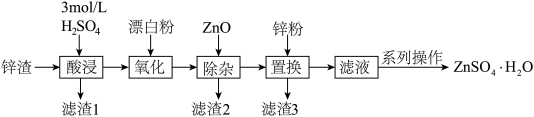
已知:①当溶液中剩余离子浓度小于1×10-5 mol∙L-1时,认为生成沉淀的反应进行完全;
②常温下,Ksp[Fe(OH)3]= 4.0×10-38,Ksp[Fe(OH)2]= 4.9×10-17,Ksp[Cu(OH)2]= 2.2×10-20,Ksp[Zn(OH)2]=1×10-17。
(1)“酸浸”时,需不断通入高温水蒸气,其目的是___________ (填字母)。用18 mol∙L-1的浓硫酸配制3 mol∙L-1H2SO4溶液,下列操作会使所配溶液浓度偏小的是___________ (填字母)。
(2)结合必要的化学反应方程式,从平衡角度解释加入ZnO得到滤渣2的原理:___________ 。除杂过程中,若控制pH=4,溶液中c(Fe3+)=___________ mol∙L-1。结合实际生产情况一般取pH4.5~5.0,pH不宜过大的原因是___________ 。
(3)滤渣3含有Zn和___________ (写化学式)。
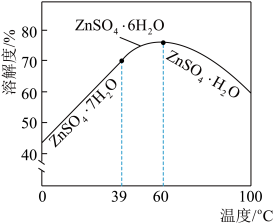
(4)硫酸锌晶体的溶解度与温度的变化如图所示。“系列操作”是:___________ ,洗涤、干燥。

已知:①当溶液中剩余离子浓度小于1×10-5 mol∙L-1时,认为生成沉淀的反应进行完全;
②常温下,Ksp[Fe(OH)3]= 4.0×10-38,Ksp[Fe(OH)2]= 4.9×10-17,Ksp[Cu(OH)2]= 2.2×10-20,Ksp[Zn(OH)2]=1×10-17。
(1)“酸浸”时,需不断通入高温水蒸气,其目的是

(2)结合必要的化学反应方程式,从平衡角度解释加入ZnO得到滤渣2的原理:
(3)滤渣3含有Zn和
(4)硫酸锌晶体的溶解度与温度的变化如图所示。“系列操作”是:

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气中含有CO、NO等有害气体。
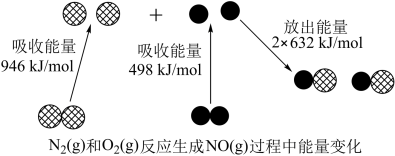
(1)汽车尾气中NO生成过程的能量变化如图示。1molN2和1molO2完全反应生成NO会________ (填“吸收”或“放出”)________ kJ能量。
(2)一种新型催化剂用于NO和CO的反应:2NO+2CO 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
①请将表中数据补充完整:a___________ 。
②能验证温度对化学反应速率规律的是实验____________________ (填实验序号)。
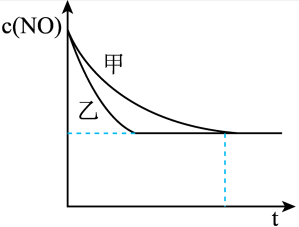
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线________________ (填“甲”或“乙”)。
④在容积固定的容器中发生反应2NO+2CO 2CO2+N2,不能说明已达到平衡状态的是
2CO2+N2,不能说明已达到平衡状态的是________ (不定项选择);
A.容器内CO浓度不变 B.容器内NO的浓度等于CO2的浓度
C.v逆(NO)=2v正(N2) D.容器内混合气体密度保持不变
(1)汽车尾气中NO生成过程的能量变化如图示。1molN2和1molO2完全反应生成NO会

(2)一种新型催化剂用于NO和CO的反应:2NO+2CO
 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。| 实验编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.2×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.2×10-3 | b | 124 |
| Ⅲ | 350 | a | 5.80×10-3 | 82 |
①请将表中数据补充完整:a
②能验证温度对化学反应速率规律的是实验
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线

④在容积固定的容器中发生反应2NO+2CO
 2CO2+N2,不能说明已达到平衡状态的是
2CO2+N2,不能说明已达到平衡状态的是A.容器内CO浓度不变 B.容器内NO的浓度等于CO2的浓度
C.v逆(NO)=2v正(N2) D.容器内混合气体密度保持不变
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】“环境就是民生,青山就是美丽,蓝天也是幸福。”拥有天蓝、地绿、水净的美好家园,是每个中国人的梦想。回答下列问题:
(1)汽车尾气(含CO、N2、SO2和NO等)是城市空气污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转化器”,它能使一氧化碳跟一氧化氮反应生成可参与大气生态循环的无毒气体。写出在催化剂的作用下CO跟NO反应的化学方程式___________ 。
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氮废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以 和NH3·H2O形式存在,为达到变废为宝回收利用的目的某团队设计处理流程如下:
和NH3·H2O形式存在,为达到变废为宝回收利用的目的某团队设计处理流程如下:___________ 。
②过程Ⅱ为硝化过程,在微生物的作用下实现 →
→ →
→ 的转化,在碱性条件下,
的转化,在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为___________ 。
③过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→ →N2的转化,将0.5mol
→N2的转化,将0.5mol 完全转化为N2,转移电子的物质的量为
完全转化为N2,转移电子的物质的量为___________ 。
(3)按如图所示装置探究浓、稀硝酸氧化性的相对强弱(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
①装置b、c、d中盛放的药品依次是___________ 、___________ 、___________ 。其中装置a中发生反应的化学方程式是___________ 。
②实验结束后,同学们发现装置a中溶液呈绿色,而不显蓝色。针对溶液呈绿色的原因,提出以下假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
探究如下:取装置a中绿色溶液,分为两等份。
取一份于如图所示装置中,___________ (填“操作”和“现象”),证实装置a中溶解了NO2。___________ (填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(1)汽车尾气(含CO、N2、SO2和NO等)是城市空气污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转化器”,它能使一氧化碳跟一氧化氮反应生成可参与大气生态循环的无毒气体。写出在催化剂的作用下CO跟NO反应的化学方程式
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氮废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以
 和NH3·H2O形式存在,为达到变废为宝回收利用的目的某团队设计处理流程如下:
和NH3·H2O形式存在,为达到变废为宝回收利用的目的某团队设计处理流程如下: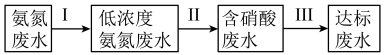
②过程Ⅱ为硝化过程,在微生物的作用下实现
 →
→ →
→ 的转化,在碱性条件下,
的转化,在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为③过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→
 →N2的转化,将0.5mol
→N2的转化,将0.5mol 完全转化为N2,转移电子的物质的量为
完全转化为N2,转移电子的物质的量为(3)按如图所示装置探究浓、稀硝酸氧化性的相对强弱(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
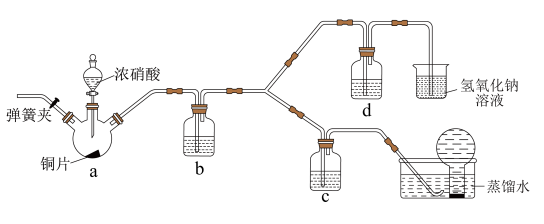
①装置b、c、d中盛放的药品依次是
②实验结束后,同学们发现装置a中溶液呈绿色,而不显蓝色。针对溶液呈绿色的原因,提出以下假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
探究如下:取装置a中绿色溶液,分为两等份。
取一份于如图所示装置中,
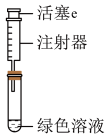
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
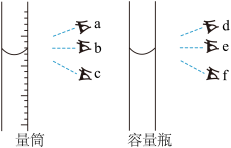
【推荐2】某课外小组为鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验:

(1)装置I中温度降低的是________ ;溶解度大的是_______ 。(选填固体的化学式,下同)
(2)装置II中反应后气球相对小的试管中发生的化学反应方程式为_________ 。
(3)装置III中澄清石灰水变浑浊的离子反应方程式________ 。
(4)装置IV试管C中装入的固体是_____ (填化学式),石灰水变浑浊的是试管_____ (填字母)。

(1)装置I中温度降低的是
(2)装置II中反应后气球相对小的试管中发生的化学反应方程式为
(3)装置III中澄清石灰水变浑浊的离子反应方程式
(4)装置IV试管C中装入的固体是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】在实验过程中,若一种气体极易溶于一种液体,则容易发生倒吸现象,给实验造成危险。现有4位同学分别设计了一个实验,希望通过观察到的明显现象来说明二氧化碳极易溶于氢氧化钠溶液,设计的装置如下:

其中一位同学向充满二氧化碳的塑料瓶D中加入氢氧化钠溶液,盖紧瓶塞后振荡,如果看到瓶子变瘪了,说明二氧化碳与氢氧化钠溶液发生了反应。对装置A~C,将能达到实验目的的装置、操作方法和实验现象填入下表(可不填满):
_______________________________

其中一位同学向充满二氧化碳的塑料瓶D中加入氢氧化钠溶液,盖紧瓶塞后振荡,如果看到瓶子变瘪了,说明二氧化碳与氢氧化钠溶液发生了反应。对装置A~C,将能达到实验目的的装置、操作方法和实验现象填入下表(可不填满):
| 所选装置 | 操作方法 | 实验现象 |
您最近一年使用:0次



