防治环境污染,改善生态环境已成为全球共识。十九大报告提出“要像对待生命一样对待生态环境”。回答下列问题:
Ⅰ.大气污染
(1)下列物质会形成酸雨的是___________ (填字母)。
A.碳氧化物 B.硫氧化物 C.氮氧化物
(2)汽车尾气处理:在汽车排气管上安装催化转化器,将其中的有害气体NO、CO转化为无害气体,反应的化学方程式为___________ 。
(3)工业上消除氮氧化物的污染可用如下反应; 。反应中还原剂为
。反应中还原剂为___________ (填化学式);若反应中消耗1mol ,则转移电子的物质的量为
,则转移电子的物质的量为___________ mol。
Ⅱ.水体污染
(4)过量排放含氮元素的废水,会引起水华等水体污染问题。含有大量 的废水脱氮可以用NaClO氧化法。一定条件下,溶液pH对NaClO去除
的废水脱氮可以用NaClO氧化法。一定条件下,溶液pH对NaClO去除 能力的影响如图所示。
能力的影响如图所示。

① 时,NaClO溶液氧化
时,NaClO溶液氧化 生成
生成 和
和 的离子方程式为
的离子方程式为___________ 。
②去除氨氮废水适宜的pH约为___________ 。
(5)测定废水中的氮含量:取a g废水,将所含氮完全转化为 ,所得
,所得 用过量的
用过量的 mL
mL 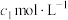
 溶液完全吸收,剩余
溶液完全吸收,剩余 用
用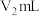
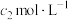 NaOH溶液恰好中和,则废水中氮元素的质量分数是
NaOH溶液恰好中和,则废水中氮元素的质量分数是___________ 。
Ⅰ.大气污染
(1)下列物质会形成酸雨的是
A.碳氧化物 B.硫氧化物 C.氮氧化物
(2)汽车尾气处理:在汽车排气管上安装催化转化器,将其中的有害气体NO、CO转化为无害气体,反应的化学方程式为
(3)工业上消除氮氧化物的污染可用如下反应;
 。反应中还原剂为
。反应中还原剂为 ,则转移电子的物质的量为
,则转移电子的物质的量为Ⅱ.水体污染
(4)过量排放含氮元素的废水,会引起水华等水体污染问题。含有大量
 的废水脱氮可以用NaClO氧化法。一定条件下,溶液pH对NaClO去除
的废水脱氮可以用NaClO氧化法。一定条件下,溶液pH对NaClO去除 能力的影响如图所示。
能力的影响如图所示。
①
 时,NaClO溶液氧化
时,NaClO溶液氧化 生成
生成 和
和 的离子方程式为
的离子方程式为②去除氨氮废水适宜的pH约为
(5)测定废水中的氮含量:取a g废水,将所含氮完全转化为
 ,所得
,所得 用过量的
用过量的 mL
mL 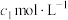
 溶液完全吸收,剩余
溶液完全吸收,剩余 用
用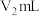
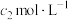 NaOH溶液恰好中和,则废水中氮元素的质量分数是
NaOH溶液恰好中和,则废水中氮元素的质量分数是
更新时间:2023-05-28 15:14:44
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)我国四大发明之一的火药是由硫磺粉、硝酸钾、木炭粉按一定比例混合而成的,爆炸时的反应为 ,在该反应的生成物中,属于非电解质的物质是
,在该反应的生成物中,属于非电解质的物质是_____ (填化学式,下同),属于电解质的物质是_____ ,还原产物是_____ ;当3.2gS参与反应时,生成的气体体积为_____ L(标准状况下)。
(2) 是高效、绿色的水处理剂,其原理如图所示。
是高效、绿色的水处理剂,其原理如图所示。
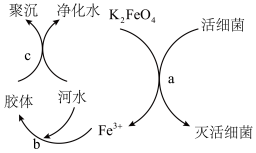
①从物质的类别来看,高铁酸钾( )属于
)属于_____ (“酸”“碱”“盐”或“氧化物”)。
②从元素的化合价角度来看, 中铁的化合价为
中铁的化合价为_____ 价,则过程a中 体现了
体现了_____ (填“氧化”或“还原”)性,活细菌发生了_____ 反应,该过程中消耗0.2mol 时,转移的电子数目为
时,转移的电子数目为_____ 。
(3)纯碱和小苏打是日常家庭厨房中的常见用品,从物质的类别来看,均属于盐类。若取适量小苏打加水溶解,配制成溶液,再向其中加入少量澄清石灰水,发生反应的离子方程式是_____ 。
(1)我国四大发明之一的火药是由硫磺粉、硝酸钾、木炭粉按一定比例混合而成的,爆炸时的反应为
 ,在该反应的生成物中,属于非电解质的物质是
,在该反应的生成物中,属于非电解质的物质是(2)
 是高效、绿色的水处理剂,其原理如图所示。
是高效、绿色的水处理剂,其原理如图所示。
①从物质的类别来看,高铁酸钾(
 )属于
)属于②从元素的化合价角度来看,
 中铁的化合价为
中铁的化合价为 体现了
体现了 时,转移的电子数目为
时,转移的电子数目为(3)纯碱和小苏打是日常家庭厨房中的常见用品,从物质的类别来看,均属于盐类。若取适量小苏打加水溶解,配制成溶液,再向其中加入少量澄清石灰水,发生反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】写出下列反应的离子方程式。
(1)碳酸银溶于稀硝酸___________
(2)工业上用稀硫酸除铁锈(Fe2O3)___________
(3)向Ba(OH)2溶液中逐渐加入NaHSO4溶液至钡离子完全沉淀___________
(4)用滴管向棉花上(包有少量Na2O2)滴几滴水,棉花立刻燃烧起来___________
(5)漂白粉溶于水中,对染色的衣物起到漂白作用,原理___________
(6)工业废水中Cr2O72-有毒,酸性条件下用FeSO4·7H2O做处理剂,将Cr2O72-转化为Cr3+________ 。
(1)碳酸银溶于稀硝酸
(2)工业上用稀硫酸除铁锈(Fe2O3)
(3)向Ba(OH)2溶液中逐渐加入NaHSO4溶液至钡离子完全沉淀
(4)用滴管向棉花上(包有少量Na2O2)滴几滴水,棉花立刻燃烧起来
(5)漂白粉溶于水中,对染色的衣物起到漂白作用,原理
(6)工业废水中Cr2O72-有毒,酸性条件下用FeSO4·7H2O做处理剂,将Cr2O72-转化为Cr3+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列十种物质:① ②铝③
②铝③ ④
④ ⑤
⑤ ⑥
⑥ ⑦氢氧化铁胶体⑧稀盐酸⑨
⑦氢氧化铁胶体⑧稀盐酸⑨ 溶液⑩
溶液⑩
(1)以上物质属于电解质的是___________ (填序号)。
(2)写出①与③反应的离子反应方程式___________ 。
(3)将⑨的饱和溶液滴入沸水中可以制得⑦,写出该化学方程式_____ ,是否制备成功可以通过____ (性质或现象检验)来检测。
(4)写出将少量④通入澄清石灰水中的离子反应方程式___________
 ②铝③
②铝③ ④
④ ⑤
⑤ ⑥
⑥ ⑦氢氧化铁胶体⑧稀盐酸⑨
⑦氢氧化铁胶体⑧稀盐酸⑨ 溶液⑩
溶液⑩
(1)以上物质属于电解质的是
(2)写出①与③反应的离子反应方程式
(3)将⑨的饱和溶液滴入沸水中可以制得⑦,写出该化学方程式
(4)写出将少量④通入澄清石灰水中的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列六种物质:①液态氯化氢;②二氧化碳;③硫酸铜溶液;④熔融氯化钠;⑤ 固体;⑥铁丝.
固体;⑥铁丝.
(1)上述六种物质中,属于非电解质的是__________ ,能导电的电解质是__________ (填序号)。
(2)③和⑥反应的基本反应类型为__________ ,其离子方程式为__________ 。
(3)氯化氢在水溶液中的电离方程式为__________ 。
(4)向③中加入⑤的水溶液的现象为__________ 。
(5) 与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失
与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失______ 。
__________ __________
__________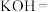 __________
__________ __________
__________ __________
__________
 固体;⑥铁丝.
固体;⑥铁丝.(1)上述六种物质中,属于非电解质的是
(2)③和⑥反应的基本反应类型为
(3)氯化氢在水溶液中的电离方程式为
(4)向③中加入⑤的水溶液的现象为
(5)
 与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失
与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失__________
 __________
__________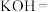 __________
__________ __________
__________ __________
__________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请按要求书写下列离子方程式:
(1)利用FeCl3溶液制备胶体的离子方程式为_______________________________ ;
(2)将过量的 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式________________________ 。
(3)FeSO4的酸性溶液与H2O2反应试写出该反应的离子方程式:____________________ ;
(4)氧化亚铜中加入稀硫酸____________________________ ;
(5)工业上用次氯酸钠和FeCl3在碱性条件下制备新型绿色消毒剂高铁酸钠(Na2FeO4)该反应的离子方程式是:______________________________ 。
(1)利用FeCl3溶液制备胶体的离子方程式为
(2)将过量的
 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式(3)FeSO4的酸性溶液与H2O2反应试写出该反应的离子方程式:
(4)氧化亚铜中加入稀硫酸
(5)工业上用次氯酸钠和FeCl3在碱性条件下制备新型绿色消毒剂高铁酸钠(Na2FeO4)该反应的离子方程式是:
您最近一年使用:0次
【推荐3】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2。它能被常见的强氧化剂氧化,在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是_________ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是_________ (填序号)。
A.测定这两种溶液的pH B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别 D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:____________________________________ 。
(4)Fe与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是_________ (填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1。试配平下列方程式:
FeSO4+________ K2O2→ K2FeO4+ K2O+ K2SO4+ O2↑
当转移了1.5NA个电子时,在标况下可收集到_________ 升氧气。
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.测定这两种溶液的pH B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别 D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1。试配平下列方程式:
FeSO4+
当转移了1.5NA个电子时,在标况下可收集到
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在a、b两支试管中,分别装上质量相等形状相同的一颗锌粒,然后向两支试管中:
(1)分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。则a、b两支试管中的现象:相同点是_______ ;不同点是_______ ,反应完毕后生成气体的总体积是a_______ b。
(2)分别加入相同pH、相同体积的稀盐酸和稀醋酸时,两支试管中的反应速率在反应刚开始时是a_______ b(填“大于”、“等于”或“小于”下同),当两种酸都反应完毕后生成气体的体积是a_______ b
(1)分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。则a、b两支试管中的现象:相同点是
(2)分别加入相同pH、相同体积的稀盐酸和稀醋酸时,两支试管中的反应速率在反应刚开始时是a
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】乙二酸 俗称草酸,在实验研究和化学工业中应用广泛。
俗称草酸,在实验研究和化学工业中应用广泛。
(1)25℃时,向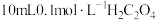 溶液中逐滴加入
溶液中逐滴加入 溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:

① 等浓度的Na2C2O4和NaHC2O4混合溶液显_______ 性。(填“酸”“碱”或“中”);25℃时,草酸的电离平衡常数分别是 、
、 ,则
,则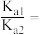
_______ 。
② a点溶液中,
_______ 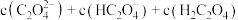 (填“>”“=”或“<”),此时溶液的pH=
(填“>”“=”或“<”),此时溶液的pH=_______ 。
(2)① 酸性高锰酸钾应该用_______ (填“酸式”或“碱式”)滴定管盛装。
② 若要测定草酸亚铁晶体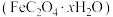 的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用
的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用 酸性溶液滴定,达到滴定终点时,消耗
酸性溶液滴定,达到滴定终点时,消耗 的酸性
的酸性 溶液18.00mL。则x=
溶液18.00mL。则x=_______ 。
 俗称草酸,在实验研究和化学工业中应用广泛。
俗称草酸,在实验研究和化学工业中应用广泛。(1)25℃时,向
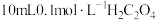 溶液中逐滴加入
溶液中逐滴加入 溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
① 等浓度的Na2C2O4和NaHC2O4混合溶液显
 、
、 ,则
,则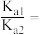
② a点溶液中,

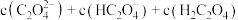 (填“>”“=”或“<”),此时溶液的pH=
(填“>”“=”或“<”),此时溶液的pH=(2)① 酸性高锰酸钾应该用
② 若要测定草酸亚铁晶体
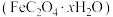 的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用
的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用 酸性溶液滴定,达到滴定终点时,消耗
酸性溶液滴定,达到滴定终点时,消耗 的酸性
的酸性 溶液18.00mL。则x=
溶液18.00mL。则x=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】新型电池在飞速发展的信息技术中发挥着越来越重要的作用。
Li2FeSiO4是极具发展潜力的新型锂离子电池电极材料,在苹果的几款最新型的产品中已经有了一定程度的应用。其中一种制备Li2FeSiO4的方法为:
固相法:2Li2SiO3+FeSO4=Li2FeSiO4+Li2SO4+SiO2
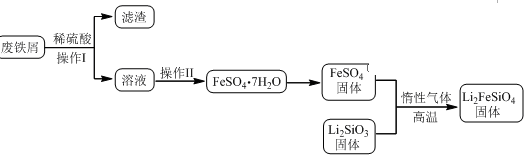
某学习小组按如下实验流程制备Li2FeSiO4并测定所得产品中Li2FeSiO4的含量。
实验(一)制备流程:
实验(二) Li2FeSiO4含量测定:
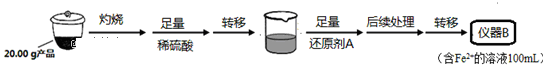
从仪器B中取20.00mL溶液至锥形瓶中,另取0.20mol•L-1的酸性KMnO4标准溶液装入仪器C中,用氧化还原滴定法测定Fe2+含量,杂质不与酸性KMnO4标准溶液反应。经4次滴定,每次消耗KMnO4溶液的体积如下:
(1)实验(二)中的仪器名称:仪器B____ ,仪器C____ 。
(2)制备Li2FeSiO4时必须在惰性气体氛围中进行,其原因是____ 。
(3)在操作Ⅰ时,所需用到的玻璃仪器中,除了普通漏斗、烧杯外,还需____ ;
(4)操作Ⅱ的步骤是:__ 、__ 、过滤、洗涤。
(5)还原剂A可用SO2,写出该反应的离子方程式____ ,此时后续处理的主要目的是____ 。
(6)滴定终点时现象为____ ;根据滴定结果,可确定产品中Li2FeSiO4的质量分数为____ ;若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的Li2FeSiO4含量____ (填“偏高”、“偏低”或“不变”)。
Li2FeSiO4是极具发展潜力的新型锂离子电池电极材料,在苹果的几款最新型的产品中已经有了一定程度的应用。其中一种制备Li2FeSiO4的方法为:
固相法:2Li2SiO3+FeSO4=Li2FeSiO4+Li2SO4+SiO2
某学习小组按如下实验流程制备Li2FeSiO4并测定所得产品中Li2FeSiO4的含量。
实验(一)制备流程:

实验(二) Li2FeSiO4含量测定:

从仪器B中取20.00mL溶液至锥形瓶中,另取0.20mol•L-1的酸性KMnO4标准溶液装入仪器C中,用氧化还原滴定法测定Fe2+含量,杂质不与酸性KMnO4标准溶液反应。经4次滴定,每次消耗KMnO4溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积 | 20.00mL | 19.98mL | 22.40mL | 20.02mL |
(2)制备Li2FeSiO4时必须在惰性气体氛围中进行,其原因是
(3)在操作Ⅰ时,所需用到的玻璃仪器中,除了普通漏斗、烧杯外,还需
(4)操作Ⅱ的步骤是:
(5)还原剂A可用SO2,写出该反应的离子方程式
(6)滴定终点时现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】2021年12月13日从天津市疫情防控指挥部获悉,中国内地首次发现新冠病毒“奥密克戎”变异株。当下疫情对生产生活仍然影响极大,人们认识到日常杀菌消毒的重要性,其中含氯消毒剂在生产生活中有着广泛的用途。回答下列问题:
(1)写出实验室中制取氯气的离子方程式:___________ 。
(2)已知 与浓盐酸反应的化学方程式:
与浓盐酸反应的化学方程式: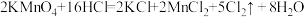 ,该反应也可以用来制取氯气,
,该反应也可以用来制取氯气,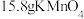 能和
能和___________ 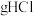 发生上述反应,其中有
发生上述反应,其中有___________ 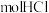 被氧化,产生的
被氧化,产生的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(3)实验室还可以利用如下反应制取氯气: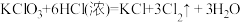 。若制取标准状况下
。若制取标准状况下 氯气,反应过程中转移电子的物质的量为
氯气,反应过程中转移电子的物质的量为___________ 。
(1)写出实验室中制取氯气的离子方程式:
(2)已知
 与浓盐酸反应的化学方程式:
与浓盐酸反应的化学方程式: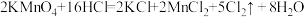 ,该反应也可以用来制取氯气,
,该反应也可以用来制取氯气,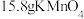 能和
能和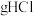 发生上述反应,其中有
发生上述反应,其中有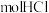 被氧化,产生的
被氧化,产生的 在标准状况下的体积为
在标准状况下的体积为(3)实验室还可以利用如下反应制取氯气:
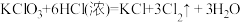 。若制取标准状况下
。若制取标准状况下 氯气,反应过程中转移电子的物质的量为
氯气,反应过程中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括
(2)
 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(用化学方程式表示)(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是 (填字母)。
A. 能与水反应 能与水反应 | B. 在一定条件下能与氧化钙反应 在一定条件下能与氧化钙反应 |
C. 是制作光导纤维的主要原料 是制作光导纤维的主要原料 | D. 能与稀硫酸反应 能与稀硫酸反应 |
 )还原法是当前制备高纯硅的主要方法,生产过程如图:
)还原法是当前制备高纯硅的主要方法,生产过程如图:石英砂 粗硅
粗硅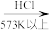
 (粗)
(粗)
 (纯)
(纯) 高纯硅
高纯硅
①写出制粗硅的化学方程式
②整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和一种气体单质,写出发生反应的化学方程式
、HCl和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是
(5)新型陶瓷材料氮化硅(
 )可应用于原子反应堆,一种制备氮化硅的反应如下:
)可应用于原子反应堆,一种制备氮化硅的反应如下:
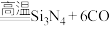 。若生成标准状况下33.6L CO时,反应过程中转移的电子数为
。若生成标准状况下33.6L CO时,反应过程中转移的电子数为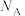 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】浩瀚的大海具有丰富的化学资源可以开发和利用,回答下列相关问题:
(1)纯碱是人类最早制取和使用的化学物质之一,其属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。我国化学家侯德榜发明了联合制碱法,制取方法是向饱和食盐水先通入足量 ,再通入过量
,再通入过量 ,得到
,得到_______ (填化学式)晶体,过滤,再由该晶体制得纯碱的化学方程式为_______ 。
(2)日前很多自来水厂使用 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,该反应的还原产物为
,该反应的还原产物为_______ ,若制得1mol  ,转移电子的数目为
,转移电子的数目为_______ 。
(3)金属钠可用于生产汽车安全气囊中的气体发生剂 ,某汽车安全气囊中含
,某汽车安全气囊中含 、
、 和
和 等物质。
等物质。
①当汽车发生较严重的碰撞时, 受热分解为Na和
受热分解为Na和 ,其化学方程式为
,其化学方程式为_______ 。
②气囊中产生的Na立即与 反应生成
反应生成 与另一种单质,该反应属于四种基本反向类型中的
与另一种单质,该反应属于四种基本反向类型中的_______ 反应。
(1)纯碱是人类最早制取和使用的化学物质之一,其属于
 ,再通入过量
,再通入过量 ,得到
,得到(2)日前很多自来水厂使用
 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,该反应的还原产物为
,该反应的还原产物为 ,转移电子的数目为
,转移电子的数目为(3)金属钠可用于生产汽车安全气囊中的气体发生剂
 ,某汽车安全气囊中含
,某汽车安全气囊中含 、
、 和
和 等物质。
等物质。①当汽车发生较严重的碰撞时,
 受热分解为Na和
受热分解为Na和 ,其化学方程式为
,其化学方程式为②气囊中产生的Na立即与
 反应生成
反应生成 与另一种单质,该反应属于四种基本反向类型中的
与另一种单质,该反应属于四种基本反向类型中的
您最近一年使用:0次



