在一定温度下,向一容积为5L的恒容密闭容器中充入2molSO2和1molO2,发生反应:2SO2(g)+O2(g) 2SO3(g) ∆H=-196 kJ∙mol-1;经5min后达到平衡,此时容器内压强与起始压强之比为0.7,请回答下列问题:
2SO3(g) ∆H=-196 kJ∙mol-1;经5min后达到平衡,此时容器内压强与起始压强之比为0.7,请回答下列问题:
(1)判断该反应达到平衡状态的标志是_______(填字母)。
(2)从反应开始到平衡的这段时间,SO2的平均反应速率v(SO2)=_______ mol·L-1·min-1。
(3)达平衡时SO2的转化率为_______ ,达到平衡时反应放出的热量为_______ kJ。
(4)从理论上分析,为了使二氧化硫尽可能多的转化为三氧化硫,应选择的条件是_______ (填“低温高压”“低温低压”“高温高压”或“高温低压”)。实际生产时选用温度400~500℃,压强采用常压的原因是_______ 。
(5)如图表示平衡时SO2的体积分数随压强和温度变化的曲线。
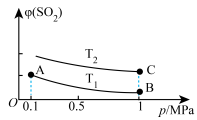
则温度关系:T1_______ T2(填“>”“<”或“=”),A、B、C三点的化学平衡常数的关系是_______ 。
 2SO3(g) ∆H=-196 kJ∙mol-1;经5min后达到平衡,此时容器内压强与起始压强之比为0.7,请回答下列问题:
2SO3(g) ∆H=-196 kJ∙mol-1;经5min后达到平衡,此时容器内压强与起始压强之比为0.7,请回答下列问题:(1)判断该反应达到平衡状态的标志是_______(填字母)。
| A.SO2的物质的量不再变化 |
| B.容器内混合气体的密度保持不变 |
| C.SO2的生成速率和SO3的生成速率相等 |
D.SO2、O2、SO3三者的浓度之比为 |
(3)达平衡时SO2的转化率为
(4)从理论上分析,为了使二氧化硫尽可能多的转化为三氧化硫,应选择的条件是
(5)如图表示平衡时SO2的体积分数随压强和温度变化的曲线。

则温度关系:T1
更新时间:2023-05-06 20:41:57
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】深入研究C、N元素的化合物有重要意义。
(1)已知:

①若该反应每转移1mol 释放186.5kJ的热量,则处理2mol NO同时释放热量
释放186.5kJ的热量,则处理2mol NO同时释放热量___________ kJ。
②查阅资料,可知从热力学角度看,即使在汽车尾气浓度很低的条件下,上述反应的进行程度也应该很大,实际上一段时间内测得汽车尾气中该反应进行的程度很小,原因可能是___________ ,要增大汽车尾气中该反应的程度,关键是要___________ 。
(2)一定温度下,在2L密闭容器中发生反应: 。下列能够表示该反应到达平衡状态的是
。下列能够表示该反应到达平衡状态的是___________ 。若2分钟内消耗1mol的CO,则用氢气表示这段时间的反应速率为___________  。
。
A.氢气的体积分数保持不变
B.CO和 的消耗速率相同
的消耗速率相同
C.气体的密度保持不变
(3)1073K时发生反应: 。反应开始的瞬时速率v与初始浓度c的实验数据如下表:
。反应开始的瞬时速率v与初始浓度c的实验数据如下表:
该反应的速率方程为___________ (用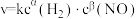 表示,其中k为速率常数,k、
表示,其中k为速率常数,k、 、
、 要求出具体数值)。
要求出具体数值)。
(1)已知:


①若该反应每转移1mol
 释放186.5kJ的热量,则处理2mol NO同时释放热量
释放186.5kJ的热量,则处理2mol NO同时释放热量②查阅资料,可知从热力学角度看,即使在汽车尾气浓度很低的条件下,上述反应的进行程度也应该很大,实际上一段时间内测得汽车尾气中该反应进行的程度很小,原因可能是
(2)一定温度下,在2L密闭容器中发生反应:
 。下列能够表示该反应到达平衡状态的是
。下列能够表示该反应到达平衡状态的是 。
。A.氢气的体积分数保持不变
B.CO和
 的消耗速率相同
的消耗速率相同C.气体的密度保持不变
(3)1073K时发生反应:
 。反应开始的瞬时速率v与初始浓度c的实验数据如下表:
。反应开始的瞬时速率v与初始浓度c的实验数据如下表:| 实验编号 | 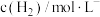 | 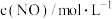 | 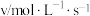 |
| 1 | 0.0060 | 0.0010 | 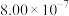 |
| 2 | 0.0060 | 0.0020 | 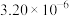 |
| 3 | 0.0060 | 0.0040 | 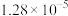 |
| 4 | 0.0030 | 0.0040 |  |
| 5 | 0.0015 | 0.0040 | 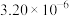 |
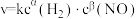 表示,其中k为速率常数,k、
表示,其中k为速率常数,k、 、
、 要求出具体数值)。
要求出具体数值)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氮氧化物和SO2是大气主要污染物,研究它们的转化关系有利于防治污染。
(1)已知:
I.2NO(g)+O2(g) 2NO2(g)△H=-113.0kJ•mol-1
2NO2(g)△H=-113.0kJ•mol-1
II.2SO2(g)+O2(g) 2SO3(g)△H=-196.6kJ•mol-1
2SO3(g)△H=-196.6kJ•mol-1
III.NO2(g)+SO2(g) SO3(g)+NO(g)△H=
SO3(g)+NO(g)△H=_____ 。
(2)氨氧化物破坏臭氧层原理:①NO+O3=NO2+O2、②NO2+O=NO+O2。常温下反应①的平衡常数为K1,反应②的平衡常数为K2,则反应O3+O=2O2的平衡常数K=_____ 。(用K1、K2表示)。一氧化氮在该反应中的作用是_____ 。
(3)反应II2SO2(g)+O2(g)=2SO3(g)在0.1Mpa、450℃的恒压容器中测得相关数据如表:
该温度下用分压表示的平衡常数(气体分压=总压x物质的量分数)Kp=______ (列出计算式)。写出一种能提高SO2平衡转化率的措施_____ 。
(4)烟气同时脱硫脱硝是目前的发展趋势。一种ClO2气相氧化法烟气脱硫脱硝反应机理和速率常数(k)如下:
脱硝:
a.NO(g)+ClO2(g)=NO2(g)+ClO(g)△H1k1=1.7×10mL•(mol•s)-1
b.NO(g)+ClO(g)=NO2(g)+Cl(g)△H2k2=8.8×1012mL•(mol•s)-1
脱硫:
c.SO2(g)+ClO2(g)=SO3(g)+ClO(g)△H3k3=2.1×10-4mL•(mol•s)-1
d.SO2(g)+ClO(g)=SO2(g)+Cl(g)△H4k4=6.9×1011mL•(mol•s)-1
①已知反应c、d的速率方程分别为v正=k3c(SO2)•c(ClO2)、v正=k4c(SO2)•c(ClO),试判断两反应的活化能大小:E3_____ E4(填“>”“<”或“=”)。控制脱硫速度的关键步骤是反应_____ (填c或d)。
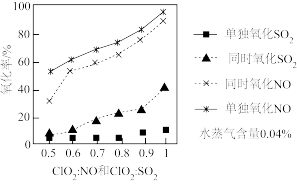
②SO2、NO单独氧化及同时氧化对两气体氧化率变化如图,同时氧化对______ 气体的氧化率影响明显,结合以上反应及其速率常数分析原因______ 。
(1)已知:
I.2NO(g)+O2(g)
 2NO2(g)△H=-113.0kJ•mol-1
2NO2(g)△H=-113.0kJ•mol-1II.2SO2(g)+O2(g)
 2SO3(g)△H=-196.6kJ•mol-1
2SO3(g)△H=-196.6kJ•mol-1III.NO2(g)+SO2(g)
 SO3(g)+NO(g)△H=
SO3(g)+NO(g)△H=(2)氨氧化物破坏臭氧层原理:①NO+O3=NO2+O2、②NO2+O=NO+O2。常温下反应①的平衡常数为K1,反应②的平衡常数为K2,则反应O3+O=2O2的平衡常数K=
(3)反应II2SO2(g)+O2(g)=2SO3(g)在0.1Mpa、450℃的恒压容器中测得相关数据如表:
| 起始原料气体积分数 | 平衡混合气体积分数 | |
| N2 | 82% | 84.9% |
| SO2 | 7% | 0.18% |
| O2 | 11% | 7.86% |
| SO3 | 0 | 7.06% |
该温度下用分压表示的平衡常数(气体分压=总压x物质的量分数)Kp=
(4)烟气同时脱硫脱硝是目前的发展趋势。一种ClO2气相氧化法烟气脱硫脱硝反应机理和速率常数(k)如下:
脱硝:
a.NO(g)+ClO2(g)=NO2(g)+ClO(g)△H1k1=1.7×10mL•(mol•s)-1
b.NO(g)+ClO(g)=NO2(g)+Cl(g)△H2k2=8.8×1012mL•(mol•s)-1
脱硫:
c.SO2(g)+ClO2(g)=SO3(g)+ClO(g)△H3k3=2.1×10-4mL•(mol•s)-1
d.SO2(g)+ClO(g)=SO2(g)+Cl(g)△H4k4=6.9×1011mL•(mol•s)-1
①已知反应c、d的速率方程分别为v正=k3c(SO2)•c(ClO2)、v正=k4c(SO2)•c(ClO),试判断两反应的活化能大小:E3
②SO2、NO单独氧化及同时氧化对两气体氧化率变化如图,同时氧化对

您最近一年使用:0次
【推荐3】(1)如图的氮循环是生态系统物质循环的重要部分,人类活动加剧了氮循环中的物质转化。
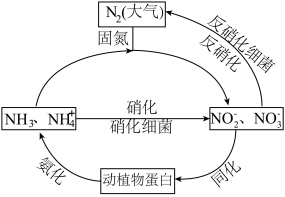
①下列说法正确的是_______ (填字母序号)
A.固氮过程中,N2只做氧化剂
B.硝化过程需要有氧化剂参与
C.反硝化过程有助于弥补人工固氮对氮循环造成的影响
D.同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化
②反硝化过程中,CH3OH可作为反应的还原剂,1mol还原剂失去6mol电子。请将该反应的离子方程式补充完整:5CH3OH+□NO3— □_______+□_______+□_______+□_______,
□_______+□_______+□_______+□_______,_____________
(2)研究表明,氮氧化物(NOx)和二氧化硫都与大气中雾霾的形成有关。
①已知:SO2生成SO3总反应方程式是2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ/mol
2SO3(g)ΔH=-196.6kJ/mol
此反应可通过如下两步完成:2NO(g)+O2(g) 2NO2(g)ΔH1=-113kJ/mol
2NO2(g)ΔH1=-113kJ/mol
NO2(g)+SO2(g) SO3(g)+NO(g)ΔH2=
SO3(g)+NO(g)ΔH2=_______ 。
②一定温度下,向2L恒容密闭容器中充入NO2和SO2各1mol,5min达到平衡,此时容器中NO2和NO的浓度之比为1∶3,则NO2的平衡转化率是_______ 。
(3)砷(As)是第四周期ⅤA族元素,其化合物,有着广泛的用途。
①AsH3的稳定性比NH3的稳定性_______ (填“强’’或“弱’’)。用原子结构解释原因_______ 。
②常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式_______ 。
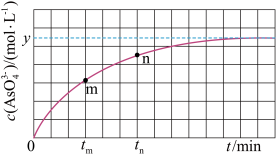
③298K时,将20mL3xmol•L-1Na3AsO3、20mL3xmol•L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH- AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43﹣)与反应时间(t)的关系如图所示。若平衡时溶液的pH=14,则该反应的平衡常数K为
AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43﹣)与反应时间(t)的关系如图所示。若平衡时溶液的pH=14,则该反应的平衡常数K为_______ 。

①下列说法正确的是
A.固氮过程中,N2只做氧化剂
B.硝化过程需要有氧化剂参与
C.反硝化过程有助于弥补人工固氮对氮循环造成的影响
D.同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化
②反硝化过程中,CH3OH可作为反应的还原剂,1mol还原剂失去6mol电子。请将该反应的离子方程式补充完整:5CH3OH+□NO3—
 □_______+□_______+□_______+□_______,
□_______+□_______+□_______+□_______,(2)研究表明,氮氧化物(NOx)和二氧化硫都与大气中雾霾的形成有关。
①已知:SO2生成SO3总反应方程式是2SO2(g)+O2(g)
 2SO3(g)ΔH=-196.6kJ/mol
2SO3(g)ΔH=-196.6kJ/mol此反应可通过如下两步完成:2NO(g)+O2(g)
 2NO2(g)ΔH1=-113kJ/mol
2NO2(g)ΔH1=-113kJ/molNO2(g)+SO2(g)
 SO3(g)+NO(g)ΔH2=
SO3(g)+NO(g)ΔH2=②一定温度下,向2L恒容密闭容器中充入NO2和SO2各1mol,5min达到平衡,此时容器中NO2和NO的浓度之比为1∶3,则NO2的平衡转化率是
(3)砷(As)是第四周期ⅤA族元素,其化合物,有着广泛的用途。
①AsH3的稳定性比NH3的稳定性
②常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式
③298K时,将20mL3xmol•L-1Na3AsO3、20mL3xmol•L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-
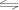 AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43﹣)与反应时间(t)的关系如图所示。若平衡时溶液的pH=14,则该反应的平衡常数K为
AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43﹣)与反应时间(t)的关系如图所示。若平衡时溶液的pH=14,则该反应的平衡常数K为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)上述反应是不是可逆反应_______ (填“是”或“不是”);在3s时NO的转化率为_______ 。
(2)如图中表示NO2的变化的曲线是_______ 。用O2表示从0~5 s内该反应的平均速率v=_______ 。

(3)能说明该反应已达到平衡状态的是_______。
(4)能使该反应的反应速率增大的是_______。
(5)在一个6L的密闭容器中放入3mol X和2molY,在一定条件下发生反应4X(g)+3Y(g)  2Q(g)+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小
2Q(g)+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小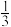 ,则该反应方程式中的n值是
,则该反应方程式中的n值是_______ 。
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.20 | 0.1 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)上述反应是不是可逆反应
(2)如图中表示NO2的变化的曲线是

(3)能说明该反应已达到平衡状态的是_______。
| A.v(NO2)=2v(O2) | B.2v逆(NO)=v正(O2) |
| C.容器内压强保持不变 | D.容器内密度保持不变 |
| A.及时分离出NO2气体 | B.适当升高温度 |
| C.降低O2的浓度 | D.选择高效催化剂 |
 2Q(g)+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小
2Q(g)+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小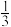 ,则该反应方程式中的n值是
,则该反应方程式中的n值是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
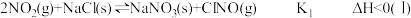
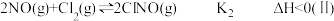
(1) 平衡常数K=
平衡常数K=___________ (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应(Ⅱ)达到平衡,测得10min内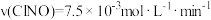 。则平衡后n(Cl2)=
。则平衡后n(Cl2)=___________ mol,NO的转化率α1=___________ 。
(3)其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2___________ α1 (填“>”“<”或“=”),平衡常数K2___________ (填“增大”“减小”或“不变”)。
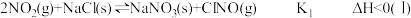
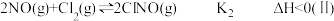
(1)
 平衡常数K=
平衡常数K=(2)为研究不同条件对反应(Ⅱ)的影响在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应(Ⅱ)达到平衡,测得10min内
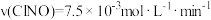 。则平衡后n(Cl2)=
。则平衡后n(Cl2)=(3)其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2
您最近一年使用:0次
【推荐3】氮的氧化物在生产、生活中有广泛应用。
Ⅰ.已知汽车气缸中氮及其化合物发生如下反应:
 (常温下平衡常数为K1)
(常温下平衡常数为K1)
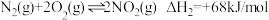 (常温下平衡常数为K2)
(常温下平衡常数为K2)
(1)则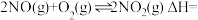
_______  ;常温下平衡常数K=
;常温下平衡常数K=_______ (用K1、K2来表示)
Ⅱ.四氧化二氮(N2O4)可作为运载火箭的推进剂,将4 mol N2O4放入2 L恒容密闭容器中发生反应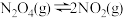 ,平衡体系中N2O4的体积分数(
,平衡体系中N2O4的体积分数( )随温度的变化如图所示:
)随温度的变化如图所示:
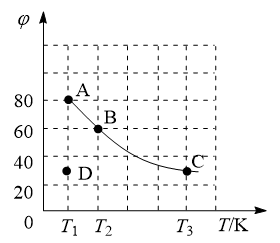
(2)D点v(正)_______ v(逆)(填“>”“=”或“<”)。
(3)A、B、C点中平衡常数K的值最大的是_______ 点。T2时,N2O4的平衡转化率为_______ ;若达平衡时间为5 s,则此时间内的N2O4平均反应速率为_______ 。
(4)若其条件不变,在 原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数
原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数_______ (填“增大”“不变”或“减小”)。
Ⅲ.碳的很多化合物在生产、生活中有广泛应用,对其进行综合利用是目前研究的热点之一。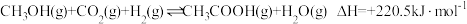 ;中科院化学所研究了该反应的反应历程,如图所示:
;中科院化学所研究了该反应的反应历程,如图所示:
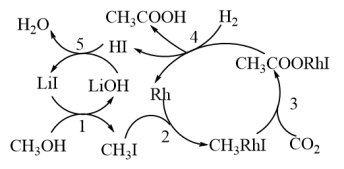
(5)反应历程中,能降低反应活化能的物质有_______ (填化学式);中间产物有_______ 种。
(6)第4步反应的化学方程式为_______ 。
Ⅰ.已知汽车气缸中氮及其化合物发生如下反应:
 (常温下平衡常数为K1)
(常温下平衡常数为K1)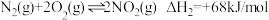 (常温下平衡常数为K2)
(常温下平衡常数为K2)(1)则
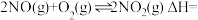
 ;常温下平衡常数K=
;常温下平衡常数K=Ⅱ.四氧化二氮(N2O4)可作为运载火箭的推进剂,将4 mol N2O4放入2 L恒容密闭容器中发生反应
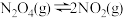 ,平衡体系中N2O4的体积分数(
,平衡体系中N2O4的体积分数( )随温度的变化如图所示:
)随温度的变化如图所示:
(2)D点v(正)
(3)A、B、C点中平衡常数K的值最大的是
(4)若其条件不变,在
 原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数
原平衡基础上,再加入一定量NO2,达到新平衡时,与原平衡相比,NO2的体积分数Ⅲ.碳的很多化合物在生产、生活中有广泛应用,对其进行综合利用是目前研究的热点之一。
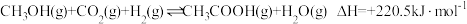 ;中科院化学所研究了该反应的反应历程,如图所示:
;中科院化学所研究了该反应的反应历程,如图所示:
(5)反应历程中,能降低反应活化能的物质有
(6)第4步反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)汽车尾气里含有的 NO 气体是由内燃机燃烧造成高温而引起氮气和氧气反应所产生的:N2(g)+O2(g) 2NO(g) ΔH>0,请回答:
2NO(g) ΔH>0,请回答:
①某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5 min后O2的物质的量为0.5 mol,则N2的反应速率为___________ 。
②假定该反应在恒容条件下进行,判断该反应达到平衡的标志是___________ 。
A.消耗 1 mol N2的同时生成 1 mol O2 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.2v正(N2)=v逆(NO)
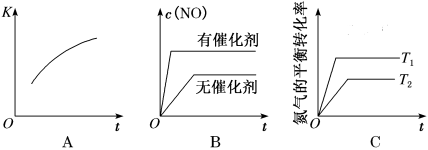
③将N2、O2的混合气体充入恒温恒容密闭容器中,如图中变化趋势正确的是___________ (填字母)。
(2)NH 硝化过程发生反应2NH
硝化过程发生反应2NH +3O2
+3O2 2HNO3+2H2O+2H+,恒温时在亚硝酸菌的作用下发生该反应。
2HNO3+2H2O+2H+,恒温时在亚硝酸菌的作用下发生该反应。
①实验测得在其它条件一定时,NH 硝化反应的速率随温度变化曲线如下图A所示,温度高于35℃时反应速率迅速下降的原因可能是
硝化反应的速率随温度变化曲线如下图A所示,温度高于35℃时反应速率迅速下降的原因可能是___________ 。

②亚硝酸盐含量过高对人和动植物都会造成一定的危害,因此要对亚硝酸盐含量过高的废水进行处理。处理方法之一是用NaClO将亚硝酸盐氧化为硝酸盐,其反应为ClO-+NO =NO
=NO +Cl-。25 ℃和35 ℃下,分别向NO
+Cl-。25 ℃和35 ℃下,分别向NO 初始浓度为5×10-3 mol/L的溶液中按不同的投料比
初始浓度为5×10-3 mol/L的溶液中按不同的投料比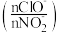 加入次氯酸钠固体(忽略溶液体积的变化),平衡时NO
加入次氯酸钠固体(忽略溶液体积的变化),平衡时NO 的去除率和温度、投料比的关系如上图B所示,a、b、c、d四点ClO-的转化率由小到大的顺序是
的去除率和温度、投料比的关系如上图B所示,a、b、c、d四点ClO-的转化率由小到大的顺序是___________ ,35 ℃时该反应的平衡常数K=___________
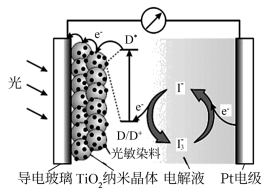
(3)下图是一种染料敏化太阳能电池示意图,电池的一个电极由吸附光敏染料(D)的TiO2,纳米晶体涂敷在导电玻璃上构成,另一电极由Pt-导电玻璃构成,工作原理为:
i.TiO2/D TiO2/D*(激发态)
TiO2/D*(激发态)
ii.TiO2/D*→TiO2/D+ + e-
iii.还原剂A+D+→D+氧化产物B
iv.还原剂A再生
回答下列问题:
①Pt电极是该电池的___________ 极(填“正”或“负”)。
②结合图示写出iii反应的离子方程式(其中染料分子用D表示)___________ 。
③电池工作过程中,导带中的e-会与D+发生复合,该反应的速率为vˊ,步骤iii的速率为v,若该电池持续稳定工作,则v___________ vˊ(填“>”或“<”)。
④导电玻璃材料的选择非常重要,你认为该材料应具备哪些性能(回答一条即可)___________ 。
(1)汽车尾气里含有的 NO 气体是由内燃机燃烧造成高温而引起氮气和氧气反应所产生的:N2(g)+O2(g)
 2NO(g) ΔH>0,请回答:
2NO(g) ΔH>0,请回答:①某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5 min后O2的物质的量为0.5 mol,则N2的反应速率为
②假定该反应在恒容条件下进行,判断该反应达到平衡的标志是
A.消耗 1 mol N2的同时生成 1 mol O2 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.2v正(N2)=v逆(NO)
③将N2、O2的混合气体充入恒温恒容密闭容器中,如图中变化趋势正确的是

(2)NH
 硝化过程发生反应2NH
硝化过程发生反应2NH +3O2
+3O2 2HNO3+2H2O+2H+,恒温时在亚硝酸菌的作用下发生该反应。
2HNO3+2H2O+2H+,恒温时在亚硝酸菌的作用下发生该反应。①实验测得在其它条件一定时,NH
 硝化反应的速率随温度变化曲线如下图A所示,温度高于35℃时反应速率迅速下降的原因可能是
硝化反应的速率随温度变化曲线如下图A所示,温度高于35℃时反应速率迅速下降的原因可能是
②亚硝酸盐含量过高对人和动植物都会造成一定的危害,因此要对亚硝酸盐含量过高的废水进行处理。处理方法之一是用NaClO将亚硝酸盐氧化为硝酸盐,其反应为ClO-+NO
 =NO
=NO +Cl-。25 ℃和35 ℃下,分别向NO
+Cl-。25 ℃和35 ℃下,分别向NO 初始浓度为5×10-3 mol/L的溶液中按不同的投料比
初始浓度为5×10-3 mol/L的溶液中按不同的投料比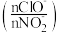 加入次氯酸钠固体(忽略溶液体积的变化),平衡时NO
加入次氯酸钠固体(忽略溶液体积的变化),平衡时NO 的去除率和温度、投料比的关系如上图B所示,a、b、c、d四点ClO-的转化率由小到大的顺序是
的去除率和温度、投料比的关系如上图B所示,a、b、c、d四点ClO-的转化率由小到大的顺序是(3)下图是一种染料敏化太阳能电池示意图,电池的一个电极由吸附光敏染料(D)的TiO2,纳米晶体涂敷在导电玻璃上构成,另一电极由Pt-导电玻璃构成,工作原理为:

i.TiO2/D
 TiO2/D*(激发态)
TiO2/D*(激发态)ii.TiO2/D*→TiO2/D+ + e-
iii.还原剂A+D+→D+氧化产物B
iv.还原剂A再生
回答下列问题:
①Pt电极是该电池的
②结合图示写出iii反应的离子方程式(其中染料分子用D表示)
③电池工作过程中,导带中的e-会与D+发生复合,该反应的速率为vˊ,步骤iii的速率为v,若该电池持续稳定工作,则v
④导电玻璃材料的选择非常重要,你认为该材料应具备哪些性能(回答一条即可)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】NOx、SO2是常用的化工原料,含NOx、SO2的烟气大量排放能造成严重的大气污染。
(1)含NH3、NOx、SO2的烟气在大气中相互作用,产生的雾霾颗粒中有多种无机盐,其中无机铵盐主要是_____________ (填化学式,只写两种)。
(2)SO2催化氧化反应2SO2(g)+O2(g)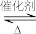 2SO3(g)的能量与反应进程如图所示:
2SO3(g)的能量与反应进程如图所示:

①该反应的正反应为____ 热(填“放”或“吸”)反应。
②若该反应在恒温恒容密闭容器中进行,能说明该 反应已达到化学平衡状态的是____ (填标号)。
A.SO2的v(正)=v(逆)
B.混合气体中同时存在SO2、O2、SO3
C.容器内混合气体密度不随时间而变化
D.容器内混合气体总压强不再随时间而变化
(3)Wang c H等研究发现用Fe2O3/CeO2作催化剂,可用乙烯脱除烟气中SO2并回收单质硫。反应原理为:CH2=CH2+3SO2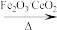 3S+2CO2+2H2O。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:
3S+2CO2+2H2O。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:

①实验中所需SO2可由Cu与浓硫酸反应制取,该反应的化学方程式为________ 。
②已知:酸性KMnO4可将CH2=CH2氧化为CO2;装置Ⅱ、Ⅲ中试剂均足量;装置(Ⅰ)的尾气中还含有未反应的SO2和CH2=CH2。检验CO2时,Ⅱ、Ⅲ、Ⅳ中盛放的试剂依次可以是_____ (填标号)。
A.酸性KMnO4溶液、品红溶液、澄清石灰水
B.NaOH溶液、酸性KMnO4溶液、澄清石灰水
C.Br2的H2O溶液、品红溶液、澄清石灰水
D.Br2的CCl4溶液、酸性KMnO4溶液、澄清石灰水
(4)取用氨水脱除烟气中SO2得到的副产品[只含(NH4)2SO4和NH4HSO4] 3.875g,与足量NaOH混合后加热充分反应,共收集到氨气1.232L(已折合为标准状况),则该副产品中(NH4)2SO4和NH4HSO4的物质的量之比n[(NH4)2SO4]∶n(NH4HSO4)=______ (写出计算结果即可)。
(1)含NH3、NOx、SO2的烟气在大气中相互作用,产生的雾霾颗粒中有多种无机盐,其中无机铵盐主要是
(2)SO2催化氧化反应2SO2(g)+O2(g)
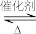 2SO3(g)的能量与反应进程如图所示:
2SO3(g)的能量与反应进程如图所示:
①该反应的正反应为
②若该反应在恒温恒容密闭容器中进行,能说明该 反应已达到化学平衡状态的是
A.SO2的v(正)=v(逆)
B.混合气体中同时存在SO2、O2、SO3
C.容器内混合气体密度不随时间而变化
D.容器内混合气体总压强不再随时间而变化
(3)Wang c H等研究发现用Fe2O3/CeO2作催化剂,可用乙烯脱除烟气中SO2并回收单质硫。反应原理为:CH2=CH2+3SO2
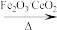 3S+2CO2+2H2O。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:
3S+2CO2+2H2O。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:
①实验中所需SO2可由Cu与浓硫酸反应制取,该反应的化学方程式为
②已知:酸性KMnO4可将CH2=CH2氧化为CO2;装置Ⅱ、Ⅲ中试剂均足量;装置(Ⅰ)的尾气中还含有未反应的SO2和CH2=CH2。检验CO2时,Ⅱ、Ⅲ、Ⅳ中盛放的试剂依次可以是
A.酸性KMnO4溶液、品红溶液、澄清石灰水
B.NaOH溶液、酸性KMnO4溶液、澄清石灰水
C.Br2的H2O溶液、品红溶液、澄清石灰水
D.Br2的CCl4溶液、酸性KMnO4溶液、澄清石灰水
(4)取用氨水脱除烟气中SO2得到的副产品[只含(NH4)2SO4和NH4HSO4] 3.875g,与足量NaOH混合后加热充分反应,共收集到氨气1.232L(已折合为标准状况),则该副产品中(NH4)2SO4和NH4HSO4的物质的量之比n[(NH4)2SO4]∶n(NH4HSO4)=
您最近一年使用:0次
【推荐3】近年来,我国化工技术获得重大突破,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇(CH3OH)是其中的一个研究项目。该研究发生的主要反应如下:
Ⅰ.CO与H2反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
Ⅱ.CO2与H2反应合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)上述反应符合原子经济性的是反应_______ (I或II)。
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是_______ 。
a.恒温恒容下,再充入CO b.升高温度
c.恒温恒容下,向其中充入Ar d.恒温恒压下,向其中充入Ar
(3)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是_______ 。
a.单位时间内消耗3molH2,同时生成1mol的CH3OH
b.CH3OH的体积分数不再发生变化
c.3v(CO2)=v(H2)
d.容器内气体密度不再改变
(4)H2还原CO电化学法制备甲醇(CO + 2H2 = CH3OH)的工作原理如图所示:
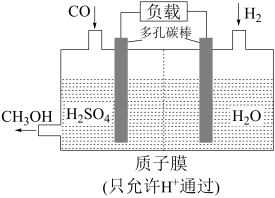
通入H2的一端是电池的_______ 极(填“正”或“负”),电池工作过程中H+通过质子膜向_______ (填“左”或者“右”)移动,通入CO的一端发生_______ (填“氧化”或者 “还原”)反应。
Ⅰ.CO与H2反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)Ⅱ.CO2与H2反应合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)(1)上述反应符合原子经济性的是反应
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是
a.恒温恒容下,再充入CO b.升高温度
c.恒温恒容下,向其中充入Ar d.恒温恒压下,向其中充入Ar
(3)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是
a.单位时间内消耗3molH2,同时生成1mol的CH3OH
b.CH3OH的体积分数不再发生变化
c.3v(CO2)=v(H2)
d.容器内气体密度不再改变
(4)H2还原CO电化学法制备甲醇(CO + 2H2 = CH3OH)的工作原理如图所示:

通入H2的一端是电池的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】我国含煤量和煤使用量均为全球第一,所以如何提高煤的使用效率,同时减少对环境的危害一直是我国科学家研究的重要课题。其中重要的汽化反应为:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ/mol;2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,则反应CO和水蒸气反应生成CO2和H2的热化学方程式:_______ 。
(2)为提高该汽化反应的CO转化率,可采用的方法有_______(填编号)。
(3)在3L密闭容器中,将4.0 mol CO与8.0 mol H2O混合迅速加热到600℃,在600℃时跟踪测定CO的物质的量变化如图所示:
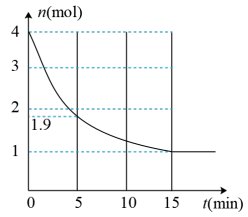
①该体系在第_______ min时达到化学平衡,从反应开始到5 min时,用CO2表示的反应速率为_______ ,600℃的平衡常数为_______ 。
②保持温度不变,15 min后向该密闭容器中再次充入3 mol CO、1 mol H2O(g)、1 mol CO2(g)、1 mol H2(g),此时平衡_______ (填“正移”、“不移”或“逆移”),其原因是_______ 。
 CO2(g)+H2(g)
CO2(g)+H2(g)(1)已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ/mol;2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,则反应CO和水蒸气反应生成CO2和H2的热化学方程式:
(2)为提高该汽化反应的CO转化率,可采用的方法有_______(填编号)。
| A.选择适当的催化剂 | B.增大压强 |
| C.升高温度 | D.及时分离出CO2 |
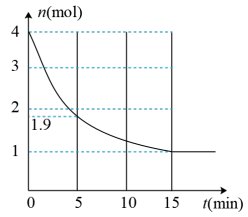
①该体系在第
②保持温度不变,15 min后向该密闭容器中再次充入3 mol CO、1 mol H2O(g)、1 mol CO2(g)、1 mol H2(g),此时平衡
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.金属冶炼与处理中常涉及离子反应和氧化还原反应。
(1)实验室常用无水乙醇处理少量残留的金属钠,写出反应的化学方程式_________ 。
(2)镁与碳在加强热时可生成易水解的MgC2,其水解的化学方程式为________ 。
(3)我国古代劳动人民曾利用明矾溶液除去铜器表面的铜锈[Cu2(OH)2CO3],请简要解释其原理:_______ 。
Ⅱ.(4)0.1 mol·L-1NaHCO3溶液与0.1 mol·L-1NaOH溶液等体积混合,所得溶液中离子浓度由大到小的顺序是:______________ 。
(5)恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)。下列描述能说明该反应达到平衡状态的是
CH3OH(g)+H2O(g)。下列描述能说明该反应达到平衡状态的是_____ (填序号)。
A 容器内的混合气体的平均相对分子质量保持不变
B 水分子中断裂2NA个H-O键,同时氢分子中生成3NA个H-H键
C CH3OH和H2O的浓度保持不变
D 容器内的混合气体的密度保持不变
(6)现有反应CH3OCH3(g)+H2O(g) 2CH3OH(g) △H=+23.4 kJ/mol,在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到10min时测得各组分浓度如下:
2CH3OH(g) △H=+23.4 kJ/mol,在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到10min时测得各组分浓度如下:
此时v正_______ v逆(填“>”、“<”或“=”),v (CH3OH) =_______ ;当反应达到平衡状态时,混合气体中CH3OCH3体积分数(CH3OCH3)%=______ %。
(1)实验室常用无水乙醇处理少量残留的金属钠,写出反应的化学方程式
(2)镁与碳在加强热时可生成易水解的MgC2,其水解的化学方程式为
(3)我国古代劳动人民曾利用明矾溶液除去铜器表面的铜锈[Cu2(OH)2CO3],请简要解释其原理:
Ⅱ.(4)0.1 mol·L-1NaHCO3溶液与0.1 mol·L-1NaOH溶液等体积混合,所得溶液中离子浓度由大到小的顺序是:
(5)恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。下列描述能说明该反应达到平衡状态的是
CH3OH(g)+H2O(g)。下列描述能说明该反应达到平衡状态的是A 容器内的混合气体的平均相对分子质量保持不变
B 水分子中断裂2NA个H-O键,同时氢分子中生成3NA个H-H键
C CH3OH和H2O的浓度保持不变
D 容器内的混合气体的密度保持不变
(6)现有反应CH3OCH3(g)+H2O(g)
 2CH3OH(g) △H=+23.4 kJ/mol,在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到10min时测得各组分浓度如下:
2CH3OH(g) △H=+23.4 kJ/mol,在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到10min时测得各组分浓度如下:| 物质 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
| 浓度/mol·L-1 | 0.9 | 0.9 | 1.2 |
此时v正
您最近一年使用:0次
【推荐3】我国在西昌卫星发射“长征三号甲”是三级液体助推火箭,一、二级为常规燃料,常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。
I.有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大。
(1)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-543 kJ·mol-1
H2(g)+F2(g)=2HF(g) ΔH2=-538 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH3=-484 kJ·mol-1
则:N2H4(g)+2F2(g)=N2(g)+4HF(g) ΔH4=______ 。
II.氧化剂二氧化氮可由NO和O2生成。800°C时,在2 L密闭容器内,0.200 mol NO与0.100 mol O2反应:2NO(g)+O2(g) 2NO2(g) ΔH的体系中,已知n(NO)随时间的变化如图所示:
2NO2(g) ΔH的体系中,已知n(NO)随时间的变化如图所示:
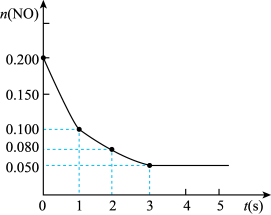
(2)已知:K(800℃)>K(1000℃),则该反应的ΔH______ 0(填“>”或“<”),用NO2表示从0~2 s内该反应的平均速率v(NO2)=______ 。
(3)能说明该反应已达到平衡状态的是______ 。
a.容器内颜色保持不变 b.2v逆(NO)=v正(O2)
c.容器内压强保持不变 d.容器内密度保持不变
(4)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有______ (任写一条)。
I.有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大。
(1)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-543 kJ·mol-1
H2(g)+F2(g)=2HF(g) ΔH2=-538 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH3=-484 kJ·mol-1
则:N2H4(g)+2F2(g)=N2(g)+4HF(g) ΔH4=
II.氧化剂二氧化氮可由NO和O2生成。800°C时,在2 L密闭容器内,0.200 mol NO与0.100 mol O2反应:2NO(g)+O2(g)
 2NO2(g) ΔH的体系中,已知n(NO)随时间的变化如图所示:
2NO2(g) ΔH的体系中,已知n(NO)随时间的变化如图所示:
(2)已知:K(800℃)>K(1000℃),则该反应的ΔH
(3)能说明该反应已达到平衡状态的是
a.容器内颜色保持不变 b.2v逆(NO)=v正(O2)
c.容器内压强保持不变 d.容器内密度保持不变
(4)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有
您最近一年使用:0次



