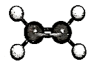
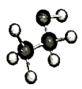
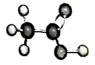
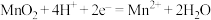设NA代表阿伏加德罗常数的值。下列说法正确的是
| A.25℃,1LpH=12的NaOH溶液中含有OH-的数目为0.02NA |
| B.在碱性锌锰电池中,消耗6.5g纯锌转移电子数为0.1NA |
| C.46g有机物C2H6O中含有极性共价键的数目一定为7NA |
| D.标准状况下22.4LCl2完全溶于水时,所得溶液中含氯微粒总数小于2NA |
更新时间:2023-06-10 22:55:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】二元酸H2A在水中的电离方程式为:H2A=H++HA-,HA-  H++A2-。25°C时,向20.00mL 0.1mol/L H2A溶液中加入NaOH溶液,pOH水与所加NaOH溶液体积的关系如图所示。已知:pOH水表示溶液中由水电离出的c水(OH- )的负对数[-lgc水(OH-)]。下列说法中不正确的是(忽略过程中溶液的体积变化)
H++A2-。25°C时,向20.00mL 0.1mol/L H2A溶液中加入NaOH溶液,pOH水与所加NaOH溶液体积的关系如图所示。已知:pOH水表示溶液中由水电离出的c水(OH- )的负对数[-lgc水(OH-)]。下列说法中不正确的是(忽略过程中溶液的体积变化)

 H++A2-。25°C时,向20.00mL 0.1mol/L H2A溶液中加入NaOH溶液,pOH水与所加NaOH溶液体积的关系如图所示。已知:pOH水表示溶液中由水电离出的c水(OH- )的负对数[-lgc水(OH-)]。下列说法中不正确的是(忽略过程中溶液的体积变化)
H++A2-。25°C时,向20.00mL 0.1mol/L H2A溶液中加入NaOH溶液,pOH水与所加NaOH溶液体积的关系如图所示。已知:pOH水表示溶液中由水电离出的c水(OH- )的负对数[-lgc水(OH-)]。下列说法中不正确的是(忽略过程中溶液的体积变化)
| A.A点溶液,c(H+ )=1 × 10-0.9 mol/L |
| B.B点溶液呈酸性,原因是NaHA电离程度比水解程度大 |
C.C点至D点变化过程中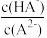 逐渐减小 逐渐减小 |
| D.D点溶液中:c(Na+)+c(HA-)+c(A2-)=0.1mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列溶液中的微粒浓度关系正确的是
A.0.1 mol·L-1 Na2CO3溶液与0.1 mol·L-1 NaHCO3溶液等体积混合: c(Na+)=c( c(Na+)=c( )+c( )+c( )+c(H2CO3) )+c(H2CO3) |
B.将pH=2的盐酸与pH=12的氨水等体积混合c(Cl-)=c( )>c(OH-)=c(H+) )>c(OH-)=c(H+) |
C.CH3COOH与CH3COONa混合溶液 : :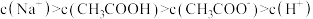 |
D.pH=4.8的NaHC2O4溶液:c(Na+)>c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含CH3CHO溶液为例),可获得电能,同时可实现海水淡化。下列说法正确的是( )
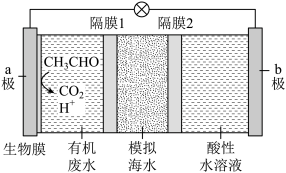

| A.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜 |
| B.a极发生反应为CH3CHO+3H2O-10e-=2CO2↑+10H+ |
| C.每处理1molCH3CHO时,模拟海水理论上除盐58.5g |
| D.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】如图所示的微生物燃料电池是一种可以利用硫酸盐还原菌作为催化剂,以废弃可降解有机物为燃料,将废弃可降解有机物的化学能转化为电能的装置。下列有关说法错误的是
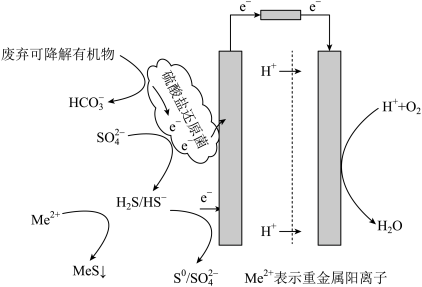

A.负极反应之一为H2S +4H2O-8e-=SO +10H+ +10H+ |
| B.正极消耗11.2LO2(标准状况),负极被氧化的H2S和HS-共0.25mol |
| C.废弃可降解有机物不同,电池电压也会不同 |
| D.该电池可以去除水体中的重金属离子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.1mol乙酸分子中含有的碳氢键数为4 |
B.1mol乙醇完全燃烧转移的电子数为6 |
C.标准状况下,11.2L  和22.4L 和22.4L  在光照下充分反应后的分子数为1.5 在光照下充分反应后的分子数为1.5 |
D.标准状况下,11.2L一氯甲烷和乙醛混合物中含氢原子数目为2 |
您最近一年使用:0次
【推荐2】诱虫烯可用芥酸和羧酸X (物质的量之比为1: 1)在浓NaOH中利用直流电源和惰性电极电解制备,芥酸和诱虫烯的结构简式如图所示。下列说法不正确的是
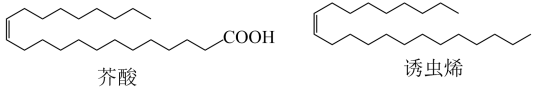
已知: Kolbe反应是游离基反应,阳极反应为RCH2COO--e-→RCH2COO· ; RCH2COO·→ RCH2· +CO2↑; 2RCH2·→RCH2—CH2R。
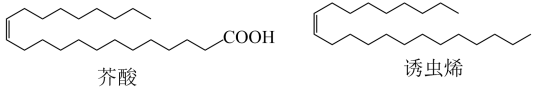
已知: Kolbe反应是游离基反应,阳极反应为RCH2COO--e-→RCH2COO· ; RCH2COO·→ RCH2· +CO2↑; 2RCH2·→RCH2—CH2R。
| A.羧酸X是乙酸 |
| B.芥酸和羧酸X都在阳极放电,发生氧化反应 |
| C.每转移1mol电子,阴极产生11.2L (标准状况下) H2 |
| D.利用Kolbe反应原理,可以获得烷烃,但不能获得环烷烃 |
您最近一年使用:0次


 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 与
与 值、微粒分布分数
值、微粒分布分数 ,X表示
,X表示 或
或 ]的关系如图所示,下列说法正确的是
]的关系如图所示,下列说法正确的是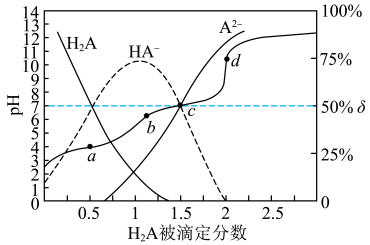

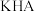 溶液可以用酚酞作指示剂
溶液可以用酚酞作指示剂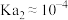
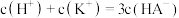

 放在一个由滤纸制成的通道内,形成了电池,该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量,下列说法错误的是
放在一个由滤纸制成的通道内,形成了电池,该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量,下列说法错误的是