下列类比或推理合理的是
已知 | 类比或推理 | |
A | 沸点:Cl2<Br2<I2 | 沸点:HCl<HBr<HI |
B | 酸性:HClO4>HIO4 | 酸性:HCl>HI |
C | 金属性:Fe>Cu | 氧化性:Fe3+<Cu2+ |
D | Na2CO3溶液显碱性 | 所有钠盐溶液均显碱性 |
| A.A | B.B | C.C | D.D |
更新时间:2023-05-15 15:18:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
A.常温下, 为2的某酸 为2的某酸 与 与 为12的某碱 为12的某碱 等体积混合,溶液呈酸性,则 等体积混合,溶液呈酸性,则 为弱酸, 为弱酸, 为强碱 为强碱 |
B.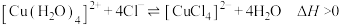 ,升高温度,平衡正向移动,溶液由蓝绿色变为黄绿色 ,升高温度,平衡正向移动,溶液由蓝绿色变为黄绿色 |
C.氨水、 溶液中分别加入适量的氯化铵晶体后,前者 溶液中分别加入适量的氯化铵晶体后,前者 增大,后者 增大,后者 减小 减小 |
D.等物质的量浓度的下列溶液中,① 、② 、② 、③ 、③ 、④ 、④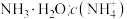 由大到小的顺序是:③>①>②>④ 由大到小的顺序是:③>①>②>④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知某温度下0.1 mol/L的NaHB(强电解质)溶液中c(H+)>c(OH-),则下列关系一定正确的是( )
| A.c(Na+)=c(HB-)+2c(B2-)+c(OH-) |
| B.c(Na+)=0.1 mol/L≥c(B2-) |
C.HB-的水解方程式为HB-+H2O B2-+H3O+ B2-+H3O+ |
| D.在该盐的溶液中,离子浓度大小顺序为c(Na+)>c(HB-)>c(B2-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温下 的稀硫酸中,含有 的稀硫酸中,含有 总数为 总数为 |
B. 溶液中,所含阴离子数目为 溶液中,所含阴离子数目为 |
C.常温下,1L0.1 mol/L的 溶液中氮原子数为 溶液中氮原子数为 |
D.一定条件下,将 和 和 充入恒容密闭容器中充分反应,生成: 充入恒容密闭容器中充分反应,生成: 的分子总数为 的分子总数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列结论正确的是
①粒子半径:S2->Cl>S ②氢化物稳定性:HF>HCl>PH3;
③单质氧化性:Cl2>S; ④酸性:H2SO4>HClO4
⑤碱性强弱:KOH>NaOH>Mg(OH)2
①粒子半径:S2->Cl>S ②氢化物稳定性:HF>HCl>PH3;
③单质氧化性:Cl2>S; ④酸性:H2SO4>HClO4
⑤碱性强弱:KOH>NaOH>Mg(OH)2
| A.① | B.①③⑤ | C.②③⑤ | D.①③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关性质的比较,不能 用元素周期律解释的是
A.非金属性: | B.热稳定性: |
C.酸性: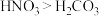 | D.金属性: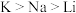 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 判断Fe(NO3)2固体是否变质 | 取少量固体溶于蒸馏水,然后滴加少量稀硫酸,再滴入KSCN溶液 | 若溶液变红,则Fe(NO3)2固体已变质 |
| B | 探究Mg与Al元素的金属性强弱 | 用pH计测同温同浓度的MgCl2和AlCl3溶液的pH | pH(MgCl2)>pH(AlCl)3则金属性:Mg>Al |
| C | 探究氢氧化铝的性质 | 将2~3mL2mol·L-1氯化铝溶液注入洁净的试管中,逐滴加入6mol·L-1氨水 | 生成白色沉淀,继续滴加,沉淀不溶解,则氢氧化铝不溶于碱 |
| D | 证明H2O2有氧化性 | 将足量的H2O2溶液滴入酸性高锰酸钾溶液中 | 若溶液中的紫红色褪去、则证明H2O2有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列根据元素周期表和元素周期律得出的推断中正确的是( )
A.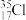 与 与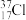 得电子能力相同 得电子能力相同 |
| B.由于HCl水溶液的酸性强于H2S水溶液的酸性,因此氯的非金属性强于硫 |
| C.Cl-、S2-、Ca2+、K+半径逐渐减小 |
| D.金属元素原子最外层电子数越少,该金属失电子能力越强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W为四种短周期非金属元素,其中X单质是一种重要的半导体材料, X、Y、Z同周期,且原子序数依次增大,Y、W同主族,离子半径Y2->W2-。
下列说法正确的是:
下列说法正确的是:
| A.X的非金属性比Y的强 |
| B.X和W组成的化合物化学性质活泼,与盐酸和氢氧化钠溶液都能反应 |
| C.Y的气态氢化物不如Z的气态氢化物稳定 |
| D.某溶液中通入Z的单质后再滴加淀粉溶液显蓝色,原溶液中一定含有I- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.含有非极性键的分子不一定是共价化合物 |
| B.分子间作用力比化学键弱得多,但它对物质的熔点、沸点有较大的影响,而对溶解度无影响 |
| C.根据π键的成键特征判断C=C键能是C﹣C键能的2倍 |
| D.H2O中心原子采取sp杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下, 是一种淡黄色的油状液体。下列对
是一种淡黄色的油状液体。下列对 的有关叙述不正确的是
的有关叙述不正确的是
 是一种淡黄色的油状液体。下列对
是一种淡黄色的油状液体。下列对 的有关叙述不正确的是
的有关叙述不正确的是A. 分子是由极性键构成的极性分子 分子是由极性键构成的极性分子 |
B. 分子的空间构型为三角锥形 分子的空间构型为三角锥形 |
C. 中的所有原子均达到8电子稳定结构 中的所有原子均达到8电子稳定结构 |
D. 的沸点比 的沸点比 的沸点低是因为 的沸点低是因为 比 比 键键能小 键键能小 |
您最近一年使用:0次





