元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分。请回答下列问题:
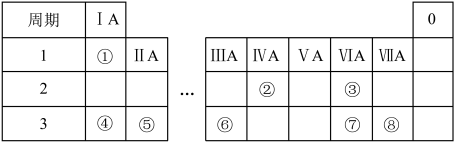
(1)画出④的原子结构示意图_____ 。
(2)①的单质在盛满⑧的单质的集气瓶中燃烧,反应现象为_____ 。
(3)③和④组成的一种物质中含有两种类型的化学键,该物质的化学式为_____ 。
(4)⑥的单质和④的最高价氧化物的水化物反应的化学方程式为_____ 。
(5)已知⑤的单质与②的最高价氧化物A在点燃条件下能反应生成黑色单质,推测④的单质_____ (填“能不能”)与A反应。
(6)为比较⑦和⑧ 非金属性,某小组同学设计实验进行探究。
非金属性,某小组同学设计实验进行探究。
【理论依据】氧化性较强的单质能置换出氧化性较弱的单质
【实验方案】
【实验过程】
按照实验方案操作,观察到的现象与预测的一致,写出该反应的化学方程式_____ 。
【实验结论】非金属性:⑦<⑧

(1)画出④的原子结构示意图
(2)①的单质在盛满⑧的单质的集气瓶中燃烧,反应现象为
(3)③和④组成的一种物质中含有两种类型的化学键,该物质的化学式为
(4)⑥的单质和④的最高价氧化物的水化物反应的化学方程式为
(5)已知⑤的单质与②的最高价氧化物A在点燃条件下能反应生成黑色单质,推测④的单质
(6)为比较⑦和⑧
 非金属性,某小组同学设计实验进行探究。
非金属性,某小组同学设计实验进行探究。【理论依据】氧化性较强的单质能置换出氧化性较弱的单质
【实验方案】
| 实验操作 | 预测现象 |
| 取Na2S溶液于试管中,滴入少量新制氯水 |
按照实验方案操作,观察到的现象与预测的一致,写出该反应的化学方程式
【实验结论】非金属性:⑦<⑧
更新时间:2023-06-07 14:05:12
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下列图示中,A、B是金属单质,E、K是非金属单质,其它为化合物,F、G、H、I、J 焰色反应均为黄色,在这些物质中只有C、K是气体,其中K是黄绿色气体,反应⑧⑨是工业由H制I的重要反应。
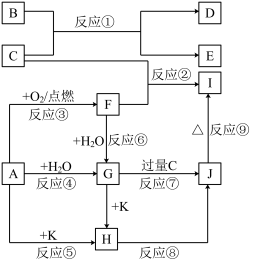
填写下列空白:
(1)写出化学式:B___ ,F___ 。
(2)写出反应①的化学反应方程式:____ 。
(3)写出反应⑦离子反应方程式:___ 。

填写下列空白:
(1)写出化学式:B
(2)写出反应①的化学反应方程式:
(3)写出反应⑦离子反应方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】含氯消毒剂是一类毒性低、价格低、杀菌效率高、被广泛使用的高效杀毒剂,在控制病原微生物污染和传播等方面右着重要作用。亚氯酸钠(NaClO2)是一种优质的漂白剂和消毒剂。一种以氯酸钠(NaClO3)为原料制备NaClO2粗品的工艺流程如图所示:
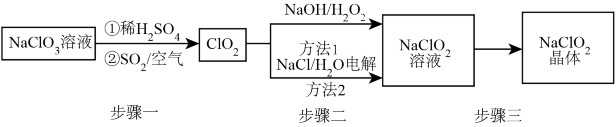
已知:①纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
②硫单质与碱在一定条件下可以反应:3S+6KOH=2K2S+K2SO3+3H2O。
(1)步骤一中通入空气的作用是____ 。
(2)方法1对所用溶液浓度要求比较精确,若需配制480mL0.5mol·L-1NaOH溶液,配制过程中所需的玻璃仪器有:烧杯、量筒、玻璃棒、____ 、____ 。
(3)方法2所用食盐水由粗盐水精制而成,精制时,为除去粗盐水中的Ca2+和SO ,按顺序加入的除杂试剂为
,按顺序加入的除杂试剂为____ 、____ 。可用NaOH溶液吸收电解产生的氯气,该反应的离子方程式是____ 。
(4)写出方法1中发生反应的化学方程式:____ ,该反应中还原剂是____ ,此方法中不宜用S代替H2O2,理由是____ 。
(5)NaClO2和 消毒时,还原产物均为Cl-。消毒剂的消毒效率可用单位质量消毒剂被还原时得电子数表示,计算NaClO2的消毒效率是Cl2的
消毒时,还原产物均为Cl-。消毒剂的消毒效率可用单位质量消毒剂被还原时得电子数表示,计算NaClO2的消毒效率是Cl2的____ 倍。(计算结果保留一位小数)

已知:①纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
②硫单质与碱在一定条件下可以反应:3S+6KOH=2K2S+K2SO3+3H2O。
(1)步骤一中通入空气的作用是
(2)方法1对所用溶液浓度要求比较精确,若需配制480mL0.5mol·L-1NaOH溶液,配制过程中所需的玻璃仪器有:烧杯、量筒、玻璃棒、
(3)方法2所用食盐水由粗盐水精制而成,精制时,为除去粗盐水中的Ca2+和SO
 ,按顺序加入的除杂试剂为
,按顺序加入的除杂试剂为(4)写出方法1中发生反应的化学方程式:
(5)NaClO2和
 消毒时,还原产物均为Cl-。消毒剂的消毒效率可用单位质量消毒剂被还原时得电子数表示,计算NaClO2的消毒效率是Cl2的
消毒时,还原产物均为Cl-。消毒剂的消毒效率可用单位质量消毒剂被还原时得电子数表示,计算NaClO2的消毒效率是Cl2的
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】84消毒液是一种常见的含氯消毒剂。如图1为某品牌84消毒液的说明书中的部分内容。

(1)84消毒液的主要成分为 _______ (用化学式表示)。
(2)常温,将氯气通入NaOH溶液中可制得84消毒液的主要成分。写出离子方程式:_______ 。
(3)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有ClO﹣、Cl﹣、HClO;相同浓度时,HClO的氧化性强于ClO﹣;ORP是反映水溶液中所有物质表现出来的氧化﹣还原性,ORP值越大,氧化性越强。
Ⅰ.将2mL84消毒液中加2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.将2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得84消毒液在不同温度时ORP随时间的变化曲线如图2。
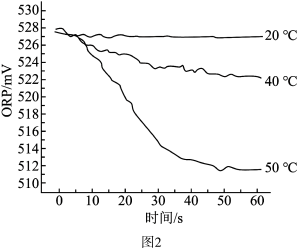
①已知白醋显酸性,不具有漂白性。实验Ⅰ、Ⅱ现象不同的原因是_______ 。
②实验表明,向84消毒液中加入较多硫酸时会产生氯气,生成氯气的离子方程式是_______ 。
③由实验Ⅲ可得出的结论是_______ 。ORP值不同的原因可能是 _______ 。

| 产品特点 本品是以次氯酸钠为主要成分的液体消毒剂。可杀灭肠道致病菌、化脓性球菌、致病性酵母菌,并能灭活病毒。 注意事项 (1)本品易使有色衣脱色,禁止用于丝、毛、麻织物的消毒。 (2)不得将本品与酸性产品(如洁厕类清洁产品)同时使用。 (3)置于避光、阴凉处保存。 (4)需稀释后使用,勿口服。 |
(2)常温,将氯气通入NaOH溶液中可制得84消毒液的主要成分。写出离子方程式:
(3)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有ClO﹣、Cl﹣、HClO;相同浓度时,HClO的氧化性强于ClO﹣;ORP是反映水溶液中所有物质表现出来的氧化﹣还原性,ORP值越大,氧化性越强。
Ⅰ.将2mL84消毒液中加2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.将2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得84消毒液在不同温度时ORP随时间的变化曲线如图2。

①已知白醋显酸性,不具有漂白性。实验Ⅰ、Ⅱ现象不同的原因是
②实验表明,向84消毒液中加入较多硫酸时会产生氯气,生成氯气的离子方程式是
③由实验Ⅲ可得出的结论是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】(1)写出下列具有10个电子的粒子的化学式:原子的原子结构示意图_____________ ,由2个原子组成的分子是_____________ 、阴离子是_____________ 。
(2)X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+4、+5、+7,核电荷数按照Y、Z、X、W的顺序增大。已知Y与Z的原子次外层的电子数均为2,W、X的原子次外层的电子数均为8。
①写出Y元素的名称_____________________ 。
②写出W元素在周期表中的位置__________________ 。
③写出X的最高价氧化物与Z的最高价氧化物对应水化物反应的化学方程式________________________ 。
④按碱性减弱、酸性增强的顺序写出各元素最高价氧化物对应水化物的分子式:_____________ ,_____________ ,_____________ ,_____________ 。
(2)X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+4、+5、+7,核电荷数按照Y、Z、X、W的顺序增大。已知Y与Z的原子次外层的电子数均为2,W、X的原子次外层的电子数均为8。
①写出Y元素的名称
②写出W元素在周期表中的位置
③写出X的最高价氧化物与Z的最高价氧化物对应水化物反应的化学方程式
④按碱性减弱、酸性增强的顺序写出各元素最高价氧化物对应水化物的分子式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。请用相关的化学术语回答下列问题:
(1) 在这些元素中,最不活泼的是 ,非金属性最强的是___________,金属性最强的是___________;(填元素符号或化学式,下同。)
(2) 这些元素形成的最高价氧化物对应的水化物中碱性最强的 ,酸性最强的__________;
(3) ①、②、③、④、⑤这五种元素的原子半径由大到小的顺序为 ;
(4) ⑥的氢化物的电子式为 ,① 在空气中燃烧后生成产物的电子式 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA[ | 0 |
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ① | ③ | ④ | ⑧ | ⑨ | |||
| 4 | ② |
(2) 这些元素形成的最高价氧化物对应的水化物中碱性最强的 ,酸性最强的__________;
(3) ①、②、③、④、⑤这五种元素的原子半径由大到小的顺序为 ;
(4) ⑥的氢化物的电子式为 ,① 在空气中燃烧后生成产物的电子式 。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】下图是周期表的一部分,回答下列问题:
(1)A的原子结构示意图是_________________ ;
(2)E在周期表的位置为_________________________ ;与E同族的下一周期元素的原子序数为___________ ;
(3)表中元素形成气态氢化物最稳定的是___________ (填化学式,下同),最高价氧化物对应水化物酸性最强的是________________ ;
(4)下列不能用来对比C和D金属性强弱的是_________
a.C单质的熔点比D低
b.C的阳离子的氧化性弱于D的阳离子的氧化性
c.C单质与水反应比D单质与水反应剧烈
d.C最高价氧化物对应水化物的碱性比D强
(5)元素A与H分别与H形成的18电子分子Q和W(常用作火箭燃料)可以发生氧化还原反应,生成H单质和A的另一种氢化物。请写出该反应的方程式:______________________ 。
| H | A | B | ||||||
| C | D | E | F | G | ||||
(2)E在周期表的位置为
(3)表中元素形成气态氢化物最稳定的是
(4)下列不能用来对比C和D金属性强弱的是
a.C单质的熔点比D低
b.C的阳离子的氧化性弱于D的阳离子的氧化性
c.C单质与水反应比D单质与水反应剧烈
d.C最高价氧化物对应水化物的碱性比D强
(5)元素A与H分别与H形成的18电子分子Q和W(常用作火箭燃料)可以发生氧化还原反应,生成H单质和A的另一种氢化物。请写出该反应的方程式:
您最近一年使用:0次
【推荐1】化合物X(仅含三种短周期元素)是一种络合氢化物的储氢材料,在400℃下隔绝空气加热分解。X中某种元素的单质常用来制作信号弹和烟火。某研究小组为了探究X的组成,设计并完成了如图实验:
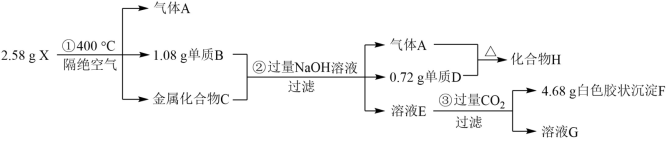
已知A为气体单质,回答下列问题:
(1)X中所含元素为___ (填写元素符号),写出化合物H的化学式___ 。
(2)写出X在400℃下隔绝空气加热分解的化学方程式___ 。
(3)写出溶液E中一种溶质与溶液G反应生成F的离子方程式___ 。
(4)设计实验比较C中两种元素的金属性强弱___ 。
(5)化合物H___ (填“能”或“不能”)与水反应生成H2,理由是___ 。

已知A为气体单质,回答下列问题:
(1)X中所含元素为
(2)写出X在400℃下隔绝空气加热分解的化学方程式
(3)写出溶液E中一种溶质与溶液G反应生成F的离子方程式
(4)设计实验比较C中两种元素的金属性强弱
(5)化合物H
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)写出下列具有10个电子的粒子的化学式:原子的原子结构示意图_____________ ,由2个原子组成的分子是_____________ 、阴离子是_____________ 。
(2)X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+4、+5、+7,核电荷数按照Y、Z、X、W的顺序增大。已知Y与Z的原子次外层的电子数均为2,W、X的原子次外层的电子数均为8。
①写出Y元素的名称_____________________ 。
②写出W元素在周期表中的位置__________________ 。
③写出X的最高价氧化物与Z的最高价氧化物对应水化物反应的化学方程式________________________ 。
④按碱性减弱、酸性增强的顺序写出各元素最高价氧化物对应水化物的分子式:_____________ ,_____________ ,_____________ ,_____________ 。
(2)X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+4、+5、+7,核电荷数按照Y、Z、X、W的顺序增大。已知Y与Z的原子次外层的电子数均为2,W、X的原子次外层的电子数均为8。
①写出Y元素的名称
②写出W元素在周期表中的位置
③写出X的最高价氧化物与Z的最高价氧化物对应水化物反应的化学方程式
④按碱性减弱、酸性增强的顺序写出各元素最高价氧化物对应水化物的分子式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】第五代隐身战机运用了先进的吸波材料。钡铁氧体是一种应用最广的吸波材料之一。回答下列问题:
(1)铝与钡处于相邻主族,铝的原子核外有_______ 种能量不同的电子。氢氧化铝可以溶于氢氧化钡得到无色溶液,写出离子方程式_______ 。
(2)钡的金属性_______ (大于或小于)铝,下列能比较铝与钡的金属性强弱的是_______ 。
a.高温下铝冶炼钡4BaO+2Al→BaO·Al2O3+3Ba↑
b.铝与水反应需加热,钡与水剧烈反应
c.氧化铝熔点高于氧化钡
(3)某钡铁氧体化学式为BaFe18O27,将其写为氧化物的形式_______ 。将0.030mol该铁氧体溶于2.0mol/L的稀硝酸,恰好溶解时需要硝酸_______ mL。
(4)碳酸钡可用于制钡铁氧体,一种制纳米碳酸钡的原料为BaCl2、NH4HCO3和氨水,从电离平衡的角度分析氨水的作用_______ 。
(5)实验室中,氧化钡是一种高效干燥剂,可以除去乙醚等有机试剂中的少量水,但不能用于除乙酸乙酯中的少量水,原因是_______ 。
(1)铝与钡处于相邻主族,铝的原子核外有
(2)钡的金属性
a.高温下铝冶炼钡4BaO+2Al→BaO·Al2O3+3Ba↑
b.铝与水反应需加热,钡与水剧烈反应
c.氧化铝熔点高于氧化钡
(3)某钡铁氧体化学式为BaFe18O27,将其写为氧化物的形式
(4)碳酸钡可用于制钡铁氧体,一种制纳米碳酸钡的原料为BaCl2、NH4HCO3和氨水,从电离平衡的角度分析氨水的作用
(5)实验室中,氧化钡是一种高效干燥剂,可以除去乙醚等有机试剂中的少量水,但不能用于除乙酸乙酯中的少量水,原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】现有六种短周期元素A、B、C、D、E、F,其原子序数依次增大,其中B与C、D与F分别位于同一周期,A与D、C与F分别位于同一主族,且A、D两元素原子的质子数之和是C、F两元素原子质子数之和的一半。又知六种元素所形成的常见单质在常温常压下三种是气体,三种是固体。请回答下列问题:
(1)D离子的结构示意图____________________ ;F元素氧化物的晶体类型为______________ 。
(2)比较B、C、D元素简单离子半径的大小:____ >____ >____ (填微粒符号)
(3)请说出C的氢化物比F的氢化物稳定的根本原因:_____________ ;用高能射线照射液态水时,一个A2C分子能释放出一个电子,同时产生一种具有较强的氧化性的阳离子,试写出阳离子的电子式:____________ ,该阳离子中存在的化学键有_____________ ,并写出该阳离子与F氢化物的水溶液反应的离子方程式:____________ 。
(4)E是金属元素,且E单质可以与空气中的N2、CO2等反应,E的最高价氧化物的水化物难溶于水,已知298K时,该难溶物质的的KSP=5.6×10-12,若此时测得溶液pH=13.00,则此温度下残留在溶液中的E离子物质的量浓度为_______ mol·L-1。
(1)D离子的结构示意图
(2)比较B、C、D元素简单离子半径的大小:
(3)请说出C的氢化物比F的氢化物稳定的根本原因:
(4)E是金属元素,且E单质可以与空气中的N2、CO2等反应,E的最高价氧化物的水化物难溶于水,已知298K时,该难溶物质的的KSP=5.6×10-12,若此时测得溶液pH=13.00,则此温度下残留在溶液中的E离子物质的量浓度为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】物质结构包括原子结构、分子结构及晶体结构,物质结构决定了物质的性质。
(1)下列说法中正确的是_________ 。
A.半径:O2->Na+> Mg2+ B.含氧酸的酸性:Cl>S>P
C.简单氢化物的稳定性:N>O>F D.熔点:金刚石>碳化硅>硅单质
(2)C、N、O的电负性由大到小的顺序为_______ 。Na、Mg、Al的第一电离能由大到小的顺序为_______ 。
(3)乙酸分子中σ键与π键的数目比为_______ 。HCOOCH3是乙酸的一种同分异构体,但沸点却比乙酸低得多,原因是_______ 。
(4)已知AlC13在178℃升华,熔融时生成二聚体Al2Cl6(结构式如下)。
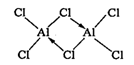
电解法制铝的原料是熔融的A12O3而不是AlC13,原因是________ ;电解法制镁的原料是熔融的MgCl2而不用MgO,原因是________ 。
(1)下列说法中正确的是
A.半径:O2->Na+> Mg2+ B.含氧酸的酸性:Cl>S>P
C.简单氢化物的稳定性:N>O>F D.熔点:金刚石>碳化硅>硅单质
(2)C、N、O的电负性由大到小的顺序为
(3)乙酸分子中σ键与π键的数目比为
(4)已知AlC13在178℃升华,熔融时生成二聚体Al2Cl6(结构式如下)。

电解法制铝的原料是熔融的A12O3而不是AlC13,原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ、前20号元素A、B、C、D,其中A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)C在周期表中的位置__________________________ ;
(2)B 元素的原子结构示意图____________________________ ;
(3)化合物D2C的电子式______________________________ ;
(4)B最简单气态氢化物与最简单的有机物的稳定性强弱关系(用相应的化学式表示):____ > ____ ;
(5)C、D离子的半径大小关系为C______ D (填:>、=、<);
(6)B的氢化物与B的最高价氧化物对应水化物反应的生成物中含有的的化学键有__________ 填选项)。
A、只含离子键 B、既有离子键又有共价键
C、只含有共价键 D、既有极性共价键又有非极性共价键
Ⅱ、利用下图装置来验证同主族元素非金属性的变化规律:
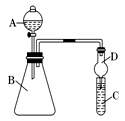
(1)要证明非金属性:Cl>I,在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾溶液,观察到C中溶液现象是:___________ ,即可证明。干燥管D的作用是___________________ 。从环境保护的角度考虑,此装置尚缺少尾气处理装置,可用_________________ 溶液吸收尾气。
(2)要证明非金属性:C>Si,在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,将观察到C中______________ 的现象。但老师认为,该现象不足以证明酸性强弱关系为碳酸>硅酸,因此应在B、D之间增加一个盛有足量__________ 的洗气装置(选填下列字母)
A.浓盐酸 B.浓NaOH溶液 C.饱和Na2CO3溶液 D.饱和NaHCO3溶液
(1)C在周期表中的位置
(2)B 元素的原子结构示意图
(3)化合物D2C的电子式
(4)B最简单气态氢化物与最简单的有机物的稳定性强弱关系(用相应的化学式表示):
(5)C、D离子的半径大小关系为C
(6)B的氢化物与B的最高价氧化物对应水化物反应的生成物中含有的的化学键有
A、只含离子键 B、既有离子键又有共价键
C、只含有共价键 D、既有极性共价键又有非极性共价键
Ⅱ、利用下图装置来验证同主族元素非金属性的变化规律:

(1)要证明非金属性:Cl>I,在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾溶液,观察到C中溶液现象是:
(2)要证明非金属性:C>Si,在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,将观察到C中
A.浓盐酸 B.浓NaOH溶液 C.饱和Na2CO3溶液 D.饱和NaHCO3溶液
您最近一年使用:0次



