碲在冶金工业中用途广泛,被誉为现代工业的维生素。某精炼铜的阳极泥经过处理后的主要成分为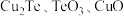 等,从中回收碲和胆矾的工艺如下:
等,从中回收碲和胆矾的工艺如下: 和
和 ;
;
② 在酸性条件下会发生歧化反应;
在酸性条件下会发生歧化反应;
③ 元素在酸化和碱浸后分别转化为
元素在酸化和碱浸后分别转化为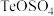 和
和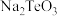
两种易溶于水的盐 。
回答下列问题:
(1)“高温焙烧”时,从结构的角度分析 的产物是
的产物是 而不是
而不是 的原因为
的原因为___________ 。
(2)“酸化”时还需要加入一定量的 ,其目的是
,其目的是___________ 。
(3)“还原”时发生反应的离子方程式为___________ 。
(4)碱浸后铜元素的存在形式为___________ (写化学式)。
(5)“电解”制 的原理如图,其中N与电源的
的原理如图,其中N与电源的___________ (填“正极”或“负极”)相连:与M相连的惰性电极上发生电极反应式为___________ 。
(7) 的立方晶胞结构如图。其中
的立方晶胞结构如图。其中 的配位数为
的配位数为___________ ;已知晶胞边长为 ,
, 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
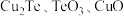 等,从中回收碲和胆矾的工艺如下:
等,从中回收碲和胆矾的工艺如下:
 和
和 ;
;②
 在酸性条件下会发生歧化反应;
在酸性条件下会发生歧化反应;③
 元素在酸化和碱浸后分别转化为
元素在酸化和碱浸后分别转化为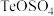 和
和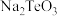
回答下列问题:
(1)“高温焙烧”时,从结构的角度分析
 的产物是
的产物是 而不是
而不是 的原因为
的原因为(2)“酸化”时还需要加入一定量的
 ,其目的是
,其目的是(3)“还原”时发生反应的离子方程式为
(4)碱浸后铜元素的存在形式为
(5)“电解”制
 的原理如图,其中N与电源的
的原理如图,其中N与电源的

| A.胆矾晶体中含有离子键、配位键、氢键等化学键 | B.胆矾属于离子晶体 |
C. 的空间结构为正四面体形 的空间结构为正四面体形 | D.电负性O>S,第一电离能 |
(7)
 的立方晶胞结构如图。其中
的立方晶胞结构如图。其中 的配位数为
的配位数为 ,
, 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。
更新时间:2023-06-22 08:49:53
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
【推荐1】现有某混合物的无色透明溶液,可能含有以下离子中的若干种:
Na+、NH4+、Cl-、Mg2+、Ba2+、 、SO42-,现取三份各100mL溶液进行如下实验:
、SO42-,现取三份各100mL溶液进行如下实验:
①第一份加入足量AgNO3溶液有沉淀产生,加足量稀硝酸后沉淀部分溶解;
②第二份加足量NaOH溶液充分加热后,收集到气体0.896L(标准状况);
③第三份加足量BaCl2溶液后,过滤后充分干燥得到沉淀6.27g,再经足量稀硝酸洗涤、干燥后,沉淀质量变为2.33g。根据上述实验现象和有关数据,回答下列问题:
(1)原溶液中一定存在的阴离子是_________ ,一定不存在的离子是_________ ,可能存在的离子是_____________ 。
(2)②中发生化学反应的离子方程式为___________ 。
(3)③中生成可溶于稀硝酸的沉淀化学式为___________ ,物质的量为___________ mol,该沉淀溶于稀硝酸的离子方程式为____________ 。
Na+、NH4+、Cl-、Mg2+、Ba2+、
 、SO42-,现取三份各100mL溶液进行如下实验:
、SO42-,现取三份各100mL溶液进行如下实验:①第一份加入足量AgNO3溶液有沉淀产生,加足量稀硝酸后沉淀部分溶解;
②第二份加足量NaOH溶液充分加热后,收集到气体0.896L(标准状况);
③第三份加足量BaCl2溶液后,过滤后充分干燥得到沉淀6.27g,再经足量稀硝酸洗涤、干燥后,沉淀质量变为2.33g。根据上述实验现象和有关数据,回答下列问题:
(1)原溶液中一定存在的阴离子是
(2)②中发生化学反应的离子方程式为
(3)③中生成可溶于稀硝酸的沉淀化学式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】明矾 在工业上用作净水剂,医药上用作收敛剂。实验小组采用废弃的铝制易拉罐按如下流程制备明矾大晶体。
在工业上用作净水剂,医药上用作收敛剂。实验小组采用废弃的铝制易拉罐按如下流程制备明矾大晶体。
(1)废铝制易拉罐溶于KOH溶液发生的主要反应为___________ (用离子方程式表示)。
(2)下列说法不正确的是___________。
(3)“系列操作II”的装置如图所示,烧杯上方所盖的纸片的作用是___________ 。 是一种慢性神经毒素,长期积累会导致神经结节。实验室可采用置换滴定法测定天然水体样品中的
是一种慢性神经毒素,长期积累会导致神经结节。实验室可采用置换滴定法测定天然水体样品中的 浓度。简要过程如下:
浓度。简要过程如下:

有关反应如下(试剂EDTA用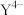 表示):
表示):
步骤①: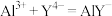
步骤②: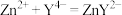
步骤③: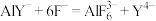
①下列有关说法不正确的是___________ 。
B.天然水体样品中的 (
(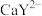 不与F反应)不影响
不与F反应)不影响 含量的测定
含量的测定
C.步骤①所加试剂EDTA,实验前不需要标定其浓度
D.如果步骤②所加 标准溶液偏少,会导致
标准溶液偏少,会导致 浓度的测定值小于真实值
浓度的测定值小于真实值
②根据检测过程,请给出配合离子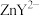 、
、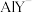 、
、 的稳定性由弱到强的顺序:
的稳定性由弱到强的顺序:___________ 。
③要准确计算水样中 浓度,须利用水样1的体积以及步骤
浓度,须利用水样1的体积以及步骤______ 的实验数据(选填:①、②、③、④)
 在工业上用作净水剂,医药上用作收敛剂。实验小组采用废弃的铝制易拉罐按如下流程制备明矾大晶体。
在工业上用作净水剂,医药上用作收敛剂。实验小组采用废弃的铝制易拉罐按如下流程制备明矾大晶体。
(1)废铝制易拉罐溶于KOH溶液发生的主要反应为
(2)下列说法不正确的是___________。
| A.可采取将废易拉罐剪碎、酒精灯加热等方式加快溶解速率 |
| B.加入KOH溶液至不再产生气泡后,趁热过滤,除去不溶物 |
| C.“系列操作I”有:蒸发浓缩、冷却结晶、过滤洗涤灼烧 |
| D.制备明矾大晶体时,小晶体应悬挂在靠近烧杯底部的位置 |
(3)“系列操作II”的装置如图所示,烧杯上方所盖的纸片的作用是

 是一种慢性神经毒素,长期积累会导致神经结节。实验室可采用置换滴定法测定天然水体样品中的
是一种慢性神经毒素,长期积累会导致神经结节。实验室可采用置换滴定法测定天然水体样品中的 浓度。简要过程如下:
浓度。简要过程如下:
有关反应如下(试剂EDTA用
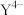 表示):
表示):步骤①:
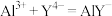
步骤②:
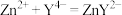
步骤③:
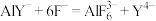
①下列有关说法不正确的是

B.天然水体样品中的
 (
(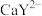 不与F反应)不影响
不与F反应)不影响 含量的测定
含量的测定C.步骤①所加试剂EDTA,实验前不需要标定其浓度
D.如果步骤②所加
 标准溶液偏少,会导致
标准溶液偏少,会导致 浓度的测定值小于真实值
浓度的测定值小于真实值②根据检测过程,请给出配合离子
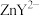 、
、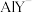 、
、 的稳定性由弱到强的顺序:
的稳定性由弱到强的顺序:③要准确计算水样中
 浓度,须利用水样1的体积以及步骤
浓度,须利用水样1的体积以及步骤
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】废铅蓄电池是发展循环铅产业的重要二次资源,对其进行资源化处理和清洁回收是铅工业可持续发展的一条重要途径,某课题组进行了如下处理:

已知:①废铅膏的主要成分为 ,还含有
,还含有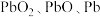 等;
等;
② 为一元强酸。
为一元强酸。
回答下列问题:
(1)铅与碳同主族,且位于第六周期,则铅的价电子排布图为_______ 。
(2)脱硫废液的成分为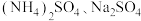 ,在“盐浸脱硫”实验中,脱硫率随时间的变化如下图所示,当脱硫率为80%时,可采用的实验条件为
,在“盐浸脱硫”实验中,脱硫率随时间的变化如下图所示,当脱硫率为80%时,可采用的实验条件为_______ ,若温度过高(高于90℃)时,单位时间内脱硫率降低,可能的原因是_______ 。

(3)“盐浸脱硫”过程需要严格控制 的用量,
的用量, 过量易生成
过量易生成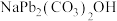 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(4)浸出液的主要成分为 ,
, 溶解反应的离子方程式为
溶解反应的离子方程式为_______ 。
(5)“电解”操作中,应该以_______ 作为阳极电极材料,电解废液经加热浓缩得到_______ (填化学式),可进行循环利用。若在实验室中进行浓缩操作,应该用_______ (填仪器名称)进行。

已知:①废铅膏的主要成分为
 ,还含有
,还含有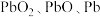 等;
等;②
 为一元强酸。
为一元强酸。回答下列问题:
(1)铅与碳同主族,且位于第六周期,则铅的价电子排布图为
(2)脱硫废液的成分为
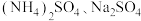 ,在“盐浸脱硫”实验中,脱硫率随时间的变化如下图所示,当脱硫率为80%时,可采用的实验条件为
,在“盐浸脱硫”实验中,脱硫率随时间的变化如下图所示,当脱硫率为80%时,可采用的实验条件为
(3)“盐浸脱硫”过程需要严格控制
 的用量,
的用量, 过量易生成
过量易生成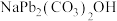 ,该反应的化学方程式为
,该反应的化学方程式为(4)浸出液的主要成分为
 ,
, 溶解反应的离子方程式为
溶解反应的离子方程式为(5)“电解”操作中,应该以
您最近一年使用:0次
【推荐1】 捕集技术能有效解决温室效应及能源短缺问题。
捕集技术能有效解决温室效应及能源短缺问题。
(1) 催化加氢制
催化加氢制 的反应体系中,发生的反应如下:
的反应体系中,发生的反应如下:
反应Ⅰ:

反应Ⅱ:

反应Ⅲ:

将 与
与 按照一定流速通过催化剂反应,测得
按照一定流速通过催化剂反应,测得 的转化率与产物的选择性[
的转化率与产物的选择性[ 选择性
选择性 ]随温度变化如图所示:
]随温度变化如图所示:

①
_______ (用含 、
、 的式子表示)。
的式子表示)。
②340℃时,原料气按 相同流速通过催化剂反应,出口处测得气体中
相同流速通过催化剂反应,出口处测得气体中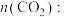

_______ 。
(2)电催化还原 生成含碳产物(如CO、
生成含碳产物(如CO、 等)原理如图所示:
等)原理如图所示:

①若阴极产物为 ,则该电极反应式为
,则该电极反应式为_______ 。
②在25℃下将 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中 ,则溶液显
,则溶液显_______ (填酸、碱或中)性;用含a的代数式表示 的电离常数
的电离常数
_______ 。
③现有含有 和
和 的混合溶液,若溶液中
的混合溶液,若溶液中 ,加入碳酸钠调节溶液的pH为
,加入碳酸钠调节溶液的pH为_______ 可使 恰好沉淀完全(离子浓度
恰好沉淀完全(离子浓度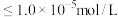 ),此时
),此时_______ (填“有”或“无”) 沉淀生成。(假设溶液体积不变,
沉淀生成。(假设溶液体积不变,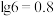 ;
; ,
,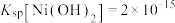 )
)
(3)已知 和
和 的溶度积常数
的溶度积常数 分别为
分别为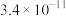 和
和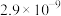 ,在浓度均为0.10mol/L的
,在浓度均为0.10mol/L的 和
和 的混合溶液中加入HF,当
的混合溶液中加入HF,当 离子开始沉淀时,溶液中
离子开始沉淀时,溶液中 的浓度为
的浓度为_______ (保留两位有效数字)。
(4)生成 沉淀是利用反应
沉淀是利用反应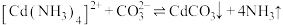 ,常温下,该反应平衡常数
,常温下,该反应平衡常数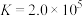 ,
, 的平衡常数
的平衡常数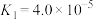 ,则
,则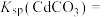
_______ 。
 捕集技术能有效解决温室效应及能源短缺问题。
捕集技术能有效解决温室效应及能源短缺问题。(1)
 催化加氢制
催化加氢制 的反应体系中,发生的反应如下:
的反应体系中,发生的反应如下:反应Ⅰ:


反应Ⅱ:


反应Ⅲ:


将
 与
与 按照一定流速通过催化剂反应,测得
按照一定流速通过催化剂反应,测得 的转化率与产物的选择性[
的转化率与产物的选择性[ 选择性
选择性 ]随温度变化如图所示:
]随温度变化如图所示:
①

 、
、 的式子表示)。
的式子表示)。②340℃时,原料气按
 相同流速通过催化剂反应,出口处测得气体中
相同流速通过催化剂反应,出口处测得气体中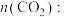

(2)电催化还原
 生成含碳产物(如CO、
生成含碳产物(如CO、 等)原理如图所示:
等)原理如图所示:
①若阴极产物为
 ,则该电极反应式为
,则该电极反应式为②在25℃下将
 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中 ,则溶液显
,则溶液显 的电离常数
的电离常数
③现有含有
 和
和 的混合溶液,若溶液中
的混合溶液,若溶液中 ,加入碳酸钠调节溶液的pH为
,加入碳酸钠调节溶液的pH为 恰好沉淀完全(离子浓度
恰好沉淀完全(离子浓度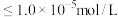 ),此时
),此时 沉淀生成。(假设溶液体积不变,
沉淀生成。(假设溶液体积不变, ;
; ,
,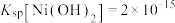 )
)(3)已知
 和
和 的溶度积常数
的溶度积常数 分别为
分别为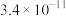 和
和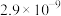 ,在浓度均为0.10mol/L的
,在浓度均为0.10mol/L的 和
和 的混合溶液中加入HF,当
的混合溶液中加入HF,当 离子开始沉淀时,溶液中
离子开始沉淀时,溶液中 的浓度为
的浓度为(4)生成
 沉淀是利用反应
沉淀是利用反应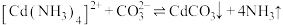 ,常温下,该反应平衡常数
,常温下,该反应平衡常数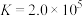 ,
, 的平衡常数
的平衡常数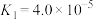 ,则
,则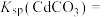
您最近一年使用:0次
【推荐2】矿石燃料的直接燃烧不仅会有能量利用率低的问题,还会造成严重的环境污染,释放出大量 等污染气体。但是如果加以良好的利用,排放的污染物也会变废为宝。
等污染气体。但是如果加以良好的利用,排放的污染物也会变废为宝。
Ⅰ.在化工生产过程中,少量CO的存在会引起催化剂中毒。为了防止催化剂中毒,用 将CO氧化,
将CO氧化, 被还原为固态S。
被还原为固态S。
已知:

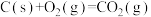

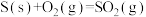

(1) 氧化
氧化 的热化学方程式为
的热化学方程式为_______ 。
Ⅱ.为了减少对环境的污染,煤在直接燃烧前要进行脱硫处理。应用电解法对煤进行脱硫处理具有脱硫效率高、经济效益好等优点。电解脱硫的基本原理如图所示,利用电极反应将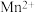 转化成
转化成 、
、 再将煤中的含硫物质(主要是)氧化为
再将煤中的含硫物质(主要是)氧化为 和
和 。
。

(2)写出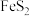 被氧化过程的离子方程式
被氧化过程的离子方程式_______ 。电解过程中,外电路每转移1mol电子,溶液中 的物质的量将
的物质的量将_______ mol(可用分数表示)。
Ⅲ.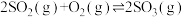 是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。
是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。
(3)一定条件下,在2L密闭容器中加入4mol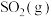 、6mol
、6mol 和2mol
和2mol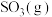 发生上述反应,在2min末达到平衡,测得
发生上述反应,在2min末达到平衡,测得 。
。
①该条件下反应的平衡常数
_______ ,若平衡后保持恒容再加入 、
、 、
、 各1mol,此
各1mol,此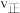
_______  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
②恒温恒容下,能说明该反应达到化学平衡状态的是_______ (填字母序号)。
a.
b.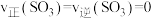
c.混合气体的密度不再变化
d. 不再变化
不再变化
e.单位时间内生成n mol 的同时生成2n mol
的同时生成2n mol
 等污染气体。但是如果加以良好的利用,排放的污染物也会变废为宝。
等污染气体。但是如果加以良好的利用,排放的污染物也会变废为宝。Ⅰ.在化工生产过程中,少量CO的存在会引起催化剂中毒。为了防止催化剂中毒,用
 将CO氧化,
将CO氧化, 被还原为固态S。
被还原为固态S。已知:


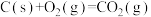

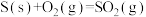

(1)
 氧化
氧化 的热化学方程式为
的热化学方程式为Ⅱ.为了减少对环境的污染,煤在直接燃烧前要进行脱硫处理。应用电解法对煤进行脱硫处理具有脱硫效率高、经济效益好等优点。电解脱硫的基本原理如图所示,利用电极反应将
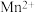 转化成
转化成 、
、 再将煤中的含硫物质(主要是)氧化为
再将煤中的含硫物质(主要是)氧化为 和
和 。
。
(2)写出
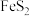 被氧化过程的离子方程式
被氧化过程的离子方程式 的物质的量将
的物质的量将Ⅲ.
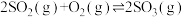 是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。
是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。(3)一定条件下,在2L密闭容器中加入4mol
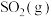 、6mol
、6mol 和2mol
和2mol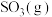 发生上述反应,在2min末达到平衡,测得
发生上述反应,在2min末达到平衡,测得 。
。①该条件下反应的平衡常数

 、
、 、
、 各1mol,此
各1mol,此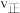
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)②恒温恒容下,能说明该反应达到化学平衡状态的是
a.

b.
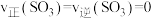
c.混合气体的密度不再变化
d.
 不再变化
不再变化e.单位时间内生成n mol
 的同时生成2n mol
的同时生成2n mol
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】含硫化合物的污染主要来源于化石燃料的燃烧、硫酸工厂的废液和炼焦、炼油厂的废气。
(1)燃煤的电化学脱硫是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(•OH)将燃煤中的含硫物质氧化除去,其装置示意图如图所示。

①将煤打成煤浆加入电解槽的目的是___ 。
②阳极的电极反应式为__ 。
(2)某硫酸厂的废液中含有一定浓度的硫酸(废液中微量的重金属离子可忽略)。为确定中和法处理该厂废液时生石灰的投料量,现取20.00mL废液放入锥形瓶中,加入酚酞作指示剂,用0.0200mol•L-1的NaOH标准溶液进行滴定。重复上述滴定操作2次。三次实验消耗NaOH溶液的体积依次为24.10mL、25.70mL和23.90mL。

①滴定前排除碱式滴定管中气泡的方法应采用如图所示操作中的___ ,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
②该硫酸厂的废液中H2SO4的物质的量浓度为___ 。
③下列操作(其他操作正确)会造成上述实验测定结果偏高的有___ (填字母)。
A.滴定终点时俯视读数 B.碱式滴定管水洗后未用标准液润洗
C.锥形瓶水洗后未干燥 D.滴定前滴定管尖嘴处有气泡,滴定后消失
(3)炼焦、炼油厂的废气中含有H2S、H2S溶于水形成的氢硫酸是一种二元弱酸。25℃时,在0.10mol•L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时溶液中的c(H2S)+c(HS-)=___ mol•L-1;
②某溶液含0.010mol•L-1Fe2+和0.10mol•L-1H2S,当溶液pH=___ 时,Fe2+开始沉淀。(已知:Ksp(FeS)=1.4×10-19)
(1)燃煤的电化学脱硫是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(•OH)将燃煤中的含硫物质氧化除去,其装置示意图如图所示。

①将煤打成煤浆加入电解槽的目的是
②阳极的电极反应式为
(2)某硫酸厂的废液中含有一定浓度的硫酸(废液中微量的重金属离子可忽略)。为确定中和法处理该厂废液时生石灰的投料量,现取20.00mL废液放入锥形瓶中,加入酚酞作指示剂,用0.0200mol•L-1的NaOH标准溶液进行滴定。重复上述滴定操作2次。三次实验消耗NaOH溶液的体积依次为24.10mL、25.70mL和23.90mL。

①滴定前排除碱式滴定管中气泡的方法应采用如图所示操作中的
②该硫酸厂的废液中H2SO4的物质的量浓度为
③下列操作(其他操作正确)会造成上述实验测定结果偏高的有
A.滴定终点时俯视读数 B.碱式滴定管水洗后未用标准液润洗
C.锥形瓶水洗后未干燥 D.滴定前滴定管尖嘴处有气泡,滴定后消失
(3)炼焦、炼油厂的废气中含有H2S、H2S溶于水形成的氢硫酸是一种二元弱酸。25℃时,在0.10mol•L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时溶液中的c(H2S)+c(HS-)=
②某溶液含0.010mol•L-1Fe2+和0.10mol•L-1H2S,当溶液pH=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】工业合成氨是人类科学技术的一项重大突破。迄今为止,人类仍然在追求低成本、高产率的合成氨技术。

(1)已知 时,
时, 的燃烧热
的燃烧热 ;
;
 。
。
①某种新型储氢材料的晶胞如图1所示,八面体中心为某价态铁的离子,顶点均为 配体;四面体中心为硼原子,顶点均为氢原子。该化合物的化学式为
配体;四面体中心为硼原子,顶点均为氢原子。该化合物的化学式为___________ ,化合物中铁的电子排布式为___________ 。
②有人提出利用 反应制备
反应制备 的思路。请结合有关数据说明该反应难以实现的原因:
的思路。请结合有关数据说明该反应难以实现的原因:___________ 。
(2)科学家通过大量理论分析和实践研究,提出了一种间接电化学合成 的新方法,其物质转化关系可表示为
的新方法,其物质转化关系可表示为 。
。
①科学家经过研究后选择 代替
代替 间接合成
间接合成 ,其原因一定成立的是
,其原因一定成立的是___________ 。
A. 的第一电离能比
的第一电离能比 的大
的大
B. 熔点比
熔点比 低,熔融时耗能更小
低,熔融时耗能更小
C. 来源比
来源比 更丰富
更丰富
②写出 的电子式:
的电子式:___________ 。
③ 为
为 溶液时,产生
溶液时,产生 的量远大于
的量远大于 为
为 的原因是
的原因是___________ 。
(3)经过理论计算并结合实验测量得出铁触媒表面合成氨反应全过程的能量变化如图2所示。其中(ad)表示吸附在催化剂表面。我国科学家提出了一种使用双温双控催化剂提高合成氨产率的新方法。该催化剂是在纳米铁表面复合少量具有光学活性的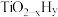 ,通过光辐射产生温差(如体系温度为495℃时,
,通过光辐射产生温差(如体系温度为495℃时, 的温度能达到547℃,而
的温度能达到547℃,而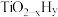 表面为415℃)。其催化合成氨机理如图3所示。
表面为415℃)。其催化合成氨机理如图3所示。

①500℃下 的平衡浓度较400℃低的原因是
的平衡浓度较400℃低的原因是___________ 。
②与传统的催化合成氨(铁触媒、400~500℃)相比,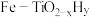 双催化剂双温催化合成氨更具优势的原因是
双催化剂双温催化合成氨更具优势的原因是___________ 。

(1)已知
 时,
时, 的燃烧热
的燃烧热 ;
; 。
。①某种新型储氢材料的晶胞如图1所示,八面体中心为某价态铁的离子,顶点均为
 配体;四面体中心为硼原子,顶点均为氢原子。该化合物的化学式为
配体;四面体中心为硼原子,顶点均为氢原子。该化合物的化学式为②有人提出利用
 反应制备
反应制备 的思路。请结合有关数据说明该反应难以实现的原因:
的思路。请结合有关数据说明该反应难以实现的原因:(2)科学家通过大量理论分析和实践研究,提出了一种间接电化学合成
 的新方法,其物质转化关系可表示为
的新方法,其物质转化关系可表示为 。
。①科学家经过研究后选择
 代替
代替 间接合成
间接合成 ,其原因一定成立的是
,其原因一定成立的是A.
 的第一电离能比
的第一电离能比 的大
的大B.
 熔点比
熔点比 低,熔融时耗能更小
低,熔融时耗能更小C.
 来源比
来源比 更丰富
更丰富②写出
 的电子式:
的电子式:③
 为
为 溶液时,产生
溶液时,产生 的量远大于
的量远大于 为
为 的原因是
的原因是(3)经过理论计算并结合实验测量得出铁触媒表面合成氨反应全过程的能量变化如图2所示。其中(ad)表示吸附在催化剂表面。我国科学家提出了一种使用双温双控催化剂提高合成氨产率的新方法。该催化剂是在纳米铁表面复合少量具有光学活性的
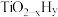 ,通过光辐射产生温差(如体系温度为495℃时,
,通过光辐射产生温差(如体系温度为495℃时, 的温度能达到547℃,而
的温度能达到547℃,而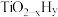 表面为415℃)。其催化合成氨机理如图3所示。
表面为415℃)。其催化合成氨机理如图3所示。
①500℃下
 的平衡浓度较400℃低的原因是
的平衡浓度较400℃低的原因是②与传统的催化合成氨(铁触媒、400~500℃)相比,
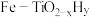 双催化剂双温催化合成氨更具优势的原因是
双催化剂双温催化合成氨更具优势的原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】2022年诺贝尔化学奖授予在发展点击化学方面做出贡献的科学家。点击化学的代表反应为CuCl催化的叠氮—炔基Husigen环加成反应,常用的无机试剂有 、
、 等。
等。
(1)铜在元素周期表中位置为___________ ,基态 的价电子排布式为
的价电子排布式为___________ 。
(2)N、S、O、F的第一电离能由大到小顺序为___________ 。
(3) 的分子结构如图所示,键角
的分子结构如图所示,键角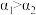 的原因主要是
的原因主要是___________ 。

(4) 是叠氮酸(
是叠氮酸( )的钠盐,
)的钠盐, 在常温下是液体,沸点相对较高,为308.8K,主要原因是
在常温下是液体,沸点相对较高,为308.8K,主要原因是___________ 。 分子的空间结构如图所示(图中键长单位为
分子的空间结构如图所示(图中键长单位为 )。
)。 、
、 和N≡N的共价键键长分别为
和N≡N的共价键键长分别为 、
、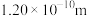 和
和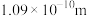 ;试画出
;试画出 分子的结构式
分子的结构式___________ 。
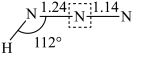
(5)CuCl的晶胞中, 的位置如图所示。
的位置如图所示。 填充于
填充于 构成的四面体空隙中,则
构成的四面体空隙中,则 的配位数为
的配位数为___________ ;若 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 ,则该晶胞中
,则该晶胞中 之间的距离为
之间的距离为___________ nm(用含ρ、 的代数式表示)。
的代数式表示)。

 、
、 等。
等。(1)铜在元素周期表中位置为
 的价电子排布式为
的价电子排布式为(2)N、S、O、F的第一电离能由大到小顺序为
(3)
 的分子结构如图所示,键角
的分子结构如图所示,键角 的原因主要是
的原因主要是
(4)
 是叠氮酸(
是叠氮酸( )的钠盐,
)的钠盐, 在常温下是液体,沸点相对较高,为308.8K,主要原因是
在常温下是液体,沸点相对较高,为308.8K,主要原因是 分子的空间结构如图所示(图中键长单位为
分子的空间结构如图所示(图中键长单位为 )。
)。 、
、 和N≡N的共价键键长分别为
和N≡N的共价键键长分别为 、
、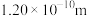 和
和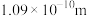 ;试画出
;试画出 分子的结构式
分子的结构式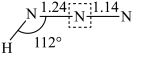
(5)CuCl的晶胞中,
 的位置如图所示。
的位置如图所示。 填充于
填充于 构成的四面体空隙中,则
构成的四面体空隙中,则 的配位数为
的配位数为 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 ,则该晶胞中
,则该晶胞中 之间的距离为
之间的距离为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】现有A、B、C、D、E、F、G、H八种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
A:核外电子数和电子层数相等,也是宇宙中最丰富的元素
B:形成化合物种类最多的元素
C:基态原子的核外p能级电子数比s能级电子数少1
D:基态原子的核外p轨道中有两个未成对电子
E:气态基态原子的第一至第四电离能分别是:I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol
F:同周期元素的简单离子中半径最小
G:主族序数与周期数的差为4
H:前四周期主族元素中电负性最小
(1)C2A4的电子式为_______ 。
(2)B元素的原子核外共有_______ 种不同空间运动状态的电子,电子所处最高能级轨道的形状为_______ 。
(3)G2D分子的VSEPR模型名称为_______ 。
(4)某同学推断E元素基态原子的轨道表示式为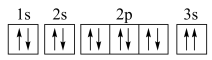 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了_______ ,解释E元素原子的第一电离能大于F元素原子的第一电离能的原因:_______ 。
(5)B2A4分子中含有的σ键、π键数目之比为_______ 。
(6)与F元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与H元素的最高价氧化物的水化物反应的离子方程式:_______ 。
(7)与H元素同周期的基态原子中,未成对电子数与H原子相同的元素有_______ 种。
A:核外电子数和电子层数相等,也是宇宙中最丰富的元素
B:形成化合物种类最多的元素
C:基态原子的核外p能级电子数比s能级电子数少1
D:基态原子的核外p轨道中有两个未成对电子
E:气态基态原子的第一至第四电离能分别是:I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol
F:同周期元素的简单离子中半径最小
G:主族序数与周期数的差为4
H:前四周期主族元素中电负性最小
(1)C2A4的电子式为
(2)B元素的原子核外共有
(3)G2D分子的VSEPR模型名称为
(4)某同学推断E元素基态原子的轨道表示式为
 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了(5)B2A4分子中含有的σ键、π键数目之比为
(6)与F元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与H元素的最高价氧化物的水化物反应的离子方程式:
(7)与H元素同周期的基态原子中,未成对电子数与H原子相同的元素有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】氮族元素(N、P、As、Sb、Bi)的单质及其化合物在生产和生活中有广泛的应用。回答下列问题:
(1)写出基态As原子的核外电子排布式_______ ,有______ 个未成对电子。
(2)五氧化二磷(P2O3)是磷在氧气中燃烧生成的白色无定形粉末或六方晶体。在白磷分子的每一个磷键上插入一个氧原子,剩余四个氧原子分别通过配位键与四个磷原子相连。则P2O5是______ (填“极性”或“非极性”)分子,磷原子的杂化方式为______ 。
(3)锑的氧化物用于制取白色颜料、油漆和塑料,焰色反应是红紫色的。下列说法正确的是_______ (填字母)。
A.锑的轨道表示式为[Kr]
B.物质的焰色反应肯定只发生物理变化
C.电子吸收能量从较低的轨道跃迁到能量较高的轨道,很快跃迁回能量较低的轨道,这时就将多余的能量以光的形式放出
D.KCl和NaCl能用焰色反应实验区分
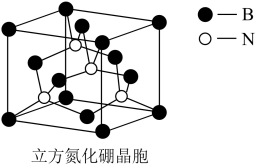
(4)立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶胞结构如图所示。25 g立方氮化硼,含有B-N键的个数为______ ,含有配位键的个数为_______ 。若晶体密度为a g·cm-3,则N与B最近的距离为_____ pm。(阿伏加德罗常数用NA表示,列出计算表达式,不用化简)
(1)写出基态As原子的核外电子排布式
(2)五氧化二磷(P2O3)是磷在氧气中燃烧生成的白色无定形粉末或六方晶体。在白磷分子的每一个磷键上插入一个氧原子,剩余四个氧原子分别通过配位键与四个磷原子相连。则P2O5是
(3)锑的氧化物用于制取白色颜料、油漆和塑料,焰色反应是红紫色的。下列说法正确的是
A.锑的轨道表示式为[Kr]

B.物质的焰色反应肯定只发生物理变化
C.电子吸收能量从较低的轨道跃迁到能量较高的轨道,很快跃迁回能量较低的轨道,这时就将多余的能量以光的形式放出
D.KCl和NaCl能用焰色反应实验区分
(4)立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶胞结构如图所示。25 g立方氮化硼,含有B-N键的个数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】“嫦娥五号”首次实现了我国地外天体采样返回,带回的月壤中包含了H、O、N、A1、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。回答下列问题:
(1)锌(Zn)、镉(Cd)是同一副族的相邻元素,Cd的原子序数更大,则基态Cd原子的价电子轨道表示式为_______ 。
(2)若配离子[Fe(CN)x](x-2)-的中心离子价电子数与配体提供的电子数之和为18,则x=_______ 。
(3)碲和硫同主族,TeO 的空间构型为
的空间构型为_______ ,写出一个与TeO 互为等电子体的分子
互为等电子体的分子_______ 。
(4)咪唑、噻唑、吡啶是含N和S的有机杂环类化合物,结构如图所示:

①上述三种物质中,沸点最高的是_______ (填化学名称)。
②吡啶中氮原子的杂化轨道的空间构型为_______ 。
③已知咪唑中存在大π键,则在咪唑分子的两个氮原子中,更容易与Cu2+形成配位键的是_______ (填“①”或“②”)号氮原子。
(5)Fe3+容易形成六配位的配合物,[Fe(H2O)6]3+通常会水解生成棕色的[Fe(H2O)5(OH)]2+,通过氢氧根离子形成双聚体[Fe2(H2O)8(OH)2]4+,请写出该双聚体的结构(水分子中O-H键省略,其他化学键用短横线“-”表示)_______ 。
(6)“嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),已知该结构单元底面(正六边形)边长为anm,该合金的密度为ρg·cm-3,则h=_______ cm(列出计算式,设NA为阿伏加德罗常数的值)。

(1)锌(Zn)、镉(Cd)是同一副族的相邻元素,Cd的原子序数更大,则基态Cd原子的价电子轨道表示式为
(2)若配离子[Fe(CN)x](x-2)-的中心离子价电子数与配体提供的电子数之和为18,则x=
(3)碲和硫同主族,TeO
 的空间构型为
的空间构型为 互为等电子体的分子
互为等电子体的分子(4)咪唑、噻唑、吡啶是含N和S的有机杂环类化合物,结构如图所示:

①上述三种物质中,沸点最高的是
②吡啶中氮原子的杂化轨道的空间构型为
③已知咪唑中存在大π键,则在咪唑分子的两个氮原子中,更容易与Cu2+形成配位键的是
(5)Fe3+容易形成六配位的配合物,[Fe(H2O)6]3+通常会水解生成棕色的[Fe(H2O)5(OH)]2+,通过氢氧根离子形成双聚体[Fe2(H2O)8(OH)2]4+,请写出该双聚体的结构(水分子中O-H键省略,其他化学键用短横线“-”表示)
(6)“嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),已知该结构单元底面(正六边形)边长为anm,该合金的密度为ρg·cm-3,则h=

您最近一年使用:0次
【推荐3】精脱硫技术主要用于煤气中羰基硫(COS)和二硫化碳(CS2)的转化。回答下列问题:
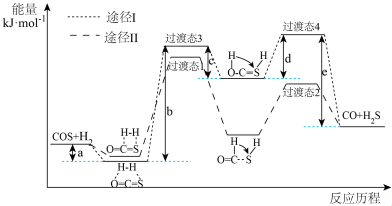
(1)利用焦炉煤气中的H2可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径I和途径Ⅱ两种可能,如图所示:___________ (填“I”或“Ⅱ”)。
②反应 的△H=
的△H=___________ kJ·mol-1。
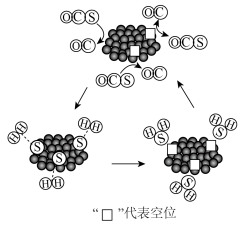
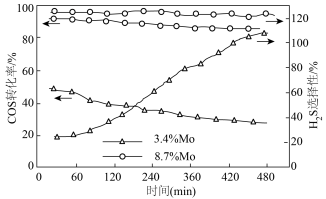
(2)MoS2可作羰基硫氢化反应的催化剂,催化机理如图所示:___________ (填“3.4%Mo”或“8.7%Mo”)作催化剂效果最好;当H2S选择性低于100%时表明部分COS气体与催化剂发生了反应,催化剂有吸硫现象,若H2S选择性高于100%,可能的原因是___________ 。
(3)金属Mo的晶胞如图所示,若原子a、b的坐标分别为(0,0,0)、(1,0,0),则原子c的坐标为___________ ,设晶体密度为ρg·cm3,则晶胞参数为___________ pm(阿伏加德罗常数的值为NA)。 ,容器内气体压强随时间变化如下表所示。
,容器内气体压强随时间变化如下表所示。
①0-250min内,H2分压的平均变化值为___________ kPa·min-l。
②该温度下,平衡常数Kp=___________ (kPa)-2(列出计算式)。
(1)利用焦炉煤气中的H2可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径I和途径Ⅱ两种可能,如图所示:
②反应
 的△H=
的△H=(2)MoS2可作羰基硫氢化反应的催化剂,催化机理如图所示:
(3)金属Mo的晶胞如图所示,若原子a、b的坐标分别为(0,0,0)、(1,0,0),则原子c的坐标为

 ,容器内气体压强随时间变化如下表所示。
,容器内气体压强随时间变化如下表所示。| 时间/min | 0 | 50 | 100 | 150 | 200 | 250 | 300 |
| 压强/kPa | 100 | 88.0 | 79.8 | 72.4 | 68.2 | 65.0 | 65.0 |
②该温度下,平衡常数Kp=
您最近一年使用:0次



