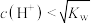25℃时,用HCl气体调节 氨水的pH,体系中微粒浓度的对数值(
氨水的pH,体系中微粒浓度的对数值( )与pH的关系如图1所示(a、b、c、d线分别对应体系中除
)与pH的关系如图1所示(a、b、c、d线分别对应体系中除 和
和 外的其它微粒),反应物的物质的量之比
外的其它微粒),反应物的物质的量之比 与pH的关系如图2所示(忽略通入气体后引起的溶液体积变化)。
与pH的关系如图2所示(忽略通入气体后引起的溶液体积变化)。
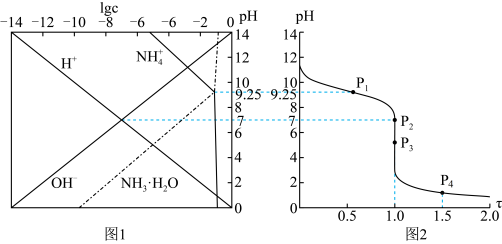
下列说法错误的是
 氨水的pH,体系中微粒浓度的对数值(
氨水的pH,体系中微粒浓度的对数值( )与pH的关系如图1所示(a、b、c、d线分别对应体系中除
)与pH的关系如图1所示(a、b、c、d线分别对应体系中除 和
和 外的其它微粒),反应物的物质的量之比
外的其它微粒),反应物的物质的量之比 与pH的关系如图2所示(忽略通入气体后引起的溶液体积变化)。
与pH的关系如图2所示(忽略通入气体后引起的溶液体积变化)。
下列说法错误的是
A. 水解平衡常数的数量级为 水解平衡常数的数量级为 |
B. 对应溶液: 对应溶液: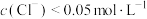 |
C.水的电离程度: |
D. 对应溶液: 对应溶液: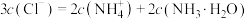 |
22-23高二上·山东滨州·期末 查看更多[2]
更新时间:2023-07-28 17:18:35
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下图是某水溶液常温下pH 从0 到14 的范围内H2CO3、HCO3-、CO32- 三种成分平衡时组成分数,下列叙述正确的是
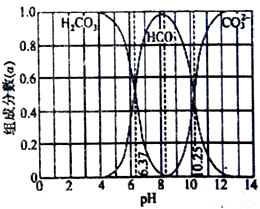

| A.此图是1.0mol/L碳酸钠溶液滴定1.0mol/L 盐酸的滴定曲线 |
| B.向pH=10.25 的溶液中通HCl 气体使pH=7,此时c(H2CO3)>c(Cl-)= c(HCO3-)>c(CO32- ) |
| C.人体血液的pH 约为7.4,则CO2在血液中多以HCO3-形式存在 |
| D.该温度下,碳酸氢根的水解平衡常数Kh= 10-3.75 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
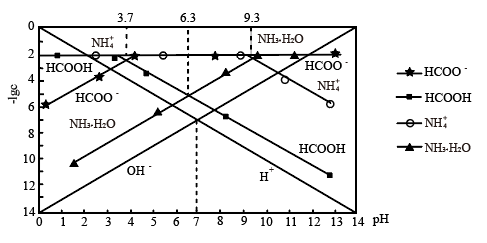
【推荐2】某温度时,分别调节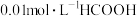 溶液、
溶液、 氨水的pH,系统中各种粒子浓度的负对数值
氨水的pH,系统中各种粒子浓度的负对数值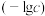 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是
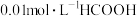 溶液、
溶液、 氨水的pH,系统中各种粒子浓度的负对数值
氨水的pH,系统中各种粒子浓度的负对数值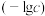 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是
| A.系统温度高于25℃ |
B.该温度下,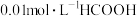 溶液的pH为3.7 溶液的pH为3.7 |
C.用标准 溶液滴定一定浓度的 溶液滴定一定浓度的 溶液用酚酞作指示剂 溶液用酚酞作指示剂 |
D.向 溶液中加入 溶液中加入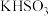 溶液至溶液呈中性: 溶液至溶液呈中性: |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】已知:①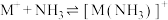

②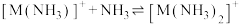

 、
、 、
、 的分布分数
的分布分数 与
与 关系如下图所示。下列说法正确的是
关系如下图所示。下列说法正确的是
{分布分数 }
}
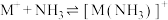

②
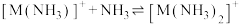

 、
、 、
、 的分布分数
的分布分数 与
与 关系如下图所示。下列说法正确的是
关系如下图所示。下列说法正确的是{分布分数
 }
}
A. |
B.曲线b代表 |
C.加水稀释,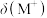 减小 减小 |
D.当 时, 时, 为含M粒子的主要存在形式 为含M粒子的主要存在形式 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】25℃时,向一定浓度的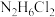 溶液中滴入
溶液中滴入 溶液,粒子浓度与混合溶液
溶液,粒子浓度与混合溶液 的变化关系如图所示。已知:肼在水中的电离方程式:
的变化关系如图所示。已知:肼在水中的电离方程式: ,
,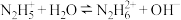 ;
; ,Y表示
,Y表示 或
或 )。下列叙述正确的是
)。下列叙述正确的是
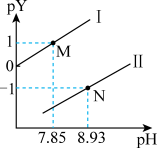
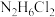 溶液中滴入
溶液中滴入 溶液,粒子浓度与混合溶液
溶液,粒子浓度与混合溶液 的变化关系如图所示。已知:肼在水中的电离方程式:
的变化关系如图所示。已知:肼在水中的电离方程式: ,
,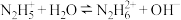 ;
; ,Y表示
,Y表示 或
或 )。下列叙述正确的是
)。下列叙述正确的是
A.曲线I表示 与 与 的变化关系 的变化关系 |
B. 的第一步电离的平衡常数的数量级为 的第一步电离的平衡常数的数量级为 |
C.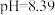 时, 时, |
D.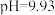 时, 时,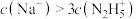 |
您最近一年使用:0次

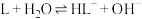
 。化合物L与
。化合物L与 形成配合物(
形成配合物(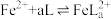 ),
),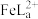 的浓度随
的浓度随 的投料百分比的变化如图所示(
的投料百分比的变化如图所示(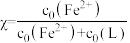 ,
, 表示初始浓度)。
表示初始浓度)。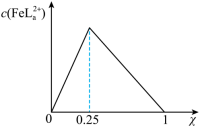
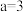
 的L溶液pH≈5
的L溶液pH≈5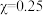 的溶液中,
的溶液中,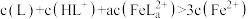
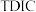 )是影响海洋生态稳定的重要指标,常温,不同
)是影响海洋生态稳定的重要指标,常温,不同 可形成珊瑚礁。下列说法中不正确的是
可形成珊瑚礁。下列说法中不正确的是
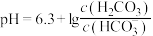

 时,海水中
时,海水中