 ,另含有少量Al)回收利用的工艺流程如图所示。
,另含有少量Al)回收利用的工艺流程如图所示。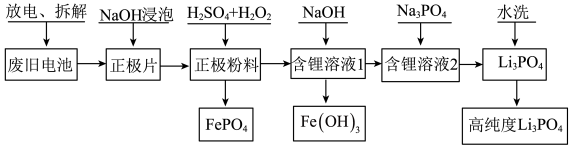
(1)
 中Fe元素的化合价为
中Fe元素的化合价为(2)拆解废旧磷酸铁锂电池会产生粉尘、废气等,采用
 溶液浸泡除去其中的Al,该过程发生的离子反应方程式为
溶液浸泡除去其中的Al,该过程发生的离子反应方程式为(3)正极粉料中加入“
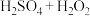 ”,其中
”,其中 的作用是
的作用是 代替
代替 不足之处是
不足之处是(4)常温下,
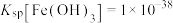 。向“含锂溶液1”中加入
。向“含锂溶液1”中加入 固体,进行深度除铁,使残留在溶液中的
固体,进行深度除铁,使残留在溶液中的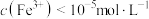 ,则应调节溶液的
,则应调节溶液的
(5)向“含锂溶液2”中加入
 溶液,得到
溶液,得到 沉淀,写出该过程发生的离子反应方程式
沉淀,写出该过程发生的离子反应方程式(6)工业上将
 、
、 粉碎与足量的炭黑混合高温灼烧制备
粉碎与足量的炭黑混合高温灼烧制备 ,同时产生CO,写出该反应的化学方程式
,同时产生CO,写出该反应的化学方程式相似题推荐
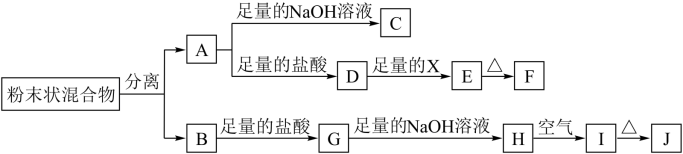
(1)写出下列物质的化学式:F
(2)分离粉末状混合物最简单的方法是
(3)D→E转化中,加入足量的X,试剂X可能是
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)A→C的离子方程式
(5)检验G溶液中的阳离子的方法

(1)写出下列物质的化学式。
A
(2)写出下列变化的化学方程式。
①A与NaOH溶液反应的化学方程式
②甲与NaOH溶液反应的离子方程式
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为
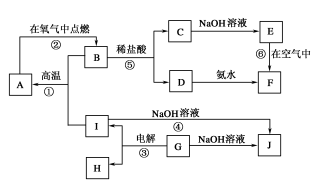
(1)I、G、J三种物质中所含同一种元素在周期表中的位置是
(2)写出反应④的离子方程式
(3)写出反应⑥的化学方程式
(4)写出反应③的电极反应式:阳极:
(5)从能量变化的角度看,①②③④反应中焓变ΔH<0的反应是
(6)A、B、C、D、E、F六种物质中所含同一种元素的电子排布式
 )广泛用于电镀、镍电池、催化剂等领域,从含有
)广泛用于电镀、镍电池、催化剂等领域,从含有 、
、 、
、 和
和 等杂质的粗
等杂质的粗 电镀废液中回收
电镀废液中回收 的流程如下图所示:
的流程如下图所示: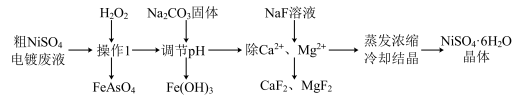
已知25℃时,
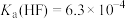 ,
,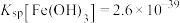 ,
,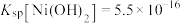 。
。请回答下列问题:
(1)
 中As元素的化合价为
中As元素的化合价为(2)“操作1”的名称是
 是一种无机弱酸,请写出加入
是一种无机弱酸,请写出加入 后生成
后生成 的离子方程式:
的离子方程式:(3)在25℃下,调节pH时,测得溶液中
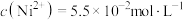 ,若需使c(Fe3+)≤2.6×10-6mol/L,则需控制溶液的pH范围为
,若需使c(Fe3+)≤2.6×10-6mol/L,则需控制溶液的pH范围为(4)除
 、
、 过程中,需控制溶液的
过程中,需控制溶液的 ,若pH过低,则
,若pH过低,则 、
、 的沉淀率会降低,原因是
的沉淀率会降低,原因是(5)实验室进行“蒸发浓缩”时所需的硅酸盐仪器包括:酒精灯、
(6)①在强碱性环境下,向
 溶液中加入NaClO溶液可制得镍电池的正极材料NiOOH,该过程中无污染性气体生成,则氧化剂与还原剂的物质的量之比为
溶液中加入NaClO溶液可制得镍电池的正极材料NiOOH,该过程中无污染性气体生成,则氧化剂与还原剂的物质的量之比为②镍氢电池以NiOOH电极为正极材料,储氢金属为负极材料,碱液(主要为KOH溶液)为电解质溶液,放电时的总反应为
 ,则NiOOH电极的反应式为
,则NiOOH电极的反应式为
已知:①酸浸时, FeTiO3转化为Fe2+和TiO2+;②本实验温度下,Ksp[Mg(OH)2]=1.0×10-11;请回答下列问题:
(1)酸浸时如何提高浸取速度和浸取率
(2)“水解”生成H2TiO3的离子方程式为
(3)“沉铁”过程中,气态产物的电子式为
(4)滤液3可用于制备Mg(OH)2。若滤液3中c(Mg2+)=1.0×10-3 mo/L,向其中加入NaOH固体,调整溶液pH值大于
(5)“电解”时,电解质为熔融的CaO,两电极材料为石墨棒。则
(6)测定铁红产品纯度:称取m g铁红,溶于一定量的硫酸之中,配成500.00 mL溶液。从其中量取20.00 mL溶液,加入过量的KI,充分反应后,用 c mol/L硫代硫酸钠(Na2S2O3)标准液滴定至终点,发生反应:I2+2S2O
 ===S4O
===S4O +2I-。平行滴定三次,硫代硫酸钠平均消耗体积为V mL。则铁红产品的纯度为
+2I-。平行滴定三次,硫代硫酸钠平均消耗体积为V mL。则铁红产品的纯度为 Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
Fe2O3及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示: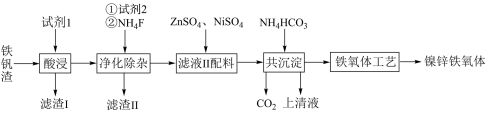
(1)试剂1是过量的
(2)试剂2为过量的铁粉,加入后可以观察的现象有
(3)NH4F溶液不能放入玻璃器皿中保存,理由是
(4)在Fe2+、Ni2+、Zn2+共沉淀过程中,若以Me代表Fe、Ni、Zn元素,则生成MeCO3•2Me(OH)2•H2O沉淀的化学方程式为
(5)按照上述流程,一座10万吨规模的炼铁厂每年产生铁矾渣约5万吨,Fe3+含量为44.8%,理论上每年至少可制备复合镍锌铁氧体(NiZnFe4O8,M=476 g • mol -1)
(6)滤液Ⅱ中加入的ZnSO4溶液,低温烘干后可得到皓矾(ZnSO4• 7H2O) 取28.70 g皓矾加热至不同温度,剩余固体的质量变化如图所示:

①100 °C时所得固体的化学式
②680 °C时所得固体的化学式为

本流程操作条件下,生成氢氧化物沉淀的pH如表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| 开始沉淀 的pH | 2.7 | 7.6 | 8.3 | 10.0 |
| 沉淀完全 的pH | 3.7 | 9.6 | 9.8 | 11.1 |
已知:Fe2+的氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+后生成Fe(OH)3沉淀除去。
请回答以下问题:
(1)步骤①中,为了加快酸溶速率,除了适当增加稀盐酸的浓度外,还可以采取的措施有
(2)步骤②中NaClO的电子式为
(3)常温时,Mg(OH)2的Ksp=1.8×10-11。当溶液pH=10.0时,溶液中的c(Mg2+)=
(4)若将步骤⑤中“稀盐酸”改为“加水、煮沸”的方式可以得到另一种沉淀物和一种无色无味的气体,请写出该反应的化学方程式:
(5)步骤⑥中涉及的操作是
【推荐2】钛铁铳矿可有效富集回收矿石中铁、钛、钪金属,获得铁精矿、钛精矿、钪精矿等主产品。从钛铁钪矿(主要成分有Sc2O3、FeTiO3、SiO2等)中制备草酸铳晶[Sc2(C2O4)3•5H2O]流程如下:
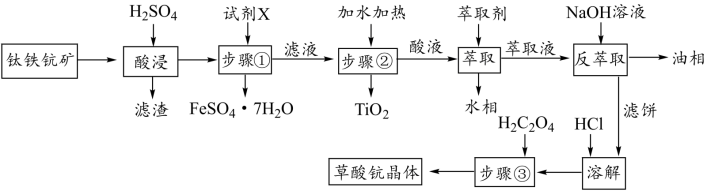
已知:①钪的萃取是根据协萃反应机理,利用P-204(磷酸二辛酯)[可用H2A2表示]和TBP(磷酸三辛酯)两种萃取剂,以煤油做萃取溶剂,将废酸中的钪以配位体形式萃取出来,经反萃取、提纯,从而得到高纯度的钪的氢氧化物。主要反应步骤由以下方程式表示萃取:Sc3++3H2A2+xH2O Sc(HA2)3•xH2O+3H+
Sc(HA2)3•xH2O+3H+
Sc(HA2)3•xH2O+xTBP Sc(HA2)3•xTBP+xH2O
Sc(HA2)3•xTBP+xH2O
②常温下Sc(OH)3的Ksp约为1.0×10-31
请回答下列问题:
(1)酸浸时为了提高酸浸速率,可采取的措施
(2)酸浸时“FeTiO3”溶解的离子方程式为
(3)步骤①的操作是浓缩、冷却、
(4)步骤②加大量的水稀释,同时加热的原因为
(5)“反萃取”的化学方程式为
(6)称取2.22g步骤③得到的草酸钪晶体[Sc2(C2O4)3•5H2O],在一定温度下加热得到0.69g固体,通过计算确定固体成分化学式为
(7)常温下,使0.1mol/LScCl3溶液中钪离子开始沉淀时的pH为
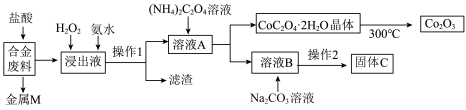
(1)金属M为
(2)加入H2O2的作用是(用离子方程式表示)
(3)充分焙烧的化学方程式为
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其原因是
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol・L-1 | 0.21 | 0.17 | 0.14 | 0.10 |

(1)操作Ⅰ的名称是
(2)检验FeCO3沉淀是否洗净的实验方法是
(3)加入NH4HCO3溶液的反应除了生成FeCO3沉淀,还会生成一种气体,生成气体的离子方程式为
(4)在空气中煅烧FeCO3的化学方程式是
(5)称取3.0 g 产品,用稀硫酸溶解,逐滴加入0.10 mol·L-1 KMnO4溶液20.00 mL,二者恰好反应完全。若此产品中只含有FeO、Fe2O3,求算产品中Fe2O3的质量分数,写出计算过程
(已知:10FeSO4+2KMnO4+8H2SO4===5Fe2(SO4)3+2MnSO4+K2SO4+8H2O)
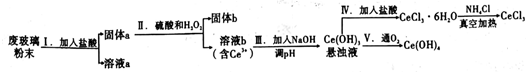
(1)步骤Ⅰ加入过量盐酸后,溶液a中的阳有离子
(2)步骤Ⅱ中反应的氧化剂和还原剂的物质的量之为
(3)为了使步骤Ⅲ所得悬浊液中的Ce3+浓度为1×10-6mol·L-1,则加入NaOH调节溶液的pH应为
(4)将NH4Cl固体与CeCl3·6H2O混合真空加热可得无水CeCl3,其中加入NH4Cl的作用是
(5)第Ⅴ步反应的化学方程式是
(6)对CeCl3样品纯度进行测定的方法:准确称取样品wg配成100mL溶液,取25.00mL置于锥形瓶中,加入稍过量的过二硫酸铵[(NH4)2S2O8]溶液将Ce3+氧化为Ce4+,然后用萃取剂[用(HT2)表示]萃取Ce4+,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点(其离子反应方程式为Ce4++Fe2+=Ce3++Fe3+),重复2~3次,平均消耗VmL标准溶液。
①“萃取”时存在反应:Ce4++n(HT)2
 Ce(H2n-4)+4H+,若要提高滴定的准确率,应使溶液呈
Ce(H2n-4)+4H+,若要提高滴定的准确率,应使溶液呈②经计算,CeCl3样品的纯度为

回答下列问题:
(1)有同学认为上述流程可以与氯碱工业联合。写出电解饱和食盐水制取次氯酸钠的化学方程式
(2)制备铁黄的离子方程式为
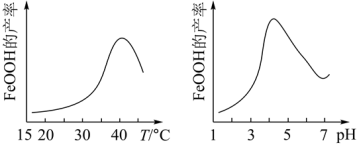
(3)用高铁酸钾作水处理剂除了可以对水体进行杀菌消毒之外,其还原产物氢氧化铁胶体还能吸附水中悬浮杂质,请写出用高铁酸钾除去水体中CN﹣的离子方程式
(4)已知:常温下,Ksp[Fe(OH)3]=4.0×10﹣38。高铁酸钾的净水能力与废水的pH有关,当溶液pH=2时,废水中c(Fe3+)=
(5)如果上述流程中,铁元素总利用率为75%。利用1L 2mol•L﹣1FeSO4溶液能制备纯度为90%的高铁酸钾



