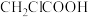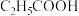Y、Z、W、M、Q是原子序数依次增大的前四周期元素,Z和M同主族,且两者的单质室温下均为气体;Q是在前四周期基态原子中未成对电子最多的元素。由上述元素中的四种组成的两种化合物的结构简式如图所示。

回答下列问题:
(1)基态Y原子的价电子排布式为_______ ,其中电子占据最高能级的电子云轮廓图为_______ 形。写出Q在周期表中的位置_______ 。
(2)W、M形成的一种化合物以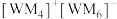 的形式存在,下列对
的形式存在,下列对 中心原子杂化方式推断合理的
中心原子杂化方式推断合理的_______ (填标号)。
a.sp2b.sp3c.sp3dd.sp3d2e.d2sp3
(3)W元素形成的一种白色单质易溶于CS2,难溶于水,可能原因是_______ 。
(4)与Q同周期且基态原子最外层电子数比Q多一个电子的主族元素为X,用电子式表示X与M形成化合物的过程_______ 。
(5)请列举一个证明Y与Z的非金属性强弱的事实_______ (用具体物质做答)

回答下列问题:
(1)基态Y原子的价电子排布式为
(2)W、M形成的一种化合物以
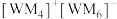 的形式存在,下列对
的形式存在,下列对 中心原子杂化方式推断合理的
中心原子杂化方式推断合理的a.sp2b.sp3c.sp3dd.sp3d2e.d2sp3
(3)W元素形成的一种白色单质易溶于CS2,难溶于水,可能原因是
(4)与Q同周期且基态原子最外层电子数比Q多一个电子的主族元素为X,用电子式表示X与M形成化合物的过程
(5)请列举一个证明Y与Z的非金属性强弱的事实
更新时间:2023-06-28 19:55:19
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W、R、P、Q是短周期主族元素,部分信息如下表所示:
(1)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为 _____ 。
(2)Z的单质与水反应的化学方程式是_____ ;R与Q两元素最高价氧化物水化物反应的离子方程式 _____ 。
(3)Y与R相比,非金属性较强的是_____ (用元素符号表示),下列事实能证明这一结论的是 _____ (填字母序号)。
a. 常温下Y的单质呈固态,R的单质呈气态
b. 稳定性XR>YX4
c. Y与R形成的化合物中Y呈正价
| X | Y | Z | W | R | P | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | -3,+5 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄 |
(2)Z的单质与水反应的化学方程式是
(3)Y与R相比,非金属性较强的是
a. 常温下Y的单质呈固态,R的单质呈气态
b. 稳定性XR>YX4
c. Y与R形成的化合物中Y呈正价
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,按要求回答问题。
(1)元素①~⑨中,金属性最强的元素是_______ (填元素符号)。
(2)元素③的原子结构示意图是_______ 。
(3)元素①和②可以形成多种化合物,其中是天然气主要成分的化合物的电子式是_______ ,比该化合物多一个碳原子的同系物的结构简式是_______ 。
(4)元素⑦、⑧、⑨的最高价氧化物对应的水化物的酸性由强到弱的顺序是_______ (填化学式)。
(5)下列可以判断元素④和⑨非金属性强弱的是_______(填序号)。
(6)元素⑧的氢化物水溶液中通入少量元素⑨的单质,发生了置换反应,有淡黄色沉淀生成,该反应的化学方程式是_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)元素③的原子结构示意图是
(3)元素①和②可以形成多种化合物,其中是天然气主要成分的化合物的电子式是
(4)元素⑦、⑧、⑨的最高价氧化物对应的水化物的酸性由强到弱的顺序是
(5)下列可以判断元素④和⑨非金属性强弱的是_______(填序号)。
| A.单质的熔点④比⑨低 |
| B.单质与氢气反应④比⑨剧烈 |
| C.气态氢化物稳定性④比⑨强 |
| D.单质的密度④比⑨小 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有四种短周期元素,它们的结构、性质等信息如表所述:
(1)X元素在周期表中的位置_____ ;其相对分子质量最小的气态氢化物常用作_____ 。
(2)用电子式表示X最高价氧化物的形成过程_____________________ 。
(3)Y的最高价氧化物对应水化物的电子式________ 。
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式为______________ 。
(5)举出实例说明M的非金属性比X强:_____________ 。
元素 | 结构、性质等信息 |
X | 构成有机物的核心元素,该元素的一种氧化物和气态氢化物都是典型的温室气体 |
Y | 短周期中(除稀有气体外)原子半径最大的元素,该单质与冷水剧烈反应 |
Z | 与Y同周期,其最高价氧化物的水化物呈两性 |
M | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒剂和杀菌剂 |
(2)用电子式表示X最高价氧化物的形成过程
(3)Y的最高价氧化物对应水化物的电子式
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式为
(5)举出实例说明M的非金属性比X强:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】Ⅰ.下列8种化学符号: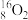 、
、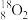 、
、 、
、 、
、 、
、 、
、 、
、
(1)表示核素的符号共_______ 种。
(2)互为同位素的是_______ 。
(3)质量相同的H216O和D216O所含中子数之比为_______ 。
请回答下列问题:
(4)Y在元素周期表中的位置是_______ 。
(5)X、Z两种元素的气态氢化物稳定性由强到弱的顺序为:_______ 。(化学式表示)
(6)Z、W两种元素的最高价氧化物对应水化物的酸性由强到弱的的顺序为:_______ (用化学式表示)
(7)下列说法能比较出Y与同族的短周期元素Q非金属性强弱的是:_______。
(8)P是W的同族元素,其最高价氧化物可用于制造光导纤维,写出P最高价氧化物与NaOH溶液反应的离子方程式:_______ 。
(9)用电子式表示WY2的形成过程:_______ 。
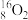 、
、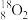 、
、 、
、 、
、 、
、 、
、 、
、
(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
Ⅱ.短周期元素X、Y、Z、W在周期表中的相对位置如下图所示,其中W元素的原子结构示意图为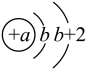 。
。
W | X | Y |
Z |
请回答下列问题:
(4)Y在元素周期表中的位置是
(5)X、Z两种元素的气态氢化物稳定性由强到弱的顺序为:
(6)Z、W两种元素的最高价氧化物对应水化物的酸性由强到弱的的顺序为:
(7)下列说法能比较出Y与同族的短周期元素Q非金属性强弱的是:_______。
| A.Y单质与Q单质发生置换反应 |
| B.Y与Q最高价氧化物对应的水化物的酸性 |
| C.Y、Q形成的化合物中两元素的化合价 |
| D.Y、Q的最简单气态氢化物的沸点 |
(8)P是W的同族元素,其最高价氧化物可用于制造光导纤维,写出P最高价氧化物与NaOH溶液反应的离子方程式:
(9)用电子式表示WY2的形成过程:
您最近一年使用:0次
【推荐2】A、B、C、D均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属 元素。A是形成化合物种类最多的元素;B原子基态电子排布中只有一个未成对电子;C是同周期元素中原子半径最小的元素;D的基态原子在前四周期元素的基态原子中单电子数最多;回答下列问题(相关回答均用元素符号表示):
(1)D的基态原子的核外电子排布式是_____ 。
(2)B的氢化物的沸点比C的氢化物的沸点___________ (填“高”或“低”),原因是______ 。
(3)A的电负性______ (填“大于”或“小于”)C的电负性,A与C形成的化合物的电子式_________ 。
(1)D的基态原子的核外电子排布式是
(2)B的氢化物的沸点比C的氢化物的沸点
(3)A的电负性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体,C和D两种元素按个数比l:l形成的化合物M,A和C两种元素按个数比2:1形成化合物N,请回答下列问题:
(1)写出F在周期表中的位置_______ ,画出D的离子结构示意图_________ 。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为________ 。
(3)C与F形成的常见化合物属于_______ 化合物(填“共价”或“离子”)。
(4)画出B单质的结构式_________ ,科学家合成出了B元素形成的B 电子式
电子式 ,则n值为
,则n值为__________ 。
(5)化合物M属于_______ 化合物(填“共价”或“离子”),如何证明?___________ ,用电子式表示其形成过程______________ 。
(6)化合物M和化合物N反应的化学方程式:________________ 。
(1)写出F在周期表中的位置
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为
(3)C与F形成的常见化合物属于
(4)画出B单质的结构式
 电子式
电子式 ,则n值为
,则n值为(5)化合物M属于
(6)化合物M和化合物N反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硼镍镧合金具有很强的储氢能力。
(1)用价层电子对互斥理论推测三氟化硼分子的立体构型为______ ,硼原子的杂化类型为_____ 。
(2)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。如图是磷化硼晶体的晶胞示意图,已知该晶胞的棱长为516pm,最近的B和P原子之间的距离为____ pm。该晶体的晶体类型是________ 。


(3)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如上图)。
①1molH3BO3的晶体中有_____ mol氢键。
②硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2O,它电离生成少量[B(OH)4]-和H+,则硼酸为_______ 元酸,[B(OH)4]-含有的化学键类型为_______ 。
(4)镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构,其中铜钙合金的结构单元如图所示。试回答下列问题:

①在元素周期表中Ca 位于______ 区。
②铜原子的基态原子核外电子排布式__________ 。
③已知镧镍合金LaNin晶胞体积为9.0×10-23cm,储氢后形成LaNinH4.5的合金(氢进入晶胞空隙,体积不变),则LaNin中,n=_____ (填数值);氢在合金中的密度为_____ (保留两位有效数字)。
(1)用价层电子对互斥理论推测三氟化硼分子的立体构型为
(2)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。如图是磷化硼晶体的晶胞示意图,已知该晶胞的棱长为516pm,最近的B和P原子之间的距离为


(3)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如上图)。
①1molH3BO3的晶体中有
②硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2O,它电离生成少量[B(OH)4]-和H+,则硼酸为
(4)镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构,其中铜钙合金的结构单元如图所示。试回答下列问题:

①在元素周期表中Ca 位于
②铜原子的基态原子核外电子排布式
③已知镧镍合金LaNin晶胞体积为9.0×10-23cm,储氢后形成LaNinH4.5的合金(氢进入晶胞空隙,体积不变),则LaNin中,n=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
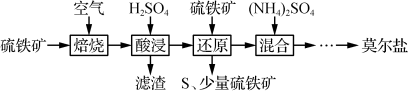
【推荐2】硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]又称莫尔盐,是一种浅绿色晶体。用硫铁矿(主要含FeS2、SiO2等)制备莫尔盐的流程如图:___________ (写两种即可)。
(2)“酸浸”时,滤渣的主要成分是___________ (写化学式)。
(3)“焙烧”时发生的主要是FeS2与O2反应生成Fe2O3和SO2,写出该反应的化学方程式_______ 。“酸浸”时发生的主要反应的离子方程式为___________ 。
(4)写出基态Fe3+核外电子排布式___________ 。
(5)证明所得莫尔盐晶体中含有 的实验方法是:取少许晶体置于试管中,溶解,
的实验方法是:取少许晶体置于试管中,溶解,__________ ,证明含有 。
。
(2)“酸浸”时,滤渣的主要成分是
(3)“焙烧”时发生的主要是FeS2与O2反应生成Fe2O3和SO2,写出该反应的化学方程式
(4)写出基态Fe3+核外电子排布式
(5)证明所得莫尔盐晶体中含有
 的实验方法是:取少许晶体置于试管中,溶解,
的实验方法是:取少许晶体置于试管中,溶解, 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】有研究团队通过光催化还原 ,将其合成一碳化合物(CO、HCOOH、
,将其合成一碳化合物(CO、HCOOH、 、
、 等)。常见的无机非贵金属光催化还原
等)。常见的无机非贵金属光催化还原 的催化剂有NiO、CuO、
的催化剂有NiO、CuO、 、
、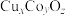 等。回答下列问题:
等。回答下列问题:
(1)CO可与金属镍形成四面体构型分子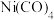 ,其中
,其中 的价电子排布式为
的价电子排布式为___________ 。该催化 还原的过程中可能产生
还原的过程中可能产生 ,该离子的VSEPR模型为
,该离子的VSEPR模型为___________ 。铁也可以与CO形成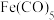 金属羰基化合物,
金属羰基化合物, 分子中含有
分子中含有___________  键。
键。
(2)镍能形成多种配合物,如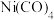 、
、 、
、 等,下列有关说法正确的是___________(填选项字母)。
等,下列有关说法正确的是___________(填选项字母)。
(3)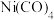 是无色液体,沸点42.1℃,熔点
是无色液体,沸点42.1℃,熔点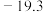 ℃,难溶于水,易溶于有机溶剂,那么固体
℃,难溶于水,易溶于有机溶剂,那么固体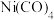 属于
属于___________ 晶体。金属Ni可以与Mg、C形成一种化合物M,M是一种新型超导体,它的临界温度为8K。已知M的晶胞结构如下图所示,则M的化学式为___________ 。

 ,将其合成一碳化合物(CO、HCOOH、
,将其合成一碳化合物(CO、HCOOH、 、
、 等)。常见的无机非贵金属光催化还原
等)。常见的无机非贵金属光催化还原 的催化剂有NiO、CuO、
的催化剂有NiO、CuO、 、
、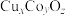 等。回答下列问题:
等。回答下列问题:(1)CO可与金属镍形成四面体构型分子
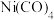 ,其中
,其中 的价电子排布式为
的价电子排布式为 还原的过程中可能产生
还原的过程中可能产生 ,该离子的VSEPR模型为
,该离子的VSEPR模型为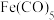 金属羰基化合物,
金属羰基化合物, 分子中含有
分子中含有 键。
键。(2)镍能形成多种配合物,如
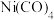 、
、 、
、 等,下列有关说法正确的是___________(填选项字母)。
等,下列有关说法正确的是___________(填选项字母)。A. 中含有共价键和离子键 中含有共价键和离子键 |
B.CO与 互为等电子体,其中CO分子内 互为等电子体,其中CO分子内 键和 键和 键的个数比为 键的个数比为 |
C. 中N原子为 中N原子为 杂化,其空间构型为正四面体形 杂化,其空间构型为正四面体形 |
D. 在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为6 在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为6 |
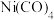 是无色液体,沸点42.1℃,熔点
是无色液体,沸点42.1℃,熔点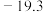 ℃,难溶于水,易溶于有机溶剂,那么固体
℃,难溶于水,易溶于有机溶剂,那么固体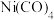 属于
属于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】从物质结构的视角认识乙酸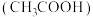 。按要求回答下列问题。
。按要求回答下列问题。
(1)组成乙酸的元素中位于周期表p区的元素有_________ 。
(2)乙酸的官能团名称为_________ ;官能团中碳原子的杂化轨道类型为_________ 。
(3)1个 分子中,含有
分子中,含有_________ 个 键,
键,_________ 个 键;共平面的原子最多有
键;共平面的原子最多有_________ 个。
(4)推测乙酸的熔点比十八酸 的
的______ (填“高”“低”“相当”),其理由是____ 。
(5)不同羧酸 时的
时的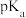 (即
(即 )如表所示:
)如表所示:
①对比表中已知数据,从分子组成与结构角度,写出所得结论(2条):________ 、_________ 。
②写出乙酸的电离方程式:______ 。写出一例能说明乙酸的酸性强于碳酸的离子方程式:______ 。
(6)写出含有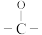 的乙酸的同分异构体的结构简式:
的乙酸的同分异构体的结构简式:_______ 。
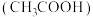 。按要求回答下列问题。
。按要求回答下列问题。(1)组成乙酸的元素中位于周期表p区的元素有
(2)乙酸的官能团名称为
(3)1个
 分子中,含有
分子中,含有 键,
键, 键;共平面的原子最多有
键;共平面的原子最多有(4)推测乙酸的熔点比十八酸
 的
的(5)不同羧酸
 时的
时的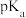 (即
(即 )如表所示:
)如表所示:羧酸 |
| 羧酸 |
|
甲酸( | 3.75 | 氯乙酸( | 2.86 |
乙酸( | 4.76 | 二氯乙酸( | 1.29 |
丙酸( | 4.88 | 三氯乙酸( | 0.65 |
①对比表中已知数据,从分子组成与结构角度,写出所得结论(2条):
②写出乙酸的电离方程式:
(6)写出含有
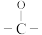 的乙酸的同分异构体的结构简式:
的乙酸的同分异构体的结构简式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】我国科学家开发了一类新型碱(土)金属钌基三元氢化物催化剂,实现了温和条件下氨的催化合成。碱土金属在化学中有着诸多应用。
(1)Ba2RuH6可作为合成氨的催化剂,Ba的价电子排布式为_______ ,氨气是一种重要的化工原料,氨气的VSEPR模型为_______ ,其极易溶于水的原因有:氨气能与水反应、________ 、_________ 。
(2)气态BeCl2可以形成一种二聚分子,其结构如图甲所示,Be的杂化类型为________ ,在图中用“→”表示出配位键。MgCl2的沸点远高于BeCl2,其原因是________ 。

(3)Ca和Cu可以形成一种合金,其晶体结构如图乙所示,该合金的化学式为________ ,若晶体底面边长为apm,高为bpm,Ca和Cu的半径分别为mpm、npm,则该合金的空间利用率为______ (列出计算表达式)。
(1)Ba2RuH6可作为合成氨的催化剂,Ba的价电子排布式为
(2)气态BeCl2可以形成一种二聚分子,其结构如图甲所示,Be的杂化类型为

(3)Ca和Cu可以形成一种合金,其晶体结构如图乙所示,该合金的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】碳族元素的单质和化合物在化工、医药、材料等领域有着广泛的应用。
(1)锗是重要半导体材料,基态Ge原子中,核外电子占据的最高能级是___________ ,该能级的电子云轮廓图为___________ 。Ge与C同族,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键,从原子结构角度分析,原因是_______________________________ 。
(2) 是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。
是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。

① 分子中C原子和S原子的杂化轨道类型分别为
分子中C原子和S原子的杂化轨道类型分别为_______________ 。
②测得 中碳硫键的键长介于C─S和C=S之间,其原因可能是
中碳硫键的键长介于C─S和C=S之间,其原因可能是_______________ 。
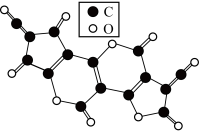
(3)X是碳的一种氧化物,X的五聚合体结构如图所示。X分子中每个原子都满足最外层8电子结构,X分子的电子式为___________ 。X分子中碳碳键的夹角为___________ 。
(4)有机卤化铅晶体具有独特的光电性能,图为其晶胞结构示意图。
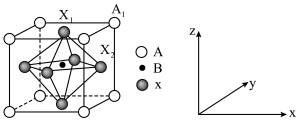
A为 ,B为
,B为 ,X为
,X为
①若该晶胞的边长为a ,则最近的两个
,则最近的两个 中心间的距离是
中心间的距离是__________ 。
②在该晶胞的另一种表达方式中,若图中 处于顶点位置,则
处于顶点位置,则 处于
处于__________ 位置。原子坐标参数B为 ;
; 为
为 ,则
,则 为
为__________ 。
(1)锗是重要半导体材料,基态Ge原子中,核外电子占据的最高能级是
(2)
 是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。
是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。
①
 分子中C原子和S原子的杂化轨道类型分别为
分子中C原子和S原子的杂化轨道类型分别为②测得
 中碳硫键的键长介于C─S和C=S之间,其原因可能是
中碳硫键的键长介于C─S和C=S之间,其原因可能是(3)X是碳的一种氧化物,X的五聚合体结构如图所示。X分子中每个原子都满足最外层8电子结构,X分子的电子式为

(4)有机卤化铅晶体具有独特的光电性能,图为其晶胞结构示意图。

A为
 ,B为
,B为 ,X为
,X为
①若该晶胞的边长为a
 ,则最近的两个
,则最近的两个 中心间的距离是
中心间的距离是②在该晶胞的另一种表达方式中,若图中
 处于顶点位置,则
处于顶点位置,则 处于
处于 ;
; 为
为 ,则
,则 为
为
您最近一年使用:0次