我国科学家发现一种钒配合物Ⅰ可以充当固氮反应的催化剂,反应过程中经历的中间体包括Ⅱ和Ⅲ。
(1)配合物Ⅰ中钒的配位原子有4种,它们是_______ 。
(2)配合物Ⅰ中,R′代表芳基, 空间结构呈角形,原因是
空间结构呈角形,原因是_______ 。
(3)配合物Ⅱ中,第一电离能最大的配位原子是_______ 。
(4)配合物Ⅱ和Ⅲ中,钒的化合价分别为 和
和 ,配合物Ⅱ、Ⅲ和
,配合物Ⅱ、Ⅲ和 三者中,两个氮原子间键长最长的是
三者中,两个氮原子间键长最长的是_______ 。
(5)近年来,研究人员发现含钒的锑化物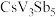 在超导方面表现出潜在的应用前景。
在超导方面表现出潜在的应用前景。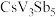 晶胞如图1所示,晶体中包含由V和Sb组成的二维平面(见图2)。
晶胞如图1所示,晶体中包含由V和Sb组成的二维平面(见图2)。_______ 。锑和磷同族,锑原子基态的价层电子排布式为_______ 。
②晶体中少部分钒原子被其它元素(包括Ti、Nb、Cr、Sn)原子取代,可得到改性材料。下列有关替代原子说法正确的是_______ 。
a.有 或
或 价态形式 b.均属于第四周期元素
价态形式 b.均属于第四周期元素
c.均属于过渡元素 d.替代原子与原离子的离子半径相近
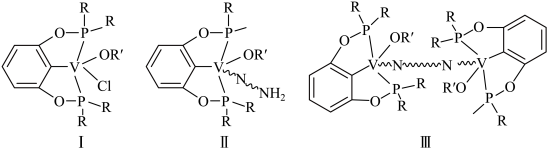
( 代表单键、双键或叁键)
代表单键、双键或叁键)
(1)配合物Ⅰ中钒的配位原子有4种,它们是
(2)配合物Ⅰ中,R′代表芳基,
 空间结构呈角形,原因是
空间结构呈角形,原因是(3)配合物Ⅱ中,第一电离能最大的配位原子是
(4)配合物Ⅱ和Ⅲ中,钒的化合价分别为
 和
和 ,配合物Ⅱ、Ⅲ和
,配合物Ⅱ、Ⅲ和 三者中,两个氮原子间键长最长的是
三者中,两个氮原子间键长最长的是(5)近年来,研究人员发现含钒的锑化物
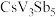 在超导方面表现出潜在的应用前景。
在超导方面表现出潜在的应用前景。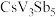 晶胞如图1所示,晶体中包含由V和Sb组成的二维平面(见图2)。
晶胞如图1所示,晶体中包含由V和Sb组成的二维平面(见图2)。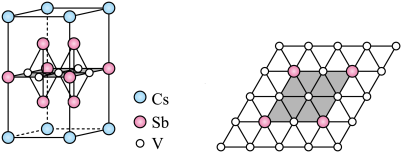
②晶体中少部分钒原子被其它元素(包括Ti、Nb、Cr、Sn)原子取代,可得到改性材料。下列有关替代原子说法正确的是
a.有
 或
或 价态形式 b.均属于第四周期元素
价态形式 b.均属于第四周期元素c.均属于过渡元素 d.替代原子与原离子的离子半径相近
更新时间:2023-08-03 19:35:17
|
相似题推荐
解答题-结构与性质
|
困难
(0.15)
名校
【推荐1】【化学选修3-物质结构与性质】a、b、c、d、e均为周期表前四周期元素,原子序数依次增大,相关信息如下表所示。
请回答:
(1)d属于________ 区的元素,其基态原子的价电子排布图为_________ 。
(2)b与其同周期相邻元素第一电离能由大到小的顺序为________ (用元素符号表示)。
(3)c的氢化物水溶液中存在的氢键有________ 种,任意画出一种________ 。
(4)a与其相邻同主族元素的最高价氧化物的熔点高低顺序为________ (用化学式表示)。若将a元素最高价氧化物水化物对应的正盐酸根离子表示为A,则A的空间构型为________ ;A的中心原子的轨道杂化类型为________ ;与A互为等电子体的一种分子为________ (填化学式)。
(5)e与Au的合金可形成面心立方最密堆积的晶体,在晶胞中e原子处于面心,该晶体具有储氢功能,氢原子可进入到由e原子与Au原子构成的四面体空隙中,储氢后的晶胞结构与金刚石晶胞结构相似,该晶体储氢后的化学式为________ ,若该晶体的相对分子质量为M,密度为ag/cm ,则晶胞的体积为
,则晶胞的体积为________ ( 用表示阿伏加德罗常数的值)。
用表示阿伏加德罗常数的值)。
| a | 原子核外电子分别占3个不同能级,且每个能级上排布的电子数相同 |
| b | 基态原子的p轨道电子数比s轨道电子数少1 |
| c | 在周期表所列元素中电负性最大 |
| d | 位于周期表中第4纵行 |
| e | 基态原子M层全充满,N层只有一个电子 |
(1)d属于
(2)b与其同周期相邻元素第一电离能由大到小的顺序为
(3)c的氢化物水溶液中存在的氢键有
(4)a与其相邻同主族元素的最高价氧化物的熔点高低顺序为
(5)e与Au的合金可形成面心立方最密堆积的晶体,在晶胞中e原子处于面心,该晶体具有储氢功能,氢原子可进入到由e原子与Au原子构成的四面体空隙中,储氢后的晶胞结构与金刚石晶胞结构相似,该晶体储氢后的化学式为
 ,则晶胞的体积为
,则晶胞的体积为 用表示阿伏加德罗常数的值)。
用表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
名校
解题方法
【推荐2】银离子导体是发现最早的固体电解质,同时也是应用面最广的固体电解质,如制作库仑计、电子开关、压敏元件、气敏传感器、记忆元件、电容器等电化学器件。
回答以下问题:
(1)Ag+的价层电子排布式为4d10,写出Ag在周期表中的位置___ 。
(2)第三周期各元素的氯化物熔点、沸点数据如下:
请解释第三周期氯化物沸点从左到右变化的原因:___ 。
(3)偏高碘酸HIO4是无机非混合酸中氧化性极强的酸之一,可将Mn氧化为HMnO4,将Fe2+氧化为H2FeO4。HIO4的中心原子杂化形式是__ ,构成HIO4的三种元素电负性大小顺序是___ ,在HIO4晶体中存在___ (填字母)
A.离子键 B.极性共价键 C.非极性共价键 D.分子间作用力 E.σ键 F.π键
(4)室温下,AgI属于六方ZnS结构,其中S原子作六方密堆积,Zn原子填充在半数的四面体空隙中。则AgI晶体中I原子的配位数是___ 。
(5)400℃以上AgI固体的导电能力是室温的上万倍,可与电解质溶液媲美,经研究发现其在146℃以上转化为一种奇特结构:α—AgI,I-作体心立方堆积,而Ag+则选择性填入I-构成的三类孔隙中:八面体孔隙(O)、四面体孔隙(T)和三角形孔隙(Tr),则平均每个α—AgI晶胞中的Ag+数是___ ,I-与I-构成的三类孔隙堆积之比为I-:O:T:Tr=1:__ :__ :12。

回答以下问题:
(1)Ag+的价层电子排布式为4d10,写出Ag在周期表中的位置
(2)第三周期各元素的氯化物熔点、沸点数据如下:
| NaCl | MgCl2 | AlCl3 | SiCl4 | PCl3 | S2Cl2 | |
| 熔点/K | 1074 | 987 | 465 | 205 | 181 | 193 |
| 沸点/K | 1686 | 1691 | 453(升华) | 216 | 349 | 411 |
请解释第三周期氯化物沸点从左到右变化的原因:
(3)偏高碘酸HIO4是无机非混合酸中氧化性极强的酸之一,可将Mn氧化为HMnO4,将Fe2+氧化为H2FeO4。HIO4的中心原子杂化形式是
A.离子键 B.极性共价键 C.非极性共价键 D.分子间作用力 E.σ键 F.π键
(4)室温下,AgI属于六方ZnS结构,其中S原子作六方密堆积,Zn原子填充在半数的四面体空隙中。则AgI晶体中I原子的配位数是
(5)400℃以上AgI固体的导电能力是室温的上万倍,可与电解质溶液媲美,经研究发现其在146℃以上转化为一种奇特结构:α—AgI,I-作体心立方堆积,而Ag+则选择性填入I-构成的三类孔隙中:八面体孔隙(O)、四面体孔隙(T)和三角形孔隙(Tr),则平均每个α—AgI晶胞中的Ag+数是

您最近一年使用:0次
【推荐3】氮、磷、砷、铁、钛等元素及其化合物在现代农业、科技和国防建设中有着许多独特的用途。
I.如LiFePO4是新型锂离子电池的电极材料,可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。
(1)Fe2+核外电子排布式为___________ ,NH4H2PO4中,除氢元素外,其余三种元素第一电离能最大的是___________ (填元素符号)。
(2)苯胺(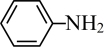 )和NH4H2PO4中的N原子杂化方式分别为
)和NH4H2PO4中的N原子杂化方式分别为___________ 。
(3)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是___________ 。
II.(4)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiC136H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________ 。
(5)氮化钛熔点高,硬度大,具有典型的NaCl型晶体结构,其晶胞结构如图所示。
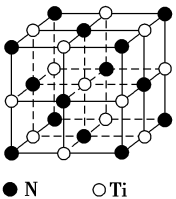
①设氮化钛晶体中Ti原子与跟它最邻近的N原子之间的距离为r,则与该Ti原子最邻近的Ti的数目为___________ 。Ti 原子与跟它次邻近的N原子之间的距离为___________ 。
②已知在氮化钛晶体中Ti原子的半径为apm,N原子的半径为bpm,它们在晶体中是紧密接触的,则在氮化钛晶体中原子的空间利用率为___________ 。(用a、b表示)
III.(6)从磷钇矿中可提取稀土元素钇(Y),某磷钇矿的晶胞如图所示,该磷钇矿的化学式为___________ 。
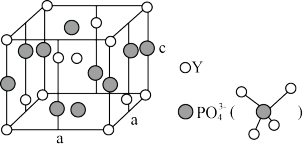
(7)已知晶胞参数为anm和cnm,阿伏加德罗常数的值为NA,则该磷钇矿的ρ为___________ 。g·cm-3 (列出计算式,用a、c表示)
I.如LiFePO4是新型锂离子电池的电极材料,可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。
(1)Fe2+核外电子排布式为
(2)苯胺(
 )和NH4H2PO4中的N原子杂化方式分别为
)和NH4H2PO4中的N原子杂化方式分别为(3)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是
II.(4)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiC136H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为
(5)氮化钛熔点高,硬度大,具有典型的NaCl型晶体结构,其晶胞结构如图所示。

①设氮化钛晶体中Ti原子与跟它最邻近的N原子之间的距离为r,则与该Ti原子最邻近的Ti的数目为
②已知在氮化钛晶体中Ti原子的半径为apm,N原子的半径为bpm,它们在晶体中是紧密接触的,则在氮化钛晶体中原子的空间利用率为
III.(6)从磷钇矿中可提取稀土元素钇(Y),某磷钇矿的晶胞如图所示,该磷钇矿的化学式为

(7)已知晶胞参数为anm和cnm,阿伏加德罗常数的值为NA,则该磷钇矿的ρ为
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐1】铜铟镓硒薄膜太阳能电池(GIGS)是第三代太阳能电池的典型代表,已成为全球光伏领域研究的热点之一,回答下列问题:
(1)镓(Ga)价电子排布式为______ ,镓(Ga)与铟(In)同主族第一电离能较小的为______ (用元素符号表示)。
(2)硒属于_______ 区元素。O、S、Se简单氢化物稳定性由强到弱的顺序为______ ,中心原子的杂化方式为___________ ,键角最大的是_____________ 。
(3)已知N-N、N=N键能之比为l:4.9,而C-C、C=C键能之比为1:2.34。则N2和C2H2中叁键能较大的是__________ (填化学式)。
(4)某晶体的晶胞结构如图所示(在该晶体中通过掺入适量的Ga以替代部分In就可以形GIGS晶体),该晶体的化学式为__________ 。

图中A原子和B原子坐标(分别为(0,0,0),(0,0, ),则C原子坐标为
),则C原子坐标为_________ 。
(1)镓(Ga)价电子排布式为
(2)硒属于
(3)已知N-N、N=N键能之比为l:4.9,而C-C、C=C键能之比为1:2.34。则N2和C2H2中叁键能较大的是
(4)某晶体的晶胞结构如图所示(在该晶体中通过掺入适量的Ga以替代部分In就可以形GIGS晶体),该晶体的化学式为

图中A原子和B原子坐标(分别为(0,0,0),(0,0,
 ),则C原子坐标为
),则C原子坐标为
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
名校
解题方法
【推荐2】商务部、海关总署在官网发布公告称,决定对镓、锗相关物项实施出口管制。锗,天然的优良半导体,在光纤通信、红外光学、太阳能电池、核物理探测等领域应用颇多。工业上利用锗锌矿(主要成分为GeO2和ZnS,还含少量Fe2O3 )来制备高纯度锗的流程如图。
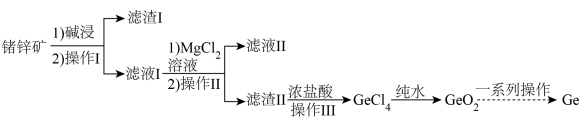
已知:①GeCl4的熔点为-49.5℃ ,沸点为84℃,其在水中或酸的稀溶液中易水解。
②GeO2可溶于强碱溶液,生成锗酸盐。
(1)在元素周期表中,Ge、As、Se位于同一周期,则基态原子的第一电离能由大到小的顺序是________ 。
(2)硅和锗与氯元素都能形成氯化物RCL(R代表Si和Ge),从原子结构角度解释原因:___ 。
(3)“滤渣II”中除含有MgGeO3外,还含有少量____________ (填化学式)。
(4)GeCl4中加水反应的离子方程式是______________ 。
(5)固态GeCl4为_______ 晶体,“操作III”分离获得GeCl4所使用的装置为________ (填标号)。
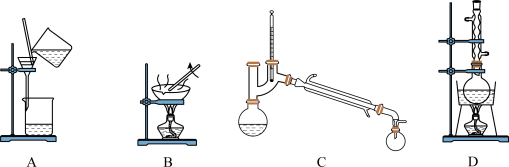
根据选择,提出改进的方法:_________ (若不需要改进,此空填“不需要")。
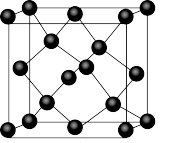
(6)Ge单晶的晶胞结构类似于金刚石,如图。已知Ge单晶的晶胞边长为a pm,设NA为阿伏加德罗常数的值,Ge单晶的密度为______ g·cm-3。

已知:①GeCl4的熔点为-49.5℃ ,沸点为84℃,其在水中或酸的稀溶液中易水解。
②GeO2可溶于强碱溶液,生成锗酸盐。
(1)在元素周期表中,Ge、As、Se位于同一周期,则基态原子的第一电离能由大到小的顺序是
(2)硅和锗与氯元素都能形成氯化物RCL(R代表Si和Ge),从原子结构角度解释原因:
(3)“滤渣II”中除含有MgGeO3外,还含有少量
(4)GeCl4中加水反应的离子方程式是
(5)固态GeCl4为

根据选择,提出改进的方法:
(6)Ge单晶的晶胞结构类似于金刚石,如图。已知Ge单晶的晶胞边长为a pm,设NA为阿伏加德罗常数的值,Ge单晶的密度为

您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
名校
【推荐3】氧元素为地壳中含量最高的元素,可形成多种重要的单质和化合物。
(1)氧元素位于元素周期表中_______ 区;第二周期元素中,第一电离能比氧大的有_______ 种。
(2)O3可用于消毒。O3的中心原子的杂化形式为_______ ;其分子的VSEPR模型为_______ ,与其互为等电子体的离子为_______ (写出一种即可)。
(3)含氧有机物中,氧原子的成键方式不同会导致有机物性质不同。解释C2H5OH的沸点高于CH3OCH3的原因为_______ 。
(4)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。
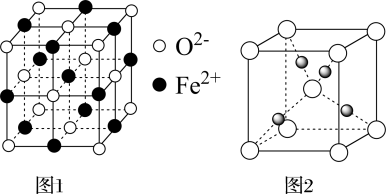
①FeO立方晶胞结构如图1所示,则Fe2+的配位数为_______ ;与O2-紧邻的所有Fe2+构成的几何构型为_______ 。
②Cu2O立方晶胞结构如图2所示,若O2-与Cu+之间最近距离为a pm,则该晶体的密度为_______ g·cm-3。(用含a、NA的代数式表示,NA代表阿伏加德罗常数的值)
(1)氧元素位于元素周期表中
(2)O3可用于消毒。O3的中心原子的杂化形式为
(3)含氧有机物中,氧原子的成键方式不同会导致有机物性质不同。解释C2H5OH的沸点高于CH3OCH3的原因为
(4)氧元素可分别与Fe和Cu形成低价态氧化物FeO和Cu2O。

①FeO立方晶胞结构如图1所示,则Fe2+的配位数为
②Cu2O立方晶胞结构如图2所示,若O2-与Cu+之间最近距离为a pm,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐1】物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_____ 种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_____ 。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是_____ ,1mol(C2H5O)3P=O分子中含有的σ键的数目为_____ 。
(4)已知固态NH3、H2O、HF的氢键键能和结构如图1:
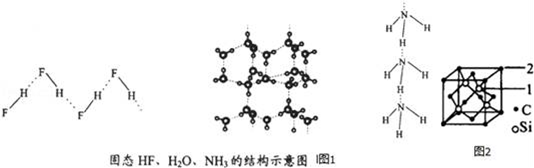
解释H2O、HF、NH3沸点依次降低的原因_____ 。
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有_____ 个,与碳原子等距离最近的碳原子有_____ 个。已知碳化硅晶胞边长为apm,则晶胞图2中1号硅原子和2号碳原子之间的距离为_____ pm,碳化硅的密度为_____ g/cm3。
(1)第二周期中,元素的第一电离能处于B与N之间的元素有
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是
(4)已知固态NH3、H2O、HF的氢键键能和结构如图1:
| 物质 | 氢键X﹣H…Y | 键能kJ.mol﹣1 |
| (HF)n | D﹣H…F | 28.1 |
| 冰 | O﹣H…O | 18.8 |
| (NH3)n | N﹣H…N | 5.4 |

解释H2O、HF、NH3沸点依次降低的原因
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
【推荐2】锂离子电池能够成为产业发展方向,主要基于其拥有较高的能量重量比和能量体积比等多项特性,正极材料为钴酸锂、锰酸锂和磷酸亚铁锂材料等。
(1)工业上用 、
、 、LiCl及苯胺(
、LiCl及苯胺(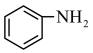 )为原料制备磷酸亚铁锂。基态Cl原子价电子的轨道表示式为
)为原料制备磷酸亚铁锂。基态Cl原子价电子的轨道表示式为_______ ,其在元素周期表中的位置为_______ ,O、N、P的电负性由大到小的顺序为_______ 。
(2)锂离子电池可采用离子液体作为电解质,以下为2种离子液体的结构。
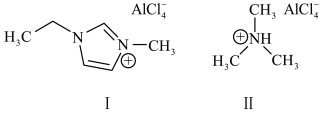
化合物Ⅰ中碳原子的杂化轨道类型为_______ ,1mol化合物Ⅰ中含有_______ 个σ键;化合物Ⅱ中阳离子的空间构型为_______ 。传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是_______ 。
(3)实验室可利用硝酸锰受热分解的方式制备锰的一种氧化物(晶胞结构如图所示)。
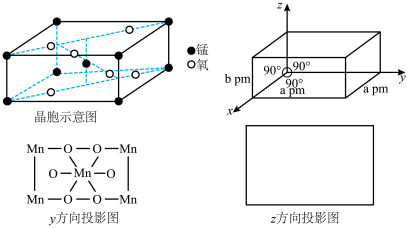
该锰的氧化物中Mn的化合价为_______ ,请画出z方向投影图_______ 。
(1)工业上用
 、
、 、LiCl及苯胺(
、LiCl及苯胺( )为原料制备磷酸亚铁锂。基态Cl原子价电子的轨道表示式为
)为原料制备磷酸亚铁锂。基态Cl原子价电子的轨道表示式为(2)锂离子电池可采用离子液体作为电解质,以下为2种离子液体的结构。

化合物Ⅰ中碳原子的杂化轨道类型为
(3)实验室可利用硝酸锰受热分解的方式制备锰的一种氧化物(晶胞结构如图所示)。

该锰的氧化物中Mn的化合价为
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐3】[化学—选修3:物质结构与性质]
(1)已知X和Y均为短周期元素,其原子的第一至第五电离能如下表所示:
根据上述信息:
①X和氯元素形成的简单分子的空间构型为________ 。
②Y的基态原子的核外电子排布式为________ ,若Y和氯元素形成的分子的相对分子质量为267,请在下列方框中写出该分子的结构式(若存在配位键,用“→”表示)
_____
(2)碳元素可以形成多种单质及化合物:
①C60的结构如图1。C60中的碳原子的杂化轨道类型是________ ;

解释:②金刚石中的C-C的键长大于C60中C-C的键长的原因是________ ;
③金刚石的熔点高于C60的原因是________ ;
(3)如图2是钾的石墨插层化合物的晶胞图(图中大球表示K原子,小球表示C原子),如图3是晶胞沿右侧方向的投影.
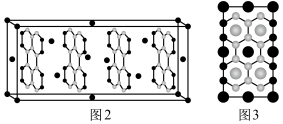
①该化合物的化学式是__________________ ;
②K层与C层之间的作用力是____________________________ ;
③K层中K原子之间的最近距离是C-C键的键长dC-C的_______________ 倍
(4)SiC的晶胞与金刚石的晶胞相似,设碳原子的直径为a cm,硅原子的直径为b cm,则晶胞的边长为_____________ cm(用含a、b的式子表示)。
(1)已知X和Y均为短周期元素,其原子的第一至第五电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 | I5 |
| X | 801 | 2427 | 3660 | 25026 | 32827 |
| Y | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
①X和氯元素形成的简单分子的空间构型为
②Y的基态原子的核外电子排布式为
(2)碳元素可以形成多种单质及化合物:
①C60的结构如图1。C60中的碳原子的杂化轨道类型是

| 碳元素单质 | C-C键长/pm | 熔点/℃ |
| 金刚石 | 154.45 | 3900 |
| C60 | 145~140 | 600(升华) |
③金刚石的熔点高于C60的原因是
(3)如图2是钾的石墨插层化合物的晶胞图(图中大球表示K原子,小球表示C原子),如图3是晶胞沿右侧方向的投影.

①该化合物的化学式是
②K层与C层之间的作用力是
③K层中K原子之间的最近距离是C-C键的键长dC-C的
(4)SiC的晶胞与金刚石的晶胞相似,设碳原子的直径为a cm,硅原子的直径为b cm,则晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐1】研究压电材料对于自动化技术具有重要意义。一种有机—无机复合压电材料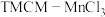 的单斜晶体结构沿晶轴方向投影如图所示(H原子未画出),晶胞内总共含有84个原子。晶胞参数为
的单斜晶体结构沿晶轴方向投影如图所示(H原子未画出),晶胞内总共含有84个原子。晶胞参数为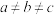 ,
, ,
,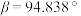 。回答下列问题:
。回答下列问题:
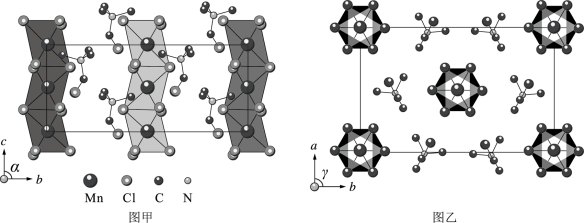
(1)基态Mn原子的价电子轨道表示式为_______ 。在元素周期表中位置为_______ 。
(2)1 mol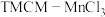 晶胞中含有Cl原子
晶胞中含有Cl原子_______ mol,含有 杂化的中心原子
杂化的中心原子_______ mol;该晶体中提供电子对形成配位键的原子是_______ 。
(3)TMCM性质活泼,一定条件下可分解生成三甲胺[ ],
], 中N原子的价层电子对构型为
中N原子的价层电子对构型为_______ ; 的沸点高于
的沸点高于 ,主要原因是
,主要原因是_______ 。
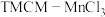 的单斜晶体结构沿晶轴方向投影如图所示(H原子未画出),晶胞内总共含有84个原子。晶胞参数为
的单斜晶体结构沿晶轴方向投影如图所示(H原子未画出),晶胞内总共含有84个原子。晶胞参数为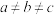 ,
, ,
,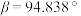 。回答下列问题:
。回答下列问题:
(1)基态Mn原子的价电子轨道表示式为
(2)1 mol
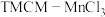 晶胞中含有Cl原子
晶胞中含有Cl原子 杂化的中心原子
杂化的中心原子(3)TMCM性质活泼,一定条件下可分解生成三甲胺[
 ],
], 中N原子的价层电子对构型为
中N原子的价层电子对构型为 的沸点高于
的沸点高于 ,主要原因是
,主要原因是
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
【推荐2】铜及其化合物是高中化学的重要组成部分,在工农业生产中具有重要的应用。
(1)在农业上可用含铜的波尔多液作为农药,配制波尔多液需要___________ (填化学式)。
(2)已知CuCl在氨水中络合后极易被空气中的 氧化。
氧化。
①补齐下列离子方程式:__________ 。
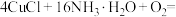 ___________
___________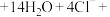 ___________
___________
②现将Cu置于 溶液中,通入
溶液中,通入 ,反应1小时,测得体系中铜离子总浓度为160mg/L,Cu的溶解速率为
,反应1小时,测得体系中铜离子总浓度为160mg/L,Cu的溶解速率为___________ 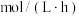 。
。
(3)查阅文献:在无氧条件下CuCl在氨水溶液中存下如下平衡(含足量CuCl固体)
ⅰ:

ⅱ: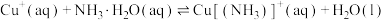

ⅲ: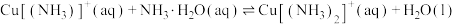

①反应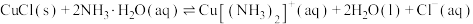

___________ (用 、
、 、
、 来表示);在上述反应中,配原子是
来表示);在上述反应中,配原子是___________ (填元素符号)。
②对于上述相关平衡体系,下列说法不正确的是:___________ (填编号)
A.加水稀释,平衡后溶液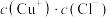 不变
不变
B.向体系中通入 ,有利于提高
,有利于提高 平衡转化率
平衡转化率
C.升高温度,有利于生成
D.溶液中存在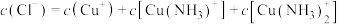
③向一定浓度的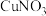 溶液中通入足量
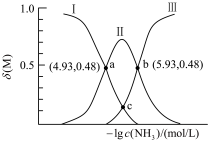
溶液中通入足量 得到澄清溶液(设溶液体积不变),测得平衡体系中含铜微粒分布系数
得到澄清溶液(设溶液体积不变),测得平衡体系中含铜微粒分布系数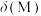 与
与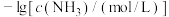 关系如下图所示(其中M代表体系中含铜微粒)。如
关系如下图所示(其中M代表体系中含铜微粒)。如 的分布系数
的分布系数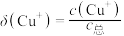 ,
, 。
。___________ 分布系数(填离子符号)。
(b)反应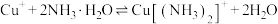 的
的
___________ 。(已知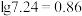 )
)
(c)c点的坐标为___________ 。(已知 )
)
(1)在农业上可用含铜的波尔多液作为农药,配制波尔多液需要
(2)已知CuCl在氨水中络合后极易被空气中的
 氧化。
氧化。①补齐下列离子方程式:
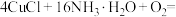 ___________
___________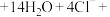 ___________
___________②现将Cu置于
 溶液中,通入
溶液中,通入 ,反应1小时,测得体系中铜离子总浓度为160mg/L,Cu的溶解速率为
,反应1小时,测得体系中铜离子总浓度为160mg/L,Cu的溶解速率为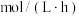 。
。(3)查阅文献:在无氧条件下CuCl在氨水溶液中存下如下平衡(含足量CuCl固体)
ⅰ:


ⅱ:
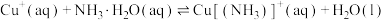

ⅲ:
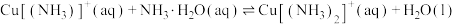

①反应
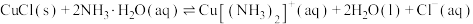

 、
、 、
、 来表示);在上述反应中,配原子是
来表示);在上述反应中,配原子是②对于上述相关平衡体系,下列说法不正确的是:
A.加水稀释,平衡后溶液
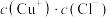 不变
不变B.向体系中通入
 ,有利于提高
,有利于提高 平衡转化率
平衡转化率C.升高温度,有利于生成

D.溶液中存在
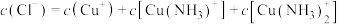
③向一定浓度的
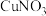 溶液中通入足量
溶液中通入足量 得到澄清溶液(设溶液体积不变),测得平衡体系中含铜微粒分布系数
得到澄清溶液(设溶液体积不变),测得平衡体系中含铜微粒分布系数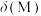 与
与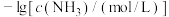 关系如下图所示(其中M代表体系中含铜微粒)。如
关系如下图所示(其中M代表体系中含铜微粒)。如 的分布系数
的分布系数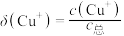 ,
, 。
。
(b)反应
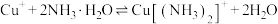 的
的
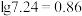 )
)(c)c点的坐标为
 )
)
您最近一年使用:0次



