碳单质有广泛的应用,完成下列问题。
(1)碳有很多同素异形体,例如金刚石、石墨和C60,已知金刚石中C-C键的键长为0.154nm,C60中C-C键键长为0.140~0.145nm。C60的熔点_____ 金刚石(填“高于”或“低于”),理由是_____ 。
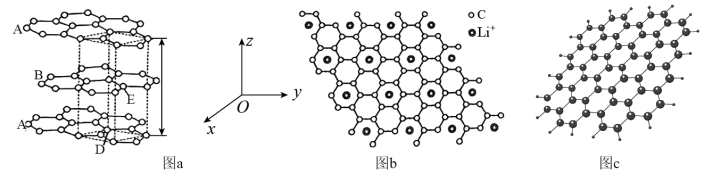
(2)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图a所示,层与层之间靠_____ 维系。图中用虚线标出了石墨的一个六方晶胞。1个六方石墨晶胞中碳原子的个数为_____ ,D处碳原子的分数坐标为(0,0,0),则E处碳原子的分数坐标为_____ (以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标)。
(3)石墨可作锂离子电池的负极材料,锂离子电池充电时,Li+嵌入石墨层间。当嵌入最大量Li+时,晶体部分结构的俯视示意图如图b,此时C与Li+的个数比是_____ 。
(4)石墨烯是一种由单层碳原子构成的二维碳纳米材料,如图c所示。下列有关石墨烯说法正确的是_____。

(1)碳有很多同素异形体,例如金刚石、石墨和C60,已知金刚石中C-C键的键长为0.154nm,C60中C-C键键长为0.140~0.145nm。C60的熔点
(2)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图a所示,层与层之间靠
(3)石墨可作锂离子电池的负极材料,锂离子电池充电时,Li+嵌入石墨层间。当嵌入最大量Li+时,晶体部分结构的俯视示意图如图b,此时C与Li+的个数比是
(4)石墨烯是一种由单层碳原子构成的二维碳纳米材料,如图c所示。下列有关石墨烯说法正确的是_____。
| A.所有碳原子位于同一平面上 | B.石墨烯具有良好的导电性 |
| C.12g石墨烯所含σ键的物质的量为1mol | D.石墨烯属于烯烃类物质 |
更新时间:2023-07-12 18:39:52
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)基态硫原子电子占据的最高能层符号为______ ,核外有______ 种能量不同的电子,硫原子核外电子有______ 种空间运动状态。
(2)与S同主族,位于第四周期的元素的符号是______ ,其价电子排布式为______
(3)已知有下列转化:
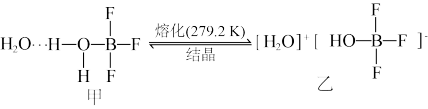
 的VSEPR模型为
的VSEPR模型为______ 。化合物乙中微粒间不存在的化学键有______ (填序号)。
A.离子键 B.共价键 C. 键 D.
键 D. 键 E.氢键
键 E.氢键
(4)相同条件下 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是______ (写分子式),理由是______ 。 中的
中的 键角
键角______ (填“>”“<”或“=”) 中的
中的 键角。
键角。
(5)已知 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为______ ,其中 键与
键与 键的个数比为
键的个数比为______ 。
(1)基态硫原子电子占据的最高能层符号为
(2)与S同主族,位于第四周期的元素的符号是
(3)已知有下列转化:
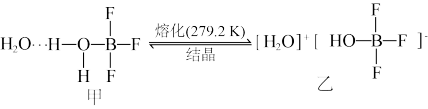
 的VSEPR模型为
的VSEPR模型为A.离子键 B.共价键 C.
 键 D.
键 D. 键 E.氢键
键 E.氢键(4)相同条件下
 与
与 分子在水中的溶解度较大的是
分子在水中的溶解度较大的是 中的
中的 键角
键角 中的
中的 键角。
键角。(5)已知
 是直线形分子,且有对称性,则
是直线形分子,且有对称性,则 分子的结构式为
分子的结构式为 键与
键与 键的个数比为
键的个数比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(1)Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是___ 。Ge单晶具有金刚石型结构,微粒之间存在的作用力是___ 。
(2)Zn的氯化物与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有σ键的数目为___ 。
(3)Co的氯化物与氨水反应可形成配合物[CoCl(NH3)5]Cl2,1mol该配合物中含有σ键的数目为___ ,含1mol[CoCl(NH3)5]Cl2的溶液中加入足量AgNO3溶液,生成___ molAgCl沉淀。
(4)C的某种单质单质 相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环。则1个这种单质分子中所含π键的数目为
相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环。则1个这种单质分子中所含π键的数目为____ 。
(2)Zn的氯化物与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
(3)Co的氯化物与氨水反应可形成配合物[CoCl(NH3)5]Cl2,1mol该配合物中含有σ键的数目为
(4)C的某种单质单质
 相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环。则1个这种单质分子中所含π键的数目为
相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环。则1个这种单质分子中所含π键的数目为
您最近一年使用:0次
【推荐3】根据物质结构与性质的相关知识,请回答下列问题:
I.用符号“>”、“<”或“=”表示下列各项关系。
(1)第一电离能:Na________ Mg,Mg________ Ca。
(2)电负性:O__________ F,F___________ Cl。
(3)能量高低:ns___________ (n+1)s,ns___________ np。
(4)主族序数___________ 价电子数___________ 元素最高正化合价。
(5)甲元素是第3周期p区元素,其最低化合价为—2价;乙元素是第四周期d区元素,其最高化合价为+6价。填写下表:
II.完成下列问题
(6)下列现象和应用与电子跃迁无关的是___________ 。
a.激光b.焰色反应c.原子光谱d.燃烧放热e.石墨导电
(7)A、B两种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍。某平面正六边形分子由A、B两种元素组成且原子个数比为1:1。则1mol该分子中含有___________ 个σ键。
(8)元素铬化合物(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①与铬同周期的基态原子中最外层电子数与铬原子相同的元素有___________ (填元素符号)
②过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]]2+___________ (填“无”或“有”)颜色
I.用符号“>”、“<”或“=”表示下列各项关系。
(1)第一电离能:Na
(2)电负性:O
(3)能量高低:ns
(4)主族序数
(5)甲元素是第3周期p区元素,其最低化合价为—2价;乙元素是第四周期d区元素,其最高化合价为+6价。填写下表:
| 元素 | 名称 | 价电子构型 | 周期 | 族 | 金属或非金属 |
| 甲 | |||||
| 乙 |
II.完成下列问题
(6)下列现象和应用与电子跃迁无关的是
a.激光b.焰色反应c.原子光谱d.燃烧放热e.石墨导电
(7)A、B两种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍。某平面正六边形分子由A、B两种元素组成且原子个数比为1:1。则1mol该分子中含有
(8)元素铬化合物(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①与铬同周期的基态原子中最外层电子数与铬原子相同的元素有
②过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]]2+
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】请用C、H、O、N、S 五种元素回答下列问题
(1)除H 外,其它四种元素中,第一电离能最大的元素基态原子电子排布图为______________ ,电负性最大的元素基态原子核外电子运动状态共有_________ 种。
(2)五种元素中,由其中两种元素构成甲、乙、丙、丁四种分子,所含原子的数目依次为3、4、6、8,都含有18 个电子。甲和乙的主要物理性质比较如下:
①1mol 乙分子含有_________ 个σ键;
②丁分子的中心原子采取_________ 杂化方式; 甲分子的VSEPR模型为_________ ,丙分子为_________ (“极性”或“非极性”) 分子。
③甲和乙的相对分子质量基本相同,造成上述物理性质差异的主要原因是:____________________ (结合具体物质解释)。
(3)已知
由以上数据可知,氮气比乙烯、乙炔难发生加成反应,原因是____________________ 。
(1)除H 外,其它四种元素中,第一电离能最大的元素基态原子电子排布图为
(2)五种元素中,由其中两种元素构成甲、乙、丙、丁四种分子,所含原子的数目依次为3、4、6、8,都含有18 个电子。甲和乙的主要物理性质比较如下:
| 熔点/K | 沸点/ K | 标准状况时在水中的溶解度 | |
| 甲 | 187 | 202 | 2.6 |
| 乙 | 272 | 423 | 以任意比互溶 |
①1mol 乙分子含有
②丁分子的中心原子采取
③甲和乙的相对分子质量基本相同,造成上述物理性质差异的主要原因是:
(3)已知
| 化学键 | N-N | N=N | N N N | C-C | C=C | C C C |
| 键能/kJ·mol-1 | 193 | 418 | 946 | 347.7 | 615 | 812 |
由以上数据可知,氮气比乙烯、乙炔难发生加成反应,原因是
您最近一年使用:0次
【推荐2】钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”、“战略金属”。
(1)基态钛原子核外共有_______ 种运动状态不相同的电子,价电子排布式_______ ;与钛同周期的元素中,基态原子的未成对电子数与钛相同的有________ 种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是_________ 。
(3)TiCl4是氧化法制取钛的中间产物。TiCl4分子结构与CCl4相同,在常温下都是液体。TiCl4分子的空间构型是_______ ;TiCl4稳定性比CCl4差,试从结构分析其原因:_______ 。
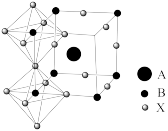
(4)钙钛矿材料是一类有着与钛酸钙相同晶体结构的材料,这种奇特的晶体结构让它具备了很多独特的理化性质,比如吸光性、电催化性等。钛酸钙晶体结构如图所示。其中,A代表Ca2+,Ti原子位于由O原子构成的正八面体的中心,则钛酸钙的化学式为______ ,Ca2+的配位数是________ 。
(1)基态钛原子核外共有
(2)钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是
(3)TiCl4是氧化法制取钛的中间产物。TiCl4分子结构与CCl4相同,在常温下都是液体。TiCl4分子的空间构型是
(4)钙钛矿材料是一类有着与钛酸钙相同晶体结构的材料,这种奇特的晶体结构让它具备了很多独特的理化性质,比如吸光性、电催化性等。钛酸钙晶体结构如图所示。其中,A代表Ca2+,Ti原子位于由O原子构成的正八面体的中心,则钛酸钙的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示:

请回答下列问题:
(1)B和N相比,电负性较大的是___ ,BN中B元素的化合价为___ ;
(2)在BF3分子中,F—B—F的键角是___ ;BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为___ ;
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为___ ,层间作用力为___ ,六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为___ ,其结构与石墨相似却不导电,原因是___ 。
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm。立方氮化硼晶胞中含有___ 个氮原子、___ 个硼原子,立方氮化硼的密度是___ g·cm-3(只要求列算式,不必计算出数值,阿伏加 德罗常数为NA)。

请回答下列问题:
(1)B和N相比,电负性较大的是
(2)在BF3分子中,F—B—F的键角是
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm。立方氮化硼晶胞中含有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】高纯四氧化三锰是电子工业生产锰锌氧软磁材料重要原料之一,以菱锰矿(主要成分为 ,含
,含 和少量
和少量 等元素)为原料制备四氧化三锰工艺流程如图所示。
等元素)为原料制备四氧化三锰工艺流程如图所示。
(1)酸浸时 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)滤渣2的主要成分为___________ (填化学式)。
(3)福美钠的化学式为 生成福美镍沉淀的结构为
生成福美镍沉淀的结构为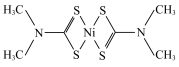 。则各原子之间的结合方式有下列中的
。则各原子之间的结合方式有下列中的___________ (填标号)。
A.离子键 B.金属键 C.氢键 D.配位键 E.极性键
(4)除钙镁时,若使 沉淀完全(浓度小于
沉淀完全(浓度小于 ),溶液中
),溶液中 最小为
最小为___________  。[已知:
。[已知:
(5)除硅时,絮凝剂为阳离子型聚丙烯酰胺,可通过“吸附—电中和—架桥”使硅酸胶体絮凝沉淀,硅酸胶体粒子带___________ 电荷(填“正”或“负”)。
(6) 在空气中被氧化生成
在空气中被氧化生成 的化学方程式为
的化学方程式为___________ 。
(7) 可表示为
可表示为 ,温度高于
,温度高于 时属于立方晶体,其中
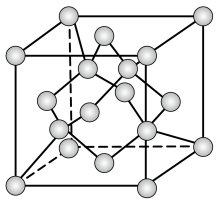
时属于立方晶体,其中 占据晶胞的顶点、面心及内部交错的4个小立方体的体心,与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若
占据晶胞的顶点、面心及内部交错的4个小立方体的体心,与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若 晶体的密度为
晶体的密度为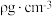 ,则晶胞棱长a=
,则晶胞棱长a=___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 ,含
,含 和少量
和少量 等元素)为原料制备四氧化三锰工艺流程如图所示。
等元素)为原料制备四氧化三锰工艺流程如图所示。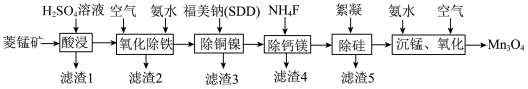
(1)酸浸时
 发生反应的离子方程式为
发生反应的离子方程式为(2)滤渣2的主要成分为
(3)福美钠的化学式为
 生成福美镍沉淀的结构为
生成福美镍沉淀的结构为 。则各原子之间的结合方式有下列中的
。则各原子之间的结合方式有下列中的A.离子键 B.金属键 C.氢键 D.配位键 E.极性键
(4)除钙镁时,若使
 沉淀完全(浓度小于
沉淀完全(浓度小于 ),溶液中
),溶液中 最小为
最小为 。[已知:
。[已知:
(5)除硅时,絮凝剂为阳离子型聚丙烯酰胺,可通过“吸附—电中和—架桥”使硅酸胶体絮凝沉淀,硅酸胶体粒子带
(6)
 在空气中被氧化生成
在空气中被氧化生成 的化学方程式为
的化学方程式为(7)
 可表示为
可表示为 ,温度高于
,温度高于 时属于立方晶体,其中
时属于立方晶体,其中 占据晶胞的顶点、面心及内部交错的4个小立方体的体心,与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若
占据晶胞的顶点、面心及内部交错的4个小立方体的体心,与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若 晶体的密度为
晶体的密度为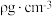 ,则晶胞棱长a=
,则晶胞棱长a= (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】砷化镓是一种半导体化合物,可用于太阳能电池。一种砷化镓废料(主要成分为 ,含
,含 、
、 、
、 等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。
等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。

已知:①“碱浸”时, 中
中 以
以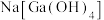 的形式进入溶液。
的形式进入溶液。
②离子完全沉淀时的 :
: 为8,
为8, 为5.6。
为5.6。
(1)As在周期表中的位置为___________ ,最高能级电子云轮廊图为___________ 形。第一电离能比较:
___________  (填“<”“>”或“=”,下同),原子半径比较:As
(填“<”“>”或“=”,下同),原子半径比较:As___________ Ga。
(2)下图为砷化镓晶胞,白球所代表原子的配位数是___________ 。已知:晶胞参数为apm,密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为___________ (用含a、d的式子表示)。

(3)“碱浸”时, 参加的离子方程式为
参加的离子方程式为___________ 。
(4)“调 ①”时,
①”时,
___________ 最合适;滤液②的溶质成分为___________ (写化学式)。
(5)写出用情性电极电解制备镓单质的电极反应方程式:___________ 。
 ,含
,含 、
、 、
、 等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。
等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。
已知:①“碱浸”时,
 中
中 以
以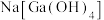 的形式进入溶液。
的形式进入溶液。②离子完全沉淀时的
 :
: 为8,
为8, 为5.6。
为5.6。(1)As在周期表中的位置为

 (填“<”“>”或“=”,下同),原子半径比较:As
(填“<”“>”或“=”,下同),原子半径比较:As(2)下图为砷化镓晶胞,白球所代表原子的配位数是
 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为
(3)“碱浸”时,
 参加的离子方程式为
参加的离子方程式为(4)“调
 ①”时,
①”时,
(5)写出用情性电极电解制备镓单质的电极反应方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵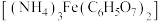 。
。
(1)Fe基态核外电子排布式为_______ ; 中与
中与 配位的原子是
配位的原子是_______ (填元素符号)。
(2) 分子中氮原子的轨道杂化类型是
分子中氮原子的轨道杂化类型是_______ ;C、N、O元素的第一电离能由大到小的顺序为_______ 。
(3)与 互为等电子体的一种分子为
互为等电子体的一种分子为_______ (填化学式)。
(4)柠檬酸的结构简式如图。1mol柠檬酸分子中碳原子与氧原子形成的 键的数目为
键的数目为_______ mol。

(5)偏铝酸钠中阴离子的空间构型_______ 。
(6)氮化硼晶体的晶胞结构与金刚石晶体的晶胞结构相同,氮化硼晶体的密度为pg/cm3,阿伏加德罗常数为NA值,氮化硼的摩尔质量为mg/mol,则氮化硼晶体的体积_______ cm3。
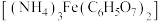 。
。(1)Fe基态核外电子排布式为
 中与
中与 配位的原子是
配位的原子是(2)
 分子中氮原子的轨道杂化类型是
分子中氮原子的轨道杂化类型是(3)与
 互为等电子体的一种分子为
互为等电子体的一种分子为(4)柠檬酸的结构简式如图。1mol柠檬酸分子中碳原子与氧原子形成的
 键的数目为
键的数目为
(5)偏铝酸钠中阴离子的空间构型
(6)氮化硼晶体的晶胞结构与金刚石晶体的晶胞结构相同,氮化硼晶体的密度为pg/cm3,阿伏加德罗常数为NA值,氮化硼的摩尔质量为mg/mol,则氮化硼晶体的体积
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】碳材料在生活中占有重要地位。
请回答:
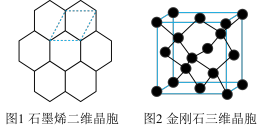
(1)下列说法正确的是 。
(2)图 1 中 C—C 键键长为 apm,则石墨烯的密度ρ=______________ g/cm2 (用含 a 式子表示,阿伏伽德罗常数为 NA)
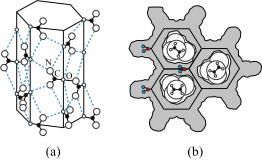
(3)尿素[(NH2)2CO]可以与正烷烃(n~CmH2m+2,m≥8)形成超分子包合物。尿素中各种元素的电负性由大到小的顺序________________ ,尿素分子通过______________________ 氢键(写出具体形式)
有序地组合成具有蜂窝状六角形通道结构的接受体,如(a)所示。正烷烃分子作为底物填入到通道之中,图(b)示出垂直于通道截面的结构。该超分子包合物能稳定存在的原因是_________________________ 。
请回答:

(1)下列说法正确的是 。
| A.石墨烯碳采用 sp2杂化,金刚石 VSPRE 模型为正四面体形 |
| B.多层石墨烯和金刚石均为共价型晶体 |
| C.1mol 石墨烯与金刚石中,σ键键数之比为 3:4 |
| D.石墨烯中 C—C 键键能较金刚石大,故石墨烯的内能更高 |
(3)尿素[(NH2)2CO]可以与正烷烃(n~CmH2m+2,m≥8)形成超分子包合物。尿素中各种元素的电负性由大到小的顺序
有序地组合成具有蜂窝状六角形通道结构的接受体,如(a)所示。正烷烃分子作为底物填入到通道之中,图(b)示出垂直于通道截面的结构。该超分子包合物能稳定存在的原因是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】化学物质结构与性质按要求回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________形象化描述;在基态14C原子中,核外存在___________对自旋相反的电子。
(2)在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接___________个六元环,六元环中最多有___________个C原子在同一平面,一个金刚石晶胞平均占有碳原子个数为___________。
(3)与N2互为等电子体的分子是___________,该分子的电子式为___________。
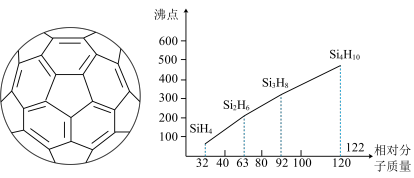
(4)已知C60分子结构如图所示:该笼状分子是由多个正六边形和正五边形组成的,面体的顶点数V、面数F及棱数E间关系为:V+F-E=2,则此分子中共有___________个正五边形。
(5)硅烷(SinH2n+2)的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是___________。

(6) NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为___________ cm(用含有a的代数式表示),在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为___________g(氧离子的半径为1.40×10-10m )。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________形象化描述;在基态14C原子中,核外存在___________对自旋相反的电子。
(2)在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接___________个六元环,六元环中最多有___________个C原子在同一平面,一个金刚石晶胞平均占有碳原子个数为___________。
(3)与N2互为等电子体的分子是___________,该分子的电子式为___________。
(4)已知C60分子结构如图所示:该笼状分子是由多个正六边形和正五边形组成的,面体的顶点数V、面数F及棱数E间关系为:V+F-E=2,则此分子中共有___________个正五边形。
(5)硅烷(SinH2n+2)的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是___________。


(6) NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为___________ cm(用含有a的代数式表示),在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为___________g(氧离子的半径为1.40×10-10m )。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。
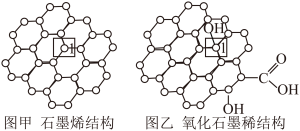
(1)图甲中, 1号C与相邻C形成σ键的个数为___________ 。在石墨烯(图甲)晶体中, 每个C原子连接___________ 个六元环,平均每个六元环占有___________ 个C原子。
(2)若将图乙所示的氧化石墨烯分散在 H2O 中,则氧化石墨烯中可与H2O 形成氢键的原子有___________ (填元素符号)。
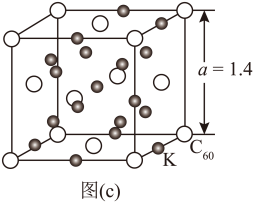
(3)碳的另一种单质 C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为K3C60。其晶胞参数a为1.4nm,则晶胞密度为___________ g/cm3。(保留一位小数)
Ⅱ.金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示。
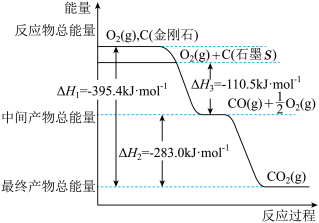
(4)在通常状况下,金刚石和石墨中___________ (填“金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH为___________ 。
(5)已知:N2、O2分子中化学键的键能分别是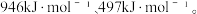
N2(g)+O2(g)=2NO(g) ΔH=180.0 kJ·mol-1,NO分子中化学键的键能为___________ kJ·mol-1。
(6)综合上述有关信息,请写出CO与NO反应的热化学方程式:___________ 。

(1)图甲中, 1号C与相邻C形成σ键的个数为

(2)若将图乙所示的氧化石墨烯分散在 H2O 中,则氧化石墨烯中可与H2O 形成氢键的原子有
(3)碳的另一种单质 C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为K3C60。其晶胞参数a为1.4nm,则晶胞密度为
Ⅱ.金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示。

(4)在通常状况下,金刚石和石墨中
(5)已知:N2、O2分子中化学键的键能分别是
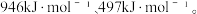
N2(g)+O2(g)=2NO(g) ΔH=180.0 kJ·mol-1,NO分子中化学键的键能为
(6)综合上述有关信息,请写出CO与NO反应的热化学方程式:
您最近一年使用:0次



