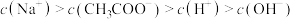25℃时,在20mL HA溶液中逐滴加入
HA溶液中逐滴加入 NaOH溶液,pH的变化曲线如图所示,下列有关说法或关系不正确的是
NaOH溶液,pH的变化曲线如图所示,下列有关说法或关系不正确的是
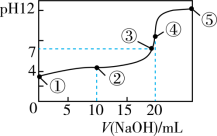
 HA溶液中逐滴加入
HA溶液中逐滴加入 NaOH溶液,pH的变化曲线如图所示,下列有关说法或关系不正确的是
NaOH溶液,pH的变化曲线如图所示,下列有关说法或关系不正确的是
| A.甲基橙可以选为该滴定过程终点判断的指示剂 |
| B.由点①可知HA是一元弱酸 |
| C.点④溶液溶质为NaA,该点溶液呈碱性 |
D.点③溶液中有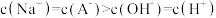 |
更新时间:2023-08-14 23:09:46
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列有关中和滴定的叙述正确的是( )
| A.滴定时,标准液的浓度一定越小越好 |
| B.用盐酸作标准液滴定NaOH溶液时,指示剂加入越多越好 |
| C.滴定管在滴液前和滴液后均有气泡一定不会造成误差 |
| D.滴定时眼睛应注视锥形瓶内溶液的颜色变化而不应注视滴定管内的液面变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】25℃时,用0.1000mol·L-1的盐酸分别滴定20.00mL 0.1000mol·L-1氨水和20.00mL 0.1000mol·L-1 NaOH溶液,滴定曲线如图所示。下列说法不正确的是


| A.25℃,Kb(NH3·H2O)的数量级为10-5 |
B.N点处的溶液中:c(NH )>c(NH3·H2O) )>c(NH3·H2O) |
| C.曲线II滴定终点时所选的指示剂为酚酞 |
| D.Q点所加盐酸的体积为b mL,则b=20 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下,测得某氨水溶液的pH约为12,将其与0.01mol/L的盐酸等体积混合后,所得溶液中物质的量浓度最大的离子是
| A.Cl- | B.NH | C.H+ | D.OH- |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】足量的锌和下列酸反应,产生H2的物质的量最多的是( )
| A.10mL 18.4mol/L H2SO4 | B.30mL 3mol/L盐酸 |
| C.30mL 2mol/L H2SO4 | D.30mL 5mol/L HNO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是


A.稀释前,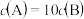 |
B.稀释前,A溶液中由水电离出的 的浓度大于 的浓度大于 |
| C.用醋酸中和A溶液至恰好完全反应时,溶液的pH为7 |
| D.在M点,A、B两种碱溶液中阳离子的物质的量浓度相等 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】25℃时,在等体积的①pH=0的H2SO4溶液、②0.05mol·L-1的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,由水电离的H+的物质的量之比是
| A.1∶10∶1010∶109 | B.1∶5∶(5×109)∶(5×108) |
| C.1∶20∶1010∶109 | D.1∶10∶104∶109 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】能影响水的电离平衡,并使溶液中的 c(H+)<c(OH-)的操作是
| A.向水中加入硫酸钾晶体 |
| B.将水加热煮沸 |
| C.向水中通入二氧化硫气体 |
| D.向水中加入小苏打晶体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法或表示错误的是
A.pH的醋酸溶液稀释,水电离出的 浓度将增大 浓度将增大 |
B.Na2CO3溶液中存在的离子浓度关系 |
C.反应 的平衡常数 的平衡常数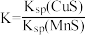 |
D.CH4的燃烧为-890.31 kJ/mol,则表示其燃烧热的热化学方程式为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】常温下, 溶液、
溶液、 溶液的
溶液的 均大于7。下列关于这两种溶液的说法正确的是
均大于7。下列关于这两种溶液的说法正确的是
 溶液、
溶液、 溶液的
溶液的 均大于7。下列关于这两种溶液的说法正确的是
均大于7。下列关于这两种溶液的说法正确的是A. 溶液中存在平衡: 溶液中存在平衡: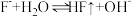 |
B.加热, 溶液的碱性增强 溶液的碱性增强 |
C. 溶液中: 溶液中: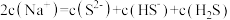 |
D. 溶液中: 溶液中: |
您最近一年使用:0次

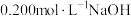 溶液滴定
溶液滴定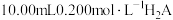 溶液,加入NaOH溶液的体积、
溶液,加入NaOH溶液的体积、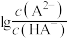 与pH的变化关系如图所示。下列说法正确的是
与pH的变化关系如图所示。下列说法正确的是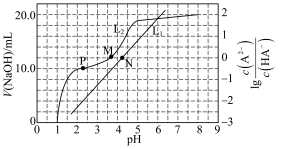
 表示加入NaOH溶液的体积与pH的变化关系
表示加入NaOH溶液的体积与pH的变化关系 的第二步电离常数
的第二步电离常数 的数量级为
的数量级为
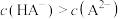
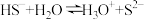
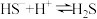

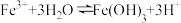
 稀溶液中,下列离子浓度关系不正确的是
稀溶液中,下列离子浓度关系不正确的是