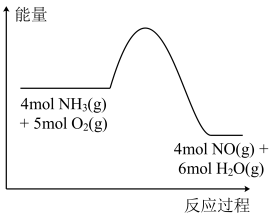
某温度下在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化如图所示。下列说法正确的是
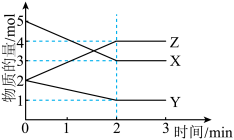

A.该反应的化学方程式为 |
| B.容器内气体的密度保持不变不能说明该反应达到平衡状态 |
| C.1min时,正反应速率小于逆反应速率 |
| D.0~2min内X的转化率为60% |
更新时间:2023-09-23 19:27:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在密闭容器中,充入SO2和18O原子组成的氧气,在一定条件下开始反应,在达到平衡后,18O存在于
| A.只存在于氧气中 | B.只存在于SO3中 |
| C.只存在于SO2和SO3中 | D.SO2、SO3、O2中都存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸 |
| B.将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验麦芽糖是还原性糖 |
| C.在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应可得到NH3分子数为NA |
| D.标准状况下,33.6 L二氯甲烷中含有氯原子的数目为3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验能达到预期目的是
| 实验内容 | 实验目的 | |
| A | 将0.2mol·L-1的KI溶液和0.05mol·L-1的FeCl3溶液等体积混合,充分反应后,取少许混合液向其中滴入AgNO3溶液 | 验证Fe3+与I-的反应有一定限度 |
| B | 将FeCl3固体溶于较浓的盐酸中,然后加水稀释 | 配制FeCl3溶液 |
| C | 将混合气体通入酸性高锰酸钾溶液中 | 除去乙烷中的乙烯 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在容积不变的密闭容器中:N2+ 3H2 2NH3,下列不能说明反应已平衡的是:
2NH3,下列不能说明反应已平衡的是:
 2NH3,下列不能说明反应已平衡的是:
2NH3,下列不能说明反应已平衡的是:| A.容器内的压强不变 |
| B.单位时间内,消耗1 mol N2的同时,生成2 molNH3 |
| C.混合气体的相对分子质量不变 |
| D.混合物的总物质的量不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在体积为2L的恒容绝热密闭容器中投入1molA和1molB,发生反应
 ,2min后达到平衡,此时容器内有0.3molC。下列说法
,2min后达到平衡,此时容器内有0.3molC。下列说法不正确 的是

 ,2min后达到平衡,此时容器内有0.3molC。下列说法
,2min后达到平衡,此时容器内有0.3molC。下列说法| A.若容器内混合气体压强不变,则反应达到平衡状态 |
B.单位时间内 生成时,则反应达到平衡状态 生成时,则反应达到平衡状态 |
| C.若开始时在该容器中投入1molA和2molB,则平衡时B的转化率小于30% |
| D.若将容器的体积压缩到原来的一半,正逆反应速率都增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中不能用勒夏特列原理来解释的是
| A.红棕色的NO2气体,加压后颜色先变深后变浅 |
| B.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| C.高压比常压有利于合成SO3 的反应 |
| D.黄绿色的氯水光照后颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实不涉及勒夏特列原理的是
A.加热蒸干 溶液得到 溶液得到 固体 固体 |
B.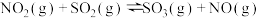 ,对该平衡体系加压后颜色加深 ,对该平衡体系加压后颜色加深 |
C.在 的红色溶液中加铁粉,振荡静置,溶液的红色变浅或褪去 的红色溶液中加铁粉,振荡静置,溶液的红色变浅或褪去 |
| D.黄绿色的氯水在光照后颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】T℃时,在1L的密闭容器中充入1molCO2和3molH2,发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)∆H=-49.0kJ·mol-1,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是( )
CH3OH(g)+H2O(g)∆H=-49.0kJ·mol-1,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是( )

 CH3OH(g)+H2O(g)∆H=-49.0kJ·mol-1,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是( )
CH3OH(g)+H2O(g)∆H=-49.0kJ·mol-1,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是( )
| A.T℃时,平衡常数K=3,CO2与H2的平衡转化率相等 |
| B.T℃时,上述条件下达到平衡时放出49.0kJ的热量 |
| C.降温和缩小容器体积均可使反应的平衡常数增大 |
| D.从反应开始到3min,H2的平均反应速率υ(H2)=0.5mol•L-1•min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法中正确的是
| A.影响化学反应速率的主要因素为浓度、温度、压强和催化剂 |
| B.能加快Fe与稀H2SO4反应产生H2的速率的措施可以是将稀硫酸改为98%的浓硫酸 |
C.恒温恒容时向已达平衡的2SO3(g) 2SO2(g)+O2(g)体系中充入SO3,SO3转化率将升高 2SO2(g)+O2(g)体系中充入SO3,SO3转化率将升高 |
D.压缩已达平衡的2NO2(g) N2O4(g)体系的体积,再达平衡时气体颜色比原平衡的深 N2O4(g)体系的体积,再达平衡时气体颜色比原平衡的深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】利用CH4(g)+2NO2(g) N2(g)+CO2(g)+2N2O(g)可消除NO2的污染。在1 L的密闭容器中,控制不同温度,分别加入0.50 mol CH4(g)和1.20 mol NO2(g)进行上述反应,测得n(CH4)随时间变化的实验数据如表。下列说法错误的是
N2(g)+CO2(g)+2N2O(g)可消除NO2的污染。在1 L的密闭容器中,控制不同温度,分别加入0.50 mol CH4(g)和1.20 mol NO2(g)进行上述反应,测得n(CH4)随时间变化的实验数据如表。下列说法错误的是
 N2(g)+CO2(g)+2N2O(g)可消除NO2的污染。在1 L的密闭容器中,控制不同温度,分别加入0.50 mol CH4(g)和1.20 mol NO2(g)进行上述反应,测得n(CH4)随时间变化的实验数据如表。下列说法错误的是
N2(g)+CO2(g)+2N2O(g)可消除NO2的污染。在1 L的密闭容器中,控制不同温度,分别加入0.50 mol CH4(g)和1.20 mol NO2(g)进行上述反应,测得n(CH4)随时间变化的实验数据如表。下列说法错误的是| 组别 | 温度 | n/mol | 0 min | 10 min | 20 min | 40 min | 50 min |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | x | 0.15 |
| A.由实验数据可知:T1>T2 |
| B.实验①中,0~20 min内,v(CH4)=0.0125 mol·L-1·min-1 |
| C.实验②中,0~10 min内,NO2的转化率为33.3% |
| D.40 min时,实验②中反应已达平衡状态 |
您最近一年使用:0次

 ,能说明反应达到化学平衡状态的是
,能说明反应达到化学平衡状态的是
 和
和 的浓度相等
的浓度相等