硫的化合物在化工生产等领域应用广泛。
(1)Na2S2可作制革工业中原皮的脱毛剂,其中硫元素的化合价是___________ 。
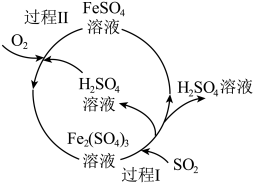
(2)含硫煤燃烧会产生大气污染物,设计了如下图所示的工艺流程进行治污。写出图中过程I反应的离子方程式___________ ,该工艺流程得到的化工产品是___________ (填化学式)。
(3)25℃时,实验测得NH4HSO3溶液中 =1500,则该溶液的pH为
=1500,则该溶液的pH为___________ (已知25℃时,H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)。
(4)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是___________(填标号)。
(5)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为___________ (已知:N2H4+H+ N2H
N2H 的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为
的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为___________ 。
(1)Na2S2可作制革工业中原皮的脱毛剂,其中硫元素的化合价是
(2)含硫煤燃烧会产生大气污染物,设计了如下图所示的工艺流程进行治污。写出图中过程I反应的离子方程式

(3)25℃时,实验测得NH4HSO3溶液中
 =1500,则该溶液的pH为
=1500,则该溶液的pH为(4)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是___________(填标号)。
| A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以 |
| B.氢硫酸的导电能力低于相同浓度的亚硫酸 |
| C.0.10 mol·L−1的氢硫酸和亚硫酸的pH分别为4.5和2.1 |
| D.氢硫酸的还原性强于亚硫酸 |
 N2H
N2H 的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为
的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为
更新时间:2023-10-21 09:50:52
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】按要求填空:
(1)写出下列物质溶于水或熔融状态下的电离方程式:
①CaCl2:___ ;②NaHCO3:___ ;③Ba(OH)2:___ ;④熔融状态的KHSO4:___ 。
(2)现有以下物质:①NaCl晶体②液态HCl③CaCO3固体④熔融KCl⑤蔗糖⑥铜⑦CO2⑧H2SO4⑨KOH固体
a.以上物质中能导电的是___ (填字母序号,下同);
b.以上物质中属于电解质的是___ ,属于非电解质的是___ ;
c.以上物质中,溶于水且生成的水溶液能导电的物质是___ 。
(3)在反应KMNO3+HCl→KCl+MnCl2+Cl2↑+H2O(未配平)中,氧化产物是___ (填化学式),当有5molHCl被氧化时,被还原的KMnO4为___ mol。
(4)现需配制0.1mol·L-1NaOH溶液450mL,如图是某同学转移溶液的示意图。

①根据计算用托盘天平称取NaOH固体的质量为___ g,为完成此溶液配制实验需要的玻璃仪器有___ ;
②图中的错误是___ ;
③配制溶液时,下列操作会导致所配溶液的浓度偏低的是___ (填字母序号)。
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹液面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线
(1)写出下列物质溶于水或熔融状态下的电离方程式:
①CaCl2:
(2)现有以下物质:①NaCl晶体②液态HCl③CaCO3固体④熔融KCl⑤蔗糖⑥铜⑦CO2⑧H2SO4⑨KOH固体
a.以上物质中能导电的是
b.以上物质中属于电解质的是
c.以上物质中,溶于水且生成的水溶液能导电的物质是
(3)在反应KMNO3+HCl→KCl+MnCl2+Cl2↑+H2O(未配平)中,氧化产物是
(4)现需配制0.1mol·L-1NaOH溶液450mL,如图是某同学转移溶液的示意图。

①根据计算用托盘天平称取NaOH固体的质量为
②图中的错误是
③配制溶液时,下列操作会导致所配溶液的浓度偏低的是
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹液面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】2020年初,突如其来的新型冠状肺炎在全世界肆虐,社会生产、人民生活都受到了一定程度的影响,同学们也不能正常上学。“停课不停学”的网络课程学习让同学们充分发挥了自主学习能力。某中学的几位同学就查阅了大量资料,并进行相关实验探究,来认识可以有效灭活新型冠状病毒的含氯消毒剂——次氯酸钠NaClO。
I.次氯酸钠的制备和性质
(1)家中常用的84消毒液的有效成分即是次氯酸钠,若将 通入冷的稀NaOH溶液中则可制得消毒液,该反应的离子方程式为
通入冷的稀NaOH溶液中则可制得消毒液,该反应的离子方程式为___________________ 。
(2)在查阅资料中,同学们发现“百度百科”中有这样一句话:家用洁厕灵(含盐酸)不能和84消毒液混用,否则会产生氯气,引起中毒,发生的反应为___________ 。该反应NaClO______ (“得到”或“失去”)电子,反应每生成标准状况下11.2 L氯气,转移的电子数为______ 。
II.同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5 mL市售84消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后的溶液各20 mL分别加入a、b、c三个洁净的烧杯中;
步骤3:用 溶液将a、b、c三个烧杯内溶液的PH分别调至10、7和4(溶液体积变化忽略不计);
溶液将a、b、c三个烧杯内溶液的PH分别调至10、7和4(溶液体积变化忽略不计);
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如表.
已知溶液中 、HClO和
、HClO和 的物质的量分数(α)随溶液pH变化的关系如图所示:
的物质的量分数(α)随溶液pH变化的关系如图所示:

(3)由实验现象可获得结论:溶液的pH在4-10范围内,pH越大,红纸褪色______ (填“越快”或“越慢”)。
(4)结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是___________ 。
I.次氯酸钠的制备和性质
(1)家中常用的84消毒液的有效成分即是次氯酸钠,若将
 通入冷的稀NaOH溶液中则可制得消毒液,该反应的离子方程式为
通入冷的稀NaOH溶液中则可制得消毒液,该反应的离子方程式为(2)在查阅资料中,同学们发现“百度百科”中有这样一句话:家用洁厕灵(含盐酸)不能和84消毒液混用,否则会产生氯气,引起中毒,发生的反应为
II.同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5 mL市售84消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后的溶液各20 mL分别加入a、b、c三个洁净的烧杯中;
步骤3:用
 溶液将a、b、c三个烧杯内溶液的PH分别调至10、7和4(溶液体积变化忽略不计);
溶液将a、b、c三个烧杯内溶液的PH分别调至10、7和4(溶液体积变化忽略不计);步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如表.
烧杯 | 溶液的pH | 现象 |
a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
c | 4 | 10min后,红纸颜色比b烧杯中10min后的浅;4h后红纸褪色 |
 、HClO和
、HClO和 的物质的量分数(α)随溶液pH变化的关系如图所示:
的物质的量分数(α)随溶液pH变化的关系如图所示:
(3)由实验现象可获得结论:溶液的pH在4-10范围内,pH越大,红纸褪色
(4)结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】某油脂厂废弃的油脂加氢所用催化剂主要含金属Ni、Al、Fe及它们的氧化物,还有少量其它不溶性物质。采用如图工艺流程回收其中的镍来制备硫酸镍晶体(NiSO4·7H2O):
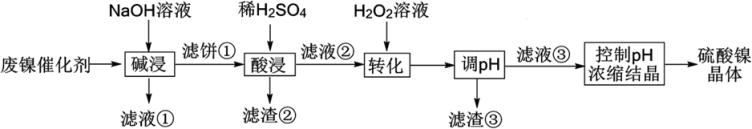
溶液中各金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
(1)废弃催化剂上的油脂在___________ 过程中被处理。
(2)滤液①中含有的无机阴离子除OH-离子外还有___________ 。
(3)“转化”过程的离子方程式为___________ ;“转化”过程温度不宜过高的原因是___________ 。
(4)“调pH”时应控制的pH范围是___________ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式___________ 。

溶液中各金属离子开始沉淀和完全沉淀的pH如表所示,回答下列问题:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时的pH | 7.1 | 3.4 | 1.5 | 6.3 |
| 完全沉淀时的pH | 9.1 | 4.7 | 2.8 | 8.3 |
(2)滤液①中含有的无机阴离子除OH-离子外还有
(3)“转化”过程的离子方程式为
(4)“调pH”时应控制的pH范围是
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】按要求回答问题:
(1)已知稀溶液中,1mol 与NaOH溶液恰好完全反应时,放出114kJ热量,写出表示
与NaOH溶液恰好完全反应时,放出114kJ热量,写出表示 与NaOH反应的中和热的热化学方程式
与NaOH反应的中和热的热化学方程式_______ 。
(2)已知在25℃、101kPa下,10g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出295kJ的热量,试写出乙醇燃烧热的热化学方程式_______ 。
(3) 是一种无色气体,遇到空气能发生爆炸性自燃,生成固体
是一种无色气体,遇到空气能发生爆炸性自燃,生成固体 和液态
和液态 。已知室温下,2g
。已知室温下,2g  自燃放出89.2kJ热量,写出该反应的热化学方程式
自燃放出89.2kJ热量,写出该反应的热化学方程式_______ 。
(4)已知:
①

②

③

写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_______ 。
(5)若稀硫酸与氢氧化钡稀溶液反应生成1mol (l),则反应放出的热量
(l),则反应放出的热量_______ (填“大于”“等于”或“小于”)57.3kJ,原因是_______ (从化学键的角度简单解释即可)。
(6)25℃时,相同pH的两种一元弱酸HA与HB溶液各2mL分别加水稀释,溶液pH随溶液体积变化的曲线如图所示。下列说法正确的是

(1)已知稀溶液中,1mol
 与NaOH溶液恰好完全反应时,放出114kJ热量,写出表示
与NaOH溶液恰好完全反应时,放出114kJ热量,写出表示 与NaOH反应的中和热的热化学方程式
与NaOH反应的中和热的热化学方程式(2)已知在25℃、101kPa下,10g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出295kJ的热量,试写出乙醇燃烧热的热化学方程式
(3)
 是一种无色气体,遇到空气能发生爆炸性自燃,生成固体
是一种无色气体,遇到空气能发生爆炸性自燃,生成固体 和液态
和液态 。已知室温下,2g
。已知室温下,2g  自燃放出89.2kJ热量,写出该反应的热化学方程式
自燃放出89.2kJ热量,写出该反应的热化学方程式(4)已知:
①


②


③


写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(5)若稀硫酸与氢氧化钡稀溶液反应生成1mol
 (l),则反应放出的热量
(l),则反应放出的热量(6)25℃时,相同pH的两种一元弱酸HA与HB溶液各2mL分别加水稀释,溶液pH随溶液体积变化的曲线如图所示。下列说法正确的是

A.a点的 大于b点的 大于b点的 | B.a点溶液的导电性大于b点溶液 |
| C.a点溶液比b点溶液中水的电离程度大 | D.同浓度的NaA与NaB溶液中, 大于 大于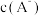 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】现有下列电解质:①稀硫酸②冰醋酸③Ba(OH)2④石炭酸⑤氨水⑥NaHSO4⑦盐酸⑧明矾⑨钾钠合金。
(1)(用序号填空)其中可以导电的有___ ,属于弱电解质的是____ ,属于盐的有___ 。
(2)写出⑥在融化状态下的电离方程式:______ 。
(3)写出将③的水溶液逐滴加入到一定量的⑧溶液中至沉淀质量最大时的离子方程式:___ 。
(1)(用序号填空)其中可以导电的有
(2)写出⑥在融化状态下的电离方程式:
(3)写出将③的水溶液逐滴加入到一定量的⑧溶液中至沉淀质量最大时的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】请回答下列问题:
(1)现有下列物质,请用序号填空:
①氧化钠固体 ②胆矾晶体 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑥蔗糖 ⑦二氧化碳
上述状态下可导电的是___________ 。属于强电解质的是___________ 。属于非电解质的是___________ 。
(2)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,利用___________ 来证明得到的分散系是氢氧化铁胶体。
(3)NaHSO4 固体溶于水的电离方程式为___________ ;
(4)写出少量硫酸铁和氢氧化钡溶液反应的离子方程式为___________ 。
(5)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断它们的化学式为:C___________ ,D ___________ ;
A与C反应的离子方程式___________ ;
A溶液中阴离子的检验方法___________ 。
(1)现有下列物质,请用序号填空:
①氧化钠固体 ②胆矾晶体 ③熔融氯化钠 ④稀盐酸 ⑤氨水 ⑥蔗糖 ⑦二氧化碳
上述状态下可导电的是
(2)向50ml沸水中加入5~6滴饱和FeCl3溶液,加热至产生红褐色液体,停止加热,利用
(3)NaHSO4 固体溶于水的电离方程式为
(4)写出少量硫酸铁和氢氧化钡溶液反应的离子方程式为
(5)A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO
 、SO
、SO 、Cl-、CO
、Cl-、CO (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断它们的化学式为:C
A与C反应的离子方程式
A溶液中阴离子的检验方法
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】已知某温度下 的电离常数
的电离常数 。该温度下,向
。该温度下,向 溶液中逐滴加入
溶液中逐滴加入 溶液,其
溶液,其 变化曲线如图所示(忽略温度变化)。
变化曲线如图所示(忽略温度变化)。

请回答下列有关问题:
(1)a、b、c、d四点中水的电离程度最大的是________ 点,滴定过程中宜选用________ 作指示剂,滴定终点在________ (填“c点以上”或“c点以下”)。
(2)下列操作中可能使所测 溶液的浓度数值偏低的是
溶液的浓度数值偏低的是_______ (填字母)。
A.酸式滴定管未用待测溶液润洗
B.锥形瓶用待测溶液润洗
C.放出酸液的滴定管开始有气泡,放出液体后气泡消失
D.碱式滴定管滴定前有气泡,滴定终点时气泡消失
E.碱式滴定管滴定前读数正确,滴定后俯视读数
(3)若向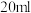 稀氨水中逐滴加入等浓度的盐酸,下列变化趋势正确的是
稀氨水中逐滴加入等浓度的盐酸,下列变化趋势正确的是________ (填序号).
A. B.
B. C.
C. D.
D.
 的电离常数
的电离常数 。该温度下,向
。该温度下,向 溶液中逐滴加入
溶液中逐滴加入 溶液,其
溶液,其 变化曲线如图所示(忽略温度变化)。
变化曲线如图所示(忽略温度变化)。
请回答下列有关问题:
(1)a、b、c、d四点中水的电离程度最大的是
(2)下列操作中可能使所测
 溶液的浓度数值偏低的是
溶液的浓度数值偏低的是A.酸式滴定管未用待测溶液润洗
B.锥形瓶用待测溶液润洗
C.放出酸液的滴定管开始有气泡,放出液体后气泡消失
D.碱式滴定管滴定前有气泡,滴定终点时气泡消失
E.碱式滴定管滴定前读数正确,滴定后俯视读数
(3)若向
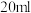 稀氨水中逐滴加入等浓度的盐酸,下列变化趋势正确的是
稀氨水中逐滴加入等浓度的盐酸,下列变化趋势正确的是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ.25℃时,部分弱酸的电离平衡常数如下表:
(1)H2S的二级电离平衡常数的表达式为_________ 。
(2)相同c(H+)浓度的HCOOH和HClO溶液中:c(HCOOH)______ c(HClO) (填“>”、“<”或“=”)。
Ⅱ.现将pH=3,体积均为V0的盐酸和醋酸溶液分别加水稀释至体积V,pH随lg( )的变化如图所示。
)的变化如图所示。

(3)醋酸的电离平衡常数表达式为Ka=________ ;加水稀释过程中,醋酸的电离平衡向______ (填“正”或“逆”)反应方向移动,Ka______ 填“增大”“减小”或“不变”)。
(4)比较b、c两点溶液的导电能力强弱:b_______ c(填大于、小于、等于)。
(5)已知HA的电离常数Ka1=4.9×10-10,H2B的电离常数Ka1=4.3×10-7,Ka2=5.6×10-12,试写出NaA与少量H2B反应的离子方程式___________ 。
| 弱酸 | HCOOH | H2S | H2CO3 | HClO |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka1=1.3×10-7 Ka2=7.1×10-15 | Ka1=4.4×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 |
(2)相同c(H+)浓度的HCOOH和HClO溶液中:c(HCOOH)
Ⅱ.现将pH=3,体积均为V0的盐酸和醋酸溶液分别加水稀释至体积V,pH随lg(
 )的变化如图所示。
)的变化如图所示。
(3)醋酸的电离平衡常数表达式为Ka=
(4)比较b、c两点溶液的导电能力强弱:b
(5)已知HA的电离常数Ka1=4.9×10-10,H2B的电离常数Ka1=4.3×10-7,Ka2=5.6×10-12,试写出NaA与少量H2B反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】研究电解质在水溶液中的平衡能了解它的存在形式。
(1)已知部分弱酸常温下的电离常数如下表:
①常温下pH相同的三种溶液HA、 、
、 ,物质的量浓度最大的是
,物质的量浓度最大的是___________ (填化学式)。
②将过量 通入
通入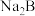 溶液,反应的离子方程式是
溶液,反应的离子方程式是___________ 。
(2)二元弱酸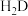 溶液中
溶液中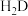 、
、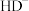 、
、 的物质的量分数
的物质的量分数 随pH的变化如图所示。
随pH的变化如图所示。

[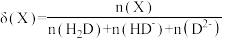 ,X为
,X为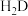 、
、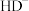 或
或 ]。
]。
则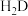 的电离平衡常数
的电离平衡常数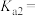
___________ 。
(3)常温下,用 的盐酸滴定
的盐酸滴定 未知浓度的氨水,滴定曲线如图所示,盐酸滴加至
未知浓度的氨水,滴定曲线如图所示,盐酸滴加至 时与氨水恰好完全中和(d点,pH约为5)。
时与氨水恰好完全中和(d点,pH约为5)。
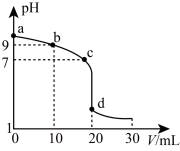
①依据变色pH范围判断下列试剂不适合作该实验终点指示剂的是:___________ 。
A.甲基橙(变色pH范围3.1~4.4) B.甲基红(变色pH范围3.4~6.2)
C.酚酞(变色pH范围8.2~10.0) D.刚果红(变色pH范围3.0~5.2)
②___________ (填序号)溶液中的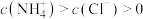 。
。
A.a点 B.b点 C.c点 D.d点
(4)滴定法常用于物质含量的测定,以下为测量市售食醋总酸含量的方法(食醋总酸含量=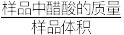 ,单位g/L)。
,单位g/L)。
取 市售食醋(假设其中酸均为醋酸)配成
市售食醋(假设其中酸均为醋酸)配成 溶液。每次取
溶液。每次取 于锥形瓶中,滴加2~3滴酚酞,在碱式滴定管中装入
于锥形瓶中,滴加2~3滴酚酞,在碱式滴定管中装入 的
的 溶液进行滴定至终点,三次滴定的消耗氢氧化钠体积平均值为
溶液进行滴定至终点,三次滴定的消耗氢氧化钠体积平均值为 ,滴定终点的现象为
,滴定终点的现象为___________ 。求算食醋总酸含量___________ 。
(1)已知部分弱酸常温下的电离常数如下表:
| 化学式 | HA |  |  |
| 电离常数K | 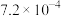 |   | 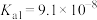 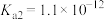 |
 、
、 ,物质的量浓度最大的是
,物质的量浓度最大的是②将过量
 通入
通入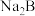 溶液,反应的离子方程式是
溶液,反应的离子方程式是(2)二元弱酸
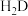 溶液中
溶液中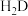 、
、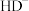 、
、 的物质的量分数
的物质的量分数 随pH的变化如图所示。
随pH的变化如图所示。
[
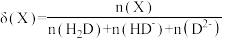 ,X为
,X为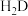 、
、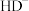 或
或 ]。
]。则
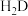 的电离平衡常数
的电离平衡常数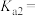
(3)常温下,用
 的盐酸滴定
的盐酸滴定 未知浓度的氨水,滴定曲线如图所示,盐酸滴加至
未知浓度的氨水,滴定曲线如图所示,盐酸滴加至 时与氨水恰好完全中和(d点,pH约为5)。
时与氨水恰好完全中和(d点,pH约为5)。
①依据变色pH范围判断下列试剂不适合作该实验终点指示剂的是:
A.甲基橙(变色pH范围3.1~4.4) B.甲基红(变色pH范围3.4~6.2)
C.酚酞(变色pH范围8.2~10.0) D.刚果红(变色pH范围3.0~5.2)
②
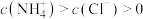 。
。A.a点 B.b点 C.c点 D.d点
(4)滴定法常用于物质含量的测定,以下为测量市售食醋总酸含量的方法(食醋总酸含量=
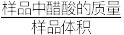 ,单位g/L)。
,单位g/L)。取
 市售食醋(假设其中酸均为醋酸)配成
市售食醋(假设其中酸均为醋酸)配成 溶液。每次取
溶液。每次取 于锥形瓶中,滴加2~3滴酚酞,在碱式滴定管中装入
于锥形瓶中,滴加2~3滴酚酞,在碱式滴定管中装入 的
的 溶液进行滴定至终点,三次滴定的消耗氢氧化钠体积平均值为
溶液进行滴定至终点,三次滴定的消耗氢氧化钠体积平均值为 ,滴定终点的现象为
,滴定终点的现象为
您最近一年使用:0次



