一定条件下,某可逆反应在密闭容器中建立化学平衡,在 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:
A.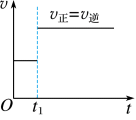 B.
B.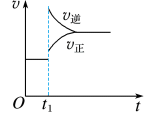
C.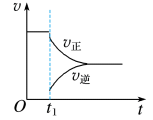 D.
D.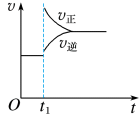
(1)对于反应: ,
, 时刻增大压强,其图像为
时刻增大压强,其图像为___________ ,平衡___________ (填“向正反应方向”“向逆反应方向”或“不”,下同)移动。
(2)对于反应 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为___________ ,平衡___________ 移动。
 时刻改变某一个条件,建立新的平衡,其
时刻改变某一个条件,建立新的平衡,其 图像如下:
图像如下:A.
 B.
B.
C.
 D.
D.
(1)对于反应:
 ,
, 时刻增大压强,其图像为
时刻增大压强,其图像为(2)对于反应
 ,
, 时刻增大容器体积,其图像为
时刻增大容器体积,其图像为
更新时间:2023-11-03 09:30:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】请根据题目要求回答下列问题:
(1)工业接触法制硫酸的生产中用到的设备有:①沸腾炉②_______ ,③吸收塔,写出设备②中,发生的主要反应的化学方程式_______________ 。
(2)已知SO2转化为SO3的反应为放热反应,下图中正确的是_____ (填序号)。
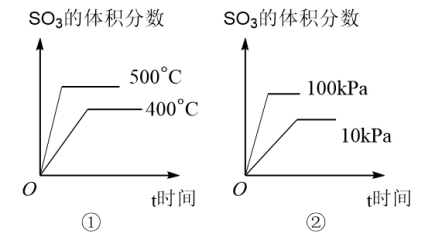
(3)在吸收塔中,为了提高SO3的吸收率,工业上选择的吸收剂是______ (填序号)。
A. H2O B. 稀H2SO4 C. 98.3%H2SO4 D. NH3·H2O溶液
(4)在101kPa时,燃烧1kg含FeS2质量分数为60%的黄铁矿,放出4265kJ的热量(假设杂质不参加反应),则表示FeS2燃烧热的热化学方程式为________________ 。
(1)工业接触法制硫酸的生产中用到的设备有:①沸腾炉②
(2)已知SO2转化为SO3的反应为放热反应,下图中正确的是

(3)在吸收塔中,为了提高SO3的吸收率,工业上选择的吸收剂是
A. H2O B. 稀H2SO4 C. 98.3%H2SO4 D. NH3·H2O溶液
(4)在101kPa时,燃烧1kg含FeS2质量分数为60%的黄铁矿,放出4265kJ的热量(假设杂质不参加反应),则表示FeS2燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)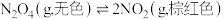 的平衡体系,降低温度,气体颜色变浅,则正反应是
的平衡体系,降低温度,气体颜色变浅,则正反应是___________ 热反应;若增大压强,平衡向___________ 移动(填“正反应方向”、“逆反应方向”或“不”),正反应速率___________ (填“增大”或“减小”)。
(2)某温度下,纯水的 为
为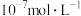 ,则此时
,则此时 为
为___________  ,若温度不变,滴入稀
,若温度不变,滴入稀 使
使 ,则由水电离出的
,则由水电离出的 为
为___________  ,某温度(T0℃)时,水的
,某温度(T0℃)时,水的 ,则该温度
,则该温度___________ (填“高于”、“低于”或“等于”)25℃其理由是___________ 。碳酸氢钠溶液显___________ 性,水解方程式表示为___________ 。
(1)
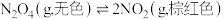 的平衡体系,降低温度,气体颜色变浅,则正反应是
的平衡体系,降低温度,气体颜色变浅,则正反应是(2)某温度下,纯水的
 为
为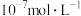 ,则此时
,则此时 为
为 ,若温度不变,滴入稀
,若温度不变,滴入稀 使
使 ,则由水电离出的
,则由水电离出的 为
为 ,某温度(T0℃)时,水的
,某温度(T0℃)时,水的 ,则该温度
,则该温度
您最近一年使用:0次
填空题
|
适中
(0.65)
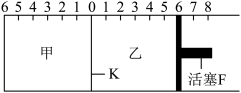
【推荐3】(1)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入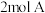 和
和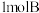 ,乙中充入
,乙中充入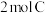 和
和 ,此时K停在0处。在一定条件下发生可逆反应:
,此时K停在0处。在一定条件下发生可逆反应: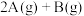

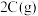 ;反应达到平衡后,再恢复至原温度。
;反应达到平衡后,再恢复至原温度。
回答下列问题:
①可根据________ 现象来判断甲、乙中反应都已达到平衡。
②达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是_________ 。
(2)若一开始就将K、F固定,其它条件均同(1),则达到平衡时:
①甲、乙中C的物质的量的关系是甲__________ 乙(填“>”、“<”或“=” )。
②如果测得甲中A的转化率为b,则乙中C的转化率为____________ 。
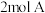 和
和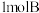 ,乙中充入
,乙中充入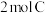 和
和 ,此时K停在0处。在一定条件下发生可逆反应:
,此时K停在0处。在一定条件下发生可逆反应: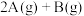

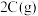 ;反应达到平衡后,再恢复至原温度。
;反应达到平衡后,再恢复至原温度。
回答下列问题:
①可根据
②达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是
(2)若一开始就将K、F固定,其它条件均同(1),则达到平衡时:
①甲、乙中C的物质的量的关系是甲
②如果测得甲中A的转化率为b,则乙中C的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(一)一种工业制硝酸的方法经历下列几个步骤:
 △H1<0
△H1<0
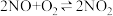 △H2<0
△H2<0
 △H3<0
△H3<0
已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有_______________ 目的;
(2)实验发现,单位时间内NH3的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因________________ 。

(3) 的反应历程如下:
的反应历程如下:
反应Ⅰ: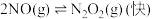 △H1<0
△H1<0

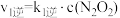
反应Ⅱ: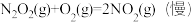 △H2<0
△H2<0
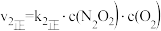
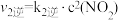
①一定条件下,反应 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=________________ 。(用含k1正、k1逆、k2正、k2逆的代数式表示);
②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数________________ k2逆增大的倍数(填“大于”“小于”或“等于”)。
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为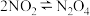 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
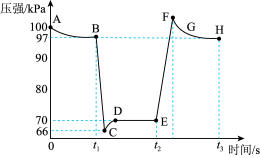
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是_______________ 。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=_______________ (不必化成小数);
(6)图像中C、E两点气体平均摩尔质量最大的点为_______________ (填代号)。
 △H1<0
△H1<0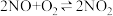 △H2<0
△H2<0 △H3<0
△H3<0已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
(2)实验发现,单位时间内NH3的氧化率[
 ]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的可能原因
(3)
 的反应历程如下:
的反应历程如下:反应Ⅰ:
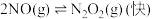 △H1<0
△H1<0 
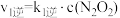
反应Ⅱ:
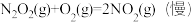 △H2<0
△H2<0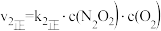
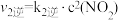
①一定条件下,反应
 达到平衡状态,平衡常数K=
达到平衡状态,平衡常数K=②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为
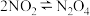 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
(5)求D点Kp=
(6)图像中C、E两点气体平均摩尔质量最大的点为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n(mol)随时间t的变化如图所示,已知达到平衡后,降低温度,A的转化率增大。
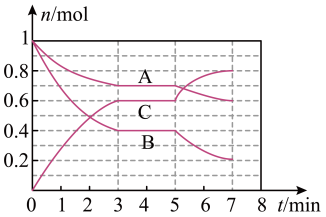
(1)根据图中数据,写出该反应的化学方程式:______ 。此反应的平衡常数的表达式K=_______ ,0~3 min内,A的速率为_______ 。在5~7min内,若K值不变,则此处曲线变化可能的原因是________ 。
(2)图中表示此反应的反应速率v和时间t的关系图:
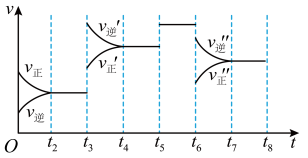
上图中t3时刻改变的条件是______ 。A的转化率最大的一段时间是_______ 。

(1)根据图中数据,写出该反应的化学方程式:
(2)图中表示此反应的反应速率v和时间t的关系图:

上图中t3时刻改变的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氨催化分解既可防治氨气污染,又能得到氢能源,得到广泛研究。
(1)已知:
①4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
②H2(g)+1/2O2(g)===H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)===H2O(g) △H3=+44.0kJ·mol-1
反应①在任何温度下都能自发进行的原因为___________ ;NH3分解为N2和H2的热化学方程式______________________ 。
(2)在Co-Al催化剂体系中,压强P0下氨气以一定流速通过反应器,在相同时间下测转化率。得到不同催化剂下氨气转化率随温度变化曲线如下图。使反应的活化能最小的催化剂为___________ 。同一催化剂下,温度高时NH3的转化率接近平衡转化率的原因___________ 。如果增大氨气浓度(其它条件不变),则b点对应的点可能为___________ 。(填“a”、“c”或“d”)
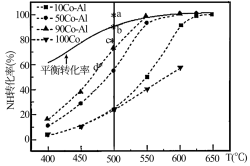
(3)T℃时,体积为2L的密闭容器中加入1.0molNH3和0.2molH2,30min达到平衡时,N2体积分数为20%,则T℃时平衡常数K=___________ ,NH3转化率为___________ ;达到平衡后再加入1.0molNH3和0.2molH2,此时体系中v正___________ v逆(填“>“<”或“=”)。
(1)已知:
①4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,②H2(g)+1/2O2(g)===H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)===H2O(g) △H3=+44.0kJ·mol-1
反应①在任何温度下都能自发进行的原因为
(2)在Co-Al催化剂体系中,压强P0下氨气以一定流速通过反应器,在相同时间下测转化率。得到不同催化剂下氨气转化率随温度变化曲线如下图。使反应的活化能最小的催化剂为

(3)T℃时,体积为2L的密闭容器中加入1.0molNH3和0.2molH2,30min达到平衡时,N2体积分数为20%,则T℃时平衡常数K=
您最近一年使用:0次



