 作为自然界丰富的“碳源”化合物,将
作为自然界丰富的“碳源”化合物,将 转化为
转化为 、
、 等燃料,不仅能缓解碳排放带来的环境问题,还将成为理想的能源补充形式。
等燃料,不仅能缓解碳排放带来的环境问题,还将成为理想的能源补充形式。(1)已知25℃和101
 时,①
时,① 的燃烧热
的燃烧热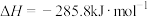 ;
;②
 的燃烧热
的燃烧热
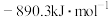 ;
;
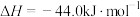 。
。则
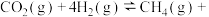
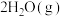

 。
。(2)控制起始时
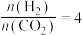 ,
, (
( 表示标准大气压),在恒容密闭容器中,发生反应[同时有副反应
表示标准大气压),在恒容密闭容器中,发生反应[同时有副反应
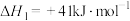 发生],平衡时各物质的物质的量分数随温度的变化如图所示:
发生],平衡时各物质的物质的量分数随温度的变化如图所示: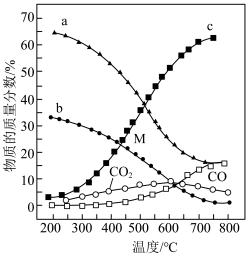
①平衡时
 的物质的量分数随温度变化的曲线为
的物质的量分数随温度变化的曲线为②温度高于500℃时,
 的物质的量分数不断增大的原因是
的物质的量分数不断增大的原因是(3)催化制氢是目前大规模制取氢气的方法之一:


 。在
。在 ℃时,将0.10
℃时,将0.10
 与0.40
与0.40
 充入5L的容器中,反应平衡后
充入5L的容器中,反应平衡后 的体积分数
的体积分数 。
。①反应平衡常数

②保持K不变,提高
 平衡转化率的措施有
平衡转化率的措施有③由
 ℃时上述实验数据计算得到
℃时上述实验数据计算得到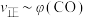 (体积分数,下同)和
(体积分数,下同)和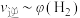 的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,表示
的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,表示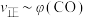 的点是
的点是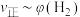 的点是
的点是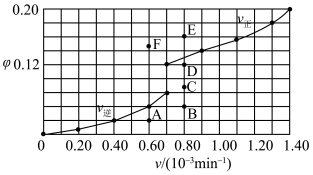
(4)近年来,生物电催化技术运用微生物电解池实现了
 的甲烷化,其工作原理如图所示。
的甲烷化,其工作原理如图所示。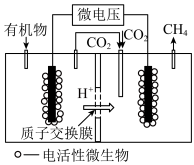
①微生物电解池实现
 甲烷化的阴极的电极反应式为
甲烷化的阴极的电极反应式为②如果处理有机物[
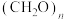 ]产生标准状况下112
]产生标准状况下112
 ,那么理论上导线中通过电子的物质的量为
,那么理论上导线中通过电子的物质的量为
更新时间:2023-11-09 07:25:31
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】工业上二氧化碳、甲烷催化重整不仅可以获得合成气(CO和H2),还可减少温室气体排放,对治理生态环境具有重要意义。
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1=a kJ/mol
CO(g)+H2O(g)=CO2(g)+H2O(g) △H2=b kJ/mol
2CO(g)+O2(g)=2CO2(g) △H3=c kJ/mol
催化重整反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的△H4=_______ 。
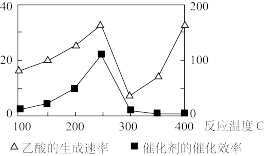
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,还可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250-300℃时,温度升高而乙酸的生成速率降低的原因可能是_______ 。
(3)催化重整 CO2(g)+CH4(g)=2CO(g)+2H2(g)的反应,测得CH4的平衡转化率与温度及压强的关系如图中曲线所示:
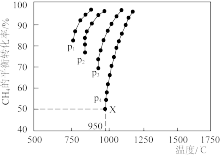
①根据图2可知,p1、p2、p3、p4由大到小的顺序为_______ 。
②在压强为p4、投料比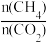 为1、950℃的条件下,X点平衡常数Kp=
为1、950℃的条件下,X点平衡常数Kp=_______ (用含p4的代数式表示,其中用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)。
物质的量分数)。
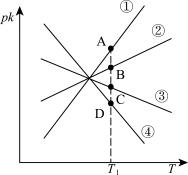
(4)若反应CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.17 kJ/mol 的正、逆反应速率分别可表示为v正=k正c(CO2)·c(H2)、k逆分别为正、逆反应速率常数,c为物质的量浓度。则如图(pK=-lgk:T表示温度
CO(g)+H2O(g) △H2=+41.17 kJ/mol 的正、逆反应速率分别可表示为v正=k正c(CO2)·c(H2)、k逆分别为正、逆反应速率常数,c为物质的量浓度。则如图(pK=-lgk:T表示温度 所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线
所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线_______ ,能表示pk逆随T变化关系的是斜线_______ 。
(5)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2 2Na2CO3+C,放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C,放电时该电池“吸入”CO2,其工作原理如图所示:
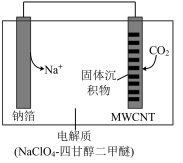
放电时,正极的电极反应式为_______ 。
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1=a kJ/mol
CO(g)+H2O(g)=CO2(g)+H2O(g) △H2=b kJ/mol
2CO(g)+O2(g)=2CO2(g) △H3=c kJ/mol
催化重整反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的△H4=
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,还可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250-300℃时,温度升高而乙酸的生成速率降低的原因可能是

(3)催化重整 CO2(g)+CH4(g)=2CO(g)+2H2(g)的反应,测得CH4的平衡转化率与温度及压强的关系如图中曲线所示:

①根据图2可知,p1、p2、p3、p4由大到小的顺序为
②在压强为p4、投料比
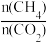 为1、950℃的条件下,X点平衡常数Kp=
为1、950℃的条件下,X点平衡常数Kp= 总压
总压 物质的量分数)。
物质的量分数)。(4)若反应CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.17 kJ/mol 的正、逆反应速率分别可表示为v正=k正c(CO2)·c(H2)、k逆分别为正、逆反应速率常数,c为物质的量浓度。则如图(pK=-lgk:T表示温度
CO(g)+H2O(g) △H2=+41.17 kJ/mol 的正、逆反应速率分别可表示为v正=k正c(CO2)·c(H2)、k逆分别为正、逆反应速率常数,c为物质的量浓度。则如图(pK=-lgk:T表示温度 所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线
所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线
(5)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2
 2Na2CO3+C,放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C,放电时该电池“吸入”CO2,其工作原理如图所示:
放电时,正极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
②2CH3OH(g) CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为__________ 。
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率为______________ ;若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=amol/L;达到平衡后,c(CH3OH)=2 mol/L,a=________ mol/L。
(3)催化反应室中总反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)的△H=
CH3OCH3(g)+CO2(g)的△H=________ ;830℃时反应③的K=1.0,则在催化反应室中反应③的K______ 1.0(填“>”、“<”或“=”)。
(4)二甲醚的燃烧热为1455 kJ·mol-1,则二甲醚燃烧的热化学方程式为
_____________________________________________________ 。

(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示。b电极是________ 极,写出a电极上发生的电极反应式_________________________________________ 。
①CO(g)+2H2(g)
 CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1②2CH3OH(g)
 CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1③CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为
| A.加入某物质作催化剂 | B.加入一定量CO |
| C.反应温度降低 | D.增大容器体积 |
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率为
(3)催化反应室中总反应3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g)的△H=
CH3OCH3(g)+CO2(g)的△H=(4)二甲醚的燃烧热为1455 kJ·mol-1,则二甲醚燃烧的热化学方程式为

(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示。b电极是
您最近一年使用:0次
【推荐3】消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。
(1) 化学上采用NH3处理NxOy不仅可以消除污染,还可作为工业生产的能量来源。
已知:2NO(g)=N2(g)+O2(g) △H=-177kJ/mol
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) △H=-1253.4kJ/mol
则用NH3处理NO生成氮气和气态水的热化学方程式为___________________ 。
(2)已知:N2(g)+3H2(g) 2NH3(g) △H<0。不同温度下,向三个容器中分别投入相同量的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。
2NH3(g) △H<0。不同温度下,向三个容器中分别投入相同量的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。

①M点的v正_________ Q点的v正(填“>”“<”或“=”)。
②T3温度下,将1molN2和3molH2充入2L的密闭容器中,维持压强为60MPa不变,达到N点的平衡状态,反应的浓度平衡常数K=_____________ (用最简分数表示),M点的平衡常数比N点的平衡常数_________ (填“大”“小”或“相等”)。
(3)水体中过量氨氮(以NH3表示)会导致水体富营养化。
①用次氯酸钠除去氨氮的原理如图所示。写出总反应化学方程式:_____________ 。
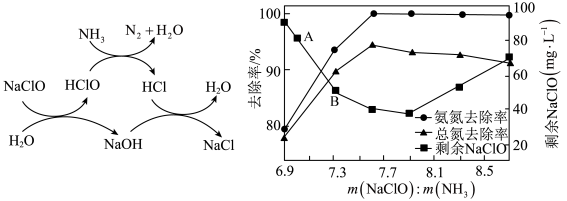
②取一定量的含氨氮废水,改变加入次氯酸钠的用量,反应一段时间后,溶液中氨氮去除率、总氮(溶液中所有可溶性的含氮化合物中氮元素的总量)去除率以及剩余次氯酸钠的含量随m(NaClO)∶m(NH3)的变化情况如上图所示。点B剩余NaClO含量低于点A的原因是____ 。当m(NaClO)∶m(NH3)>7.6时,水体中总氮去除率反而下降,可能的原因是__________ 。
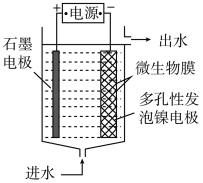
(4)电极生物膜电解脱硝是电化学和微生物工艺的组合。某微生物膜能利用电解产生的活性原子将NO3-还原为N2,工作原理如题图所示。若阳极生成标准状况下2.24 L气体,理论上可除去NO3-的物质的量为_____ mol。
(1) 化学上采用NH3处理NxOy不仅可以消除污染,还可作为工业生产的能量来源。
已知:2NO(g)=N2(g)+O2(g) △H=-177kJ/mol
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) △H=-1253.4kJ/mol
则用NH3处理NO生成氮气和气态水的热化学方程式为
(2)已知:N2(g)+3H2(g)
 2NH3(g) △H<0。不同温度下,向三个容器中分别投入相同量的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。
2NH3(g) △H<0。不同温度下,向三个容器中分别投入相同量的反应物进行反应,测得不同压强下平衡混合物中NH3的物质的量分数如图所示。
①M点的v正
②T3温度下,将1molN2和3molH2充入2L的密闭容器中,维持压强为60MPa不变,达到N点的平衡状态,反应的浓度平衡常数K=
(3)水体中过量氨氮(以NH3表示)会导致水体富营养化。
①用次氯酸钠除去氨氮的原理如图所示。写出总反应化学方程式:

②取一定量的含氨氮废水,改变加入次氯酸钠的用量,反应一段时间后,溶液中氨氮去除率、总氮(溶液中所有可溶性的含氮化合物中氮元素的总量)去除率以及剩余次氯酸钠的含量随m(NaClO)∶m(NH3)的变化情况如上图所示。点B剩余NaClO含量低于点A的原因是
(4)电极生物膜电解脱硝是电化学和微生物工艺的组合。某微生物膜能利用电解产生的活性原子将NO3-还原为N2,工作原理如题图所示。若阳极生成标准状况下2.24 L气体,理论上可除去NO3-的物质的量为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】固氮一直是科学家致力研究的重要课题,工业固氮合成氨是人类科学技术的一项重大突破,目前已有三位科学家研究合成氨而获得诺贝尔奖,其反应为:

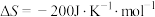 。回答下列问题:
。回答下列问题:
(1)计算合成氨反应在常温下能否自发?写出简要计算过程:_______ 。
(2)有关热力学数据如下:
常温下,大气固氮的倾向_______ 工业固氮(填“大于”或“小于”)。
(3)T℃时,在有催化剂的恒容密闭容器中充入 和
和 。下图为不同投料比[
。下图为不同投料比[ ]时某反应物X的平衡转化率变化曲线。
]时某反应物X的平衡转化率变化曲线。

①反应物X是_______ (填“ ”或“
”或“ ”)。
”)。
②判断依据是_______ 。
(4)进料体积比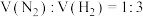 时,平衡气体中
时,平衡气体中 的物质的量分数随温度和压强变化的关系如图所示:
的物质的量分数随温度和压强变化的关系如图所示:

①该反应的平衡常数K(a)_______ K(b)(填“<”、“=”或“>”)。
②500℃、压强为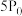 时,
时, 的转化率为:
的转化率为:_______ (保留三位有效数字),
_______ [ 为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]。
为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]。


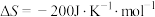 。回答下列问题:
。回答下列问题:(1)计算合成氨反应在常温下能否自发?写出简要计算过程:
(2)有关热力学数据如下:
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 25 | 2000 | 25 | 350 | 400 | 450 |
| 平衡常数K |  | 0.1 | 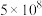 | 1.847 | 0.504 | 0.152 |
常温下,大气固氮的倾向
(3)T℃时,在有催化剂的恒容密闭容器中充入
 和
和 。下图为不同投料比[
。下图为不同投料比[ ]时某反应物X的平衡转化率变化曲线。
]时某反应物X的平衡转化率变化曲线。
①反应物X是
 ”或“
”或“ ”)。
”)。②判断依据是
(4)进料体积比
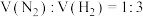 时,平衡气体中
时,平衡气体中 的物质的量分数随温度和压强变化的关系如图所示:
的物质的量分数随温度和压强变化的关系如图所示:
①该反应的平衡常数K(a)
②500℃、压强为
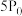 时,
时, 的转化率为:
的转化率为:
 为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]。
为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】环境问题,能源问题事关人类生存、社会可持续发展。回答下列问题:
(1)氮硫的氧化物的转化:
①已知:NO(g)+ O2(g)
O2(g) NO2(g) △H=−56.5 kJ⋅mol−1K=a (mol⋅L−1)−0.5
NO2(g) △H=−56.5 kJ⋅mol−1K=a (mol⋅L−1)−0.5
2SO2(g)+O2(g) 2SO3(g) △H=−196.6 kJ⋅mol−1K=b (mol⋅L−1)−1
2SO3(g) △H=−196.6 kJ⋅mol−1K=b (mol⋅L−1)−1
则反应NO2(g)+SO2(g) SO3(g)+NO(g) △H=
SO3(g)+NO(g) △H=___________ kJ⋅mol−1K=___________
②一定条件下,将NO2与SO2以一定比例(不是等物质的量)置于恒温恒容的密闭容器中发生上述反应,下列能说明反应一定达到平衡状态的有___________ 。
a.混合气体的密度不变
b.反应速率v(NO2):v(SO2):v(SO3):v(NO)=1:1:1:1
c.NO2和SO2的体积分数之比保持不变
d.混合气体颜色保持不变
(2)通常合成甲醇的主要反应为:CO(g)+2H2(g) CH3OH(g)△H<0,起始时容器中只有1 mol/L CO和2 mol/L H2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
CH3OH(g)△H<0,起始时容器中只有1 mol/L CO和2 mol/L H2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。

①压强为p1温度T1和T2时对应的平衡常数分别为K1、K2,则K1___________ K2(填“>”“<”“=”)请说明理由___________ 。
②若在温度为T1、压强为p1的条件下向密闭容器中加入等物质的量的CO、H2、CH3OH气体,则反应开始时v(CO)正___________ v(CO)逆(填“>”“<”“=”“无法确定”)
(3)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体CO2,其产物之一是NH4HCO3,常温下碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,NH3·H2O的电离常数Kb=1.8×10-5,则NH4HCO3溶液中c( )
)___________ c( )(填“>”“<”“=”)。
)(填“>”“<”“=”)。
(1)氮硫的氧化物的转化:
①已知:NO(g)+
 O2(g)
O2(g) NO2(g) △H=−56.5 kJ⋅mol−1K=a (mol⋅L−1)−0.5
NO2(g) △H=−56.5 kJ⋅mol−1K=a (mol⋅L−1)−0.5 2SO2(g)+O2(g)
 2SO3(g) △H=−196.6 kJ⋅mol−1K=b (mol⋅L−1)−1
2SO3(g) △H=−196.6 kJ⋅mol−1K=b (mol⋅L−1)−1则反应NO2(g)+SO2(g)
 SO3(g)+NO(g) △H=
SO3(g)+NO(g) △H=②一定条件下,将NO2与SO2以一定比例(不是等物质的量)置于恒温恒容的密闭容器中发生上述反应,下列能说明反应一定达到平衡状态的有
a.混合气体的密度不变
b.反应速率v(NO2):v(SO2):v(SO3):v(NO)=1:1:1:1
c.NO2和SO2的体积分数之比保持不变
d.混合气体颜色保持不变
(2)通常合成甲醇的主要反应为:CO(g)+2H2(g)
 CH3OH(g)△H<0,起始时容器中只有1 mol/L CO和2 mol/L H2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
CH3OH(g)△H<0,起始时容器中只有1 mol/L CO和2 mol/L H2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
①压强为p1温度T1和T2时对应的平衡常数分别为K1、K2,则K1
②若在温度为T1、压强为p1的条件下向密闭容器中加入等物质的量的CO、H2、CH3OH气体,则反应开始时v(CO)正
(3)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体CO2,其产物之一是NH4HCO3,常温下碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,NH3·H2O的电离常数Kb=1.8×10-5,则NH4HCO3溶液中c(
 )
) )(填“>”“<”“=”)。
)(填“>”“<”“=”)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫酸是工业生产中最为重要的产品之一。
(1)工业上制硫酸主要分为_________ 、________ 、_________ 三个阶段。
(2)下列是第二阶段反应的有关实验数据,请选择最合适的生产条件____________ 。
(3)现在欲提高反应速率和SO2的转化率,下列措施可行的是( ) 。
A.向装置中通入氮气且保持体积不变
B.向装置中通入氧气且保持体积不变
C.添加更多的催化剂
D.降低温度,及时转移SO3
(4)硫酸生产的尾气中含有少量SO2,可有石灰水吸收后,再用硫酸处理。此过程涉及的化学反应方程式为__________________ ,______________ 。
(5)若进入第二阶段所用设备中气体的体积分数为:SO27%、O211%、N282%。现有100体积这样的混合气体在反应后变成96.7体积,则反应后混合气体中N2和SO3的体积比为___________ ,此时SO2转化率为__________ 。
(1)工业上制硫酸主要分为
(2)下列是第二阶段反应的有关实验数据,请选择最合适的生产条件
| 压强/MPa SO2转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.8 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
A.向装置中通入氮气且保持体积不变
B.向装置中通入氧气且保持体积不变
C.添加更多的催化剂
D.降低温度,及时转移SO3
(4)硫酸生产的尾气中含有少量SO2,可有石灰水吸收后,再用硫酸处理。此过程涉及的化学反应方程式为
(5)若进入第二阶段所用设备中气体的体积分数为:SO27%、O211%、N282%。现有100体积这样的混合气体在反应后变成96.7体积,则反应后混合气体中N2和SO3的体积比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】恒温下,向一个4L的密闭容器中充入5.2mol H2和2mol N2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
(1)①研究一个化学反应要从_______ 、化学反应的快慢、化学反应的限度三个方面考虑。
②下列可以证明反应达到平衡的标志是_______ 。
A.N2、H2和NH3的浓度不再变化
B.单位时间内消耗nmol N2同时消耗3nmol H2
C.1mol氮氮三键断裂同时6mol N-H键断裂
D.容器内总压强不随时间而变化
E.混合气体的密度保持不变
F.混合气体的平均相对分子质量不再改变
③此条件下该反应的化学平衡常数K=______ ,若温度不变,只将容器体积由4L变为2L,达到新平衡时N2的平衡浓度_______ 0.4mol•L-1(填“>”、“=”或“<”)。
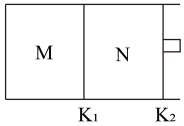
(2)如下图所示,隔板K1固定不动,活塞K2可自由移动。T℃时,M、N两个容器中均发生反应N2(g)+3H2(g)⇌2NH3(g),向容器M、N中各充入lmolN2和3molH2,初始M、N的容积和温度相同,并保持温度不变。下列有关说法中不正确 的是________。
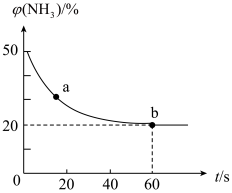
(3)合理应用和处理氮的化合物,在生产生活中有重要意义。密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g)+2NH3(g)⇌CO(NH2)2(s)+H2O(g),混合气体中NH3的物质的量分数[(NH3)]随时间变化关系如下图所示。则a点的正反应速率υ正(CO2)_______ b点的逆反应速率υ逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是_____ 。
(4)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。以尿素为原料在一定条件下发生反应:CO(NH2)2(s)+H2O(l)⇌2NH3(g)+CO2(g) △H=+133.6kJ/mol。尿素在一定条件下可将氮的氧化物还原为氮气。已知:
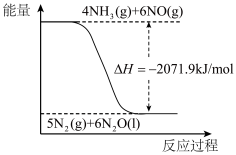
结合上述信息,尿素还原NO(g)的热化学方程式是___________ 。
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
②下列可以证明反应达到平衡的标志是
A.N2、H2和NH3的浓度不再变化
B.单位时间内消耗nmol N2同时消耗3nmol H2
C.1mol氮氮三键断裂同时6mol N-H键断裂
D.容器内总压强不随时间而变化
E.混合气体的密度保持不变
F.混合气体的平均相对分子质量不再改变
③此条件下该反应的化学平衡常数K=
(2)如下图所示,隔板K1固定不动,活塞K2可自由移动。T℃时,M、N两个容器中均发生反应N2(g)+3H2(g)⇌2NH3(g),向容器M、N中各充入lmolN2和3molH2,初始M、N的容积和温度相同,并保持温度不变。下列有关说法中

| A.反应达到平衡时N2的转化率:M>N |
| B.H2的体积分数:M>N |
| C.容器N中达到平衡,测得容器中含有1.2molNH3,此时N的容积为VL,则该反应在此条件下的平衡常数K=25V2/12 |
| D.该反应在T℃时的平衡常数K:M=N |

(4)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。以尿素为原料在一定条件下发生反应:CO(NH2)2(s)+H2O(l)⇌2NH3(g)+CO2(g) △H=+133.6kJ/mol。尿素在一定条件下可将氮的氧化物还原为氮气。已知:

结合上述信息,尿素还原NO(g)的热化学方程式是
您最近一年使用:0次
【推荐2】NH3、NOx、SO2处理不当易造成环境污染,如果对这些气体加以利用就可以变废为宝,既减少了对环境的污染,又解决了部分能源危机问题。
(l)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2,已知:
 ①
①
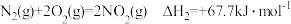 ②
②
则反应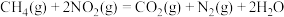 ΔH=
ΔH=___________
(2)工业上利用氨气生产氢氰酸(HCN)的反应为:CH4(g)+NH3(g) HCN(g)+3H2(g) ΔH>0
HCN(g)+3H2(g) ΔH>0
①在一定温度条件下,向2L恒容密闭容器中加入2mol CH4和2mol NH3,初始压强为4×105Pa,平衡时NH3体积分数为30%,所用时间为10min,则该时间段内用CH4的浓度变化表示的反应速率为___________ mol·L−l·min−1,该温度下平衡常数Kp=___________ (用平衡分压代替平衡浓度表示,分压=总压×物质的量分数),若保持温度不变,再向容器中加入CH4和H2各1mol,则再次平衡时HCN的体积分数 ___________ (填“增大”“不变”或“减小”)。
②其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图1所示,X代表___________ (填字母代号)。
A.温度
B.压强
C.原料中CH4与NH3的体积比


(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3进行电解生产硫酸,其中阴、阳膜组合电解装置如图2所示,电极材料为石墨,A—E分别代表生产中的原料或产品,b表示___________ (填“阴”或“阳”)离子交换膜。阳极的电极反应式为___________ 。
(l)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2,已知:
 ①
①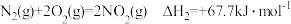 ②
②则反应
 ΔH=
ΔH=(2)工业上利用氨气生产氢氰酸(HCN)的反应为:CH4(g)+NH3(g)
 HCN(g)+3H2(g) ΔH>0
HCN(g)+3H2(g) ΔH>0①在一定温度条件下,向2L恒容密闭容器中加入2mol CH4和2mol NH3,初始压强为4×105Pa,平衡时NH3体积分数为30%,所用时间为10min,则该时间段内用CH4的浓度变化表示的反应速率为
②其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图1所示,X代表
A.温度
B.压强
C.原料中CH4与NH3的体积比


(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3进行电解生产硫酸,其中阴、阳膜组合电解装置如图2所示,电极材料为石墨,A—E分别代表生产中的原料或产品,b表示
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】将二氧化碳转化为高附加值碳基燃料可有效减少碳排放。二氧化碳催化加氢制甲醇[CO2(g)+3H2(g) CH3OH(g)+H2O(g)]引起了科学界和工业界的极大兴趣。回答下列问题:
CH3OH(g)+H2O(g)]引起了科学界和工业界的极大兴趣。回答下列问题:
(1)相关的化学键键能数据如表所示。
写出二氧化碳催化加氢制甲醇的热化学方程式____ 。
(2)采用真空封管法制备磷化硼纳米颗粒,成功的实现了高选择性电催化还原CO2制备甲醇,该反应历程如图所示。
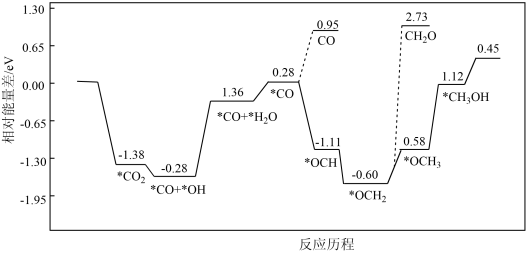
①该过程容易产生副产物____ 。
②上述合成甲醇的反应速率较慢,要使反应速率加快,需要降低某步骤的能量变化,写出该基元反应的化学方程式:____ 。
Ⅱ.工业中,CO2和H2在催化剂作用下可发生两个平行反应,分别生成CH3OH和CO。
反应a:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1;
CH3OH(g)+H2O(g) △H1;
反应b:CO2(g)+H2(g) CO(g)+H2O(g) △H2>0。
CO(g)+H2O(g) △H2>0。
在传统的催化固定反应床(CFBR)中,CO2转化率和甲醇选择性通常都比较低,科学团队发展了一种具有反应分离双功能的分子筛膜催化反应器(MR)用于CO2催化加氢制备甲醇,极大地改善了该问题,原理如图所示。
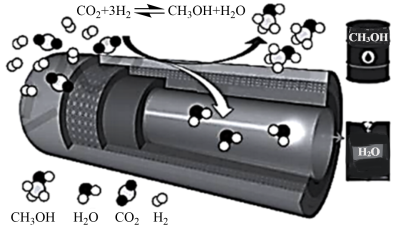
保持压强为5MPa,向密闭容器中投入一定量CO2和H2,不同反应模式下CO2的平衡转化率和甲醇选择性的相关实验数据如表所示。
已知CH3OH选择性:转化的CO2中生成CH3OH的百分比。
(3)CFBR模式时,投料比 =3一定温度下发生反应,下列说法能作为反应a达到平衡状态的判据是
=3一定温度下发生反应,下列说法能作为反应a达到平衡状态的判据是____ (填选项字母)。
A.气体压强不再变化
B.CO的体积分数不再变化
C.气体平均相对分子质量不再变化
D. 不再变化
不再变化
E.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
(4)由表中数据可知CMR模式下,CO2的转化率显著提高,结合具体反应分析可能的原因:____ 。
(5)压力平衡常数Kp是指用平衡分压代替平衡浓度进行计算的平衡常数,平衡分压=p总×物质的量分数。根据表中数据计算温度为230℃时,反应a的Kp值为____ (无需计算,写表达式)。
 CH3OH(g)+H2O(g)]引起了科学界和工业界的极大兴趣。回答下列问题:
CH3OH(g)+H2O(g)]引起了科学界和工业界的极大兴趣。回答下列问题:(1)相关的化学键键能数据如表所示。
| 化学键 | H—H | C=O | H—O | C—H | C—O |
| E(kJ/mol) | 436 | 745 | 465 | 413 | 351 |
写出二氧化碳催化加氢制甲醇的热化学方程式
(2)采用真空封管法制备磷化硼纳米颗粒,成功的实现了高选择性电催化还原CO2制备甲醇,该反应历程如图所示。

①该过程容易产生副产物
②上述合成甲醇的反应速率较慢,要使反应速率加快,需要降低某步骤的能量变化,写出该基元反应的化学方程式:
Ⅱ.工业中,CO2和H2在催化剂作用下可发生两个平行反应,分别生成CH3OH和CO。
反应a:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1;
CH3OH(g)+H2O(g) △H1;反应b:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2>0。
CO(g)+H2O(g) △H2>0。在传统的催化固定反应床(CFBR)中,CO2转化率和甲醇选择性通常都比较低,科学团队发展了一种具有反应分离双功能的分子筛膜催化反应器(MR)用于CO2催化加氢制备甲醇,极大地改善了该问题,原理如图所示。

保持压强为5MPa,向密闭容器中投入一定量CO2和H2,不同反应模式下CO2的平衡转化率和甲醇选择性的相关实验数据如表所示。
| 实验组 | 反应模式 |  | 压强/MPa | 温度/℃ | CO2转化率 | CH3OH选择性 |
| ① | CFBR | 3 | 5 | 250 | 25.6 | 61.3 |
| ② | CFBR | 3 | 5 | 230 | 20.0 | 70.0 |
| ③ | CMR | 3 | 3 | 260 | 36.1 | 100 |
已知CH3OH选择性:转化的CO2中生成CH3OH的百分比。
(3)CFBR模式时,投料比
 =3一定温度下发生反应,下列说法能作为反应a达到平衡状态的判据是
=3一定温度下发生反应,下列说法能作为反应a达到平衡状态的判据是A.气体压强不再变化
B.CO的体积分数不再变化
C.气体平均相对分子质量不再变化
D.
 不再变化
不再变化E.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
(4)由表中数据可知CMR模式下,CO2的转化率显著提高,结合具体反应分析可能的原因:
(5)压力平衡常数Kp是指用平衡分压代替平衡浓度进行计算的平衡常数,平衡分压=p总×物质的量分数。根据表中数据计算温度为230℃时,反应a的Kp值为
您最近一年使用:0次
【推荐1】图中A、B为多孔碳惰性电极,C、D为铂夹,夹在浸过Na2SO4溶液和酚酞的湿滤纸条两端;a、b为电源两极。实验前,往两支试管中充满KOH溶液并倒立于盛有KOH溶液的水槽中。实验时,断开K1,闭合K2、K3,通电一段时间,两支试管收集的气体体积如图所示。根据要求回答问题:
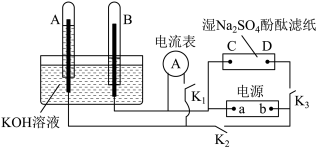
(1)电源的a极为_______ 极(填“正”或“负”);
(2)铂夹C上发生反应的电极反应式为_______ ;
(3)装置通直流电时,下列判断不正确的是_______ 。
①电极A上发生氧化反应 ②电子沿a→C→D→b 路径流动
③片刻后D点附近c( )增大 ④片刻后可观察到滤纸C点变红色
)增大 ④片刻后可观察到滤纸C点变红色
(4)现切断K2、K3,闭合K1,观察到电流表指针偏转。电极A上的电极反应式为_______ 。
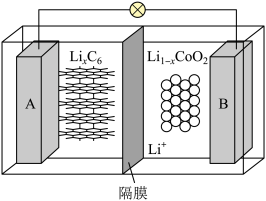
(5)特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。隔膜只允许特定的离子通过,电池反应式为:LixC6+Li1-xCoO2 C6+LiCoO2,则放电时负极的电极反应式为
C6+LiCoO2,则放电时负极的电极反应式为_______ ,充电时,电极B应与直流电源的_______ 极(填“正”或“负”)连接,此时该电极的电极反应式为_______ 。

(1)电源的a极为
(2)铂夹C上发生反应的电极反应式为
(3)装置通直流电时,下列判断不正确的是
①电极A上发生氧化反应 ②电子沿a→C→D→b 路径流动
③片刻后D点附近c(
 )增大 ④片刻后可观察到滤纸C点变红色
)增大 ④片刻后可观察到滤纸C点变红色(4)现切断K2、K3,闭合K1,观察到电流表指针偏转。电极A上的电极反应式为
(5)特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。隔膜只允许特定的离子通过,电池反应式为:LixC6+Li1-xCoO2
 C6+LiCoO2,则放电时负极的电极反应式为
C6+LiCoO2,则放电时负极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】乙酸乙酯在工业上有着广泛的用途。科学家以乙烯、乙酸为原料,杂多酸作催化剂制备乙酸乙酯,反应原理为CH2=CH2(g)+CH3COOH(g) CH3COOC2H5(l)
CH3COOC2H5(l)
(1)回答下列问题:
I.2C(s)+2H2(g) CH2=CH2(g) △H1=+52.3
CH2=CH2(g) △H1=+52.3
Ⅱ.2C(s)+2H2(g)+O2(g) CH3COOH(g) △H2=-436.4
CH3COOH(g) △H2=-436.4
Ⅲ.4C(s)+4H2(g)+O2(g CH3COOC2H5(l) △H3=-463.2
CH3COOC2H5(l) △H3=-463.2
以乙烯(g)、乙酸(g)为原料制备乙酸乙酯(l)的反应的热化学方程式为_____ 。
(2)一定条件下,在一个密闭容器中,通入各1mol的乙烯和乙酸气体,发生上述反应。
①若保持温度和压强不变,下列描述能说明反应已达化学平衡的是_____ (填字母)。
A.单位时间内,消耗乙烯和生成乙酸的物质的量相同
B.容器内混合气体的密度不再变化
C. 不再变化
不再变化
D.体系中乙烯和乙酸的转化率相等
②分别在压强P1、P2下,相同时间内测得乙酸乙酯的产率随温度的变化如图。

P1_____ P2(填“>”或“<”),理由是_____ 。A点后乙酸乙酯产率随温度升高反而下降的原因可能是_____ 。A点该反应的压强平衡常数Kp=_____ (用含P1的代数式表示)。
(3)科学家设想通过电化学方法实现乙烯的转化,其原理如图所示(均为惰性电极)。图中b极为_____ 极,M极上的电极反应式为_____ 。

 CH3COOC2H5(l)
CH3COOC2H5(l)(1)回答下列问题:
I.2C(s)+2H2(g)
 CH2=CH2(g) △H1=+52.3
CH2=CH2(g) △H1=+52.3
Ⅱ.2C(s)+2H2(g)+O2(g)
 CH3COOH(g) △H2=-436.4
CH3COOH(g) △H2=-436.4
Ⅲ.4C(s)+4H2(g)+O2(g
 CH3COOC2H5(l) △H3=-463.2
CH3COOC2H5(l) △H3=-463.2
以乙烯(g)、乙酸(g)为原料制备乙酸乙酯(l)的反应的热化学方程式为
(2)一定条件下,在一个密闭容器中,通入各1mol的乙烯和乙酸气体,发生上述反应。
①若保持温度和压强不变,下列描述能说明反应已达化学平衡的是
A.单位时间内,消耗乙烯和生成乙酸的物质的量相同
B.容器内混合气体的密度不再变化
C.
 不再变化
不再变化D.体系中乙烯和乙酸的转化率相等
②分别在压强P1、P2下,相同时间内测得乙酸乙酯的产率随温度的变化如图。

P1
(3)科学家设想通过电化学方法实现乙烯的转化,其原理如图所示(均为惰性电极)。图中b极为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
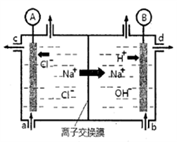
【推荐3】⑴氯碱工业是以惰性电极电解饱和食盐水,制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
完成下列填空:
①离子交换膜的作用为:____________________ 。
②写出电解饱和食盐水的离子方程式_________ 。
③氢氧化钠溶液从图中_____ 位置流出。(选填a、b、c或d)
⑵电化学在日常生活中用途广泛,图①是镁次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O===Cl-+Mg(OH)2↓,图②是Cr2O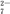 的工业废水的处理,下列说法正确的是
的工业废水的处理,下列说法正确的是( )

A.图②中Cr2O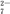 离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
B.图②的电解池中,有0.084 g阳极材料参与反应,阴极会有33.6 mL的气体产生
C.图①中发生的还原反应是:Mg2++ClO-+H2O+2e-===Cl-+Mg(OH)2
D.若图①中3.6 g镁溶解产生的电量用以图②废水处理,理论可产生10.7 g氢氧化铁沉淀
⑶观察下列装置,回答下列问题:

①装置B中PbO2上发生的电极反应方程式为_____________________________________ 。
②装置A中总反应的离子方程式为_____________________________________________ 。
③当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为________ L(标准状况下,不考虑气体的溶解)。

完成下列填空:
①离子交换膜的作用为:
②写出电解饱和食盐水的离子方程式
③氢氧化钠溶液从图中
⑵电化学在日常生活中用途广泛,图①是镁次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O===Cl-+Mg(OH)2↓,图②是Cr2O
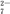 的工业废水的处理,下列说法正确的是
的工业废水的处理,下列说法正确的是
A.图②中Cr2O
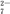 离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去B.图②的电解池中,有0.084 g阳极材料参与反应,阴极会有33.6 mL的气体产生
C.图①中发生的还原反应是:Mg2++ClO-+H2O+2e-===Cl-+Mg(OH)2
D.若图①中3.6 g镁溶解产生的电量用以图②废水处理,理论可产生10.7 g氢氧化铁沉淀
⑶观察下列装置,回答下列问题:

①装置B中PbO2上发生的电极反应方程式为
②装置A中总反应的离子方程式为
③当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为
您最近一年使用:0次



