随着科学技术的不断发展,可以通过淡化海水获取淡水、从海水中提取食盐、镁等重要的化学物质。
(1)某海水样品测得其pH值约为8.0~8.5(常温下),以下物质中,可能使海水呈碱性的有_____(填字母)。
(2)在浓氨水中通入过量 后,加入
后,加入 颗粒可制得碳酸氢钠,写出另一产物的电子式
颗粒可制得碳酸氢钠,写出另一产物的电子式_____ 。
(3)常温下,将盐酸和氨水混合,所得溶液 ,此时溶液中
,此时溶液中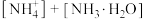
_____ 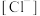 (填字母)。
(填字母)。
A.> B.< C.=
(4)碳酸钠和碳酸氢钠是两种非常重要的化工产品,下列关于两种物质的水溶液的说法错误的是_____(填字母)。
(5)海水淡化的方法主要有两种原理,除了可以利用反渗透膜的分离作用淡化海水,还可以利用_____(填字母)原理,进行海水淡化。
(1)某海水样品测得其pH值约为8.0~8.5(常温下),以下物质中,可能使海水呈碱性的有_____(填字母)。
A. | B. | C. | D. |
 后,加入
后,加入 颗粒可制得碳酸氢钠,写出另一产物的电子式
颗粒可制得碳酸氢钠,写出另一产物的电子式(3)常温下,将盐酸和氨水混合,所得溶液
 ,此时溶液中
,此时溶液中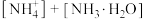
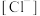 (填字母)。
(填字母)。A.> B.< C.=
(4)碳酸钠和碳酸氢钠是两种非常重要的化工产品,下列关于两种物质的水溶液的说法错误的是_____(填字母)。
| A.两种溶液之间不能相互转化 |
| B.均存在水解平衡 |
| C.均呈碱性,且加热后碱性都增强 |
D.均存在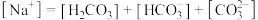 |
| A.过滤 | B.蒸馏 | C.渗析 | D.萃取。 |
更新时间:2023-09-19 06:54:39
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】 的电子式为
的电子式为___________ 。 可用空气和
可用空气和 为原料直接制备。在与熔融金属
为原料直接制备。在与熔融金属 反应前,空气需依次通过
反应前,空气需依次通过___________ 、___________ 。
A.浓硫酸 B.饱和食盐水 C. 溶液 D.
溶液 D. 溶液
溶液
 的电子式为
的电子式为 可用空气和
可用空气和 为原料直接制备。在与熔融金属
为原料直接制备。在与熔融金属 反应前,空气需依次通过
反应前,空气需依次通过A.浓硫酸 B.饱和食盐水 C.
 溶液 D.
溶液 D. 溶液
溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】工业上常用电解 溶液制备
溶液制备 ,反应方程式如下:
,反应方程式如下: 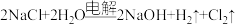
回答下列问题:
(1)用电子式表示 的形成过程:
的形成过程:_______ ;
(2) 属于
属于_______ 化合物(填“离子”或“共价”),用电子式表示 的形成过程
的形成过程_______ ;
(3) 中含有的化学键类型是
中含有的化学键类型是_______ ,其电子式为_______ ;
(4)用含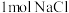 的溶液进行电解制备
的溶液进行电解制备 。
。
①该 溶液中
溶液中 的物质的量是
的物质的量是_______ 
②标准状况下,理论上最多能产生
_______ L;
③当 完全被电解消耗完时,产生的
完全被电解消耗完时,产生的 的质量为
的质量为_______ g;
④两种气体产物相同条件下的密度比是_______ 。
 溶液制备
溶液制备 ,反应方程式如下:
,反应方程式如下: 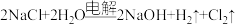
回答下列问题:
(1)用电子式表示
 的形成过程:
的形成过程:(2)
 属于
属于 的形成过程
的形成过程(3)
 中含有的化学键类型是
中含有的化学键类型是(4)用含
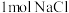 的溶液进行电解制备
的溶液进行电解制备 。
。①该
 溶液中
溶液中 的物质的量是
的物质的量是
②标准状况下,理论上最多能产生

③当
 完全被电解消耗完时,产生的
完全被电解消耗完时,产生的 的质量为
的质量为④两种气体产物相同条件下的密度比是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】写出下列物质发生水解反应的离子方程式,并指出水溶液的酸碱性。
(1) :
:_______ 、______ 。
(2) :
:_______ 、_______ 。
(3) :
:_______ 、______ 。
(1)
 :
:(2)
 :
:(3)
 :
:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,请回答下列问题:
常温下,某Na2CO3溶液中滴入酚酞,溶液呈_____ 色,则该溶液呈 ______ 性,原因是 ______ (用离子方程式表示),若在该溶液中再滴入过量的氯化钡溶液,所观察到的现象是_________ ,
(2)已知在H2S溶液中存在下列平衡:H2S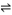 HS- + H+
HS- + H+
①向H2S溶液中加入NaOH固体时(不考虑温度变化),电离平衡向______ 移动(填“左”或“右”)
______ (填“增大”、“减小”或“不变”)。
②向H2S溶液中加入NaHS固体时,电离平衡向______ 移动(填“左”或“右”),pH ______ (填“增大”、“减小”或“不变”)。
常温下,某Na2CO3溶液中滴入酚酞,溶液呈
(2)已知在H2S溶液中存在下列平衡:H2S
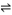 HS- + H+
HS- + H+①向H2S溶液中加入NaOH固体时(不考虑温度变化),电离平衡向

②向H2S溶液中加入NaHS固体时,电离平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1)室温下pH相等的① ②
② 和③NaOH溶液,物质的量浓度从大到小的顺序为
和③NaOH溶液,物质的量浓度从大到小的顺序为___________ (填序号);
(2)室温下浓度均为0.1 的①
的① ②
② 和③
和③ 溶液中,
溶液中, 物质的量浓度从大到小的顺序为:
物质的量浓度从大到小的顺序为:___________ (填序号);
(3)室温下0.1 的NaX、NaY,NaZ溶液pH依次增大,可知HX、HY、HZ的酸性从强到弱的顺序为
的NaX、NaY,NaZ溶液pH依次增大,可知HX、HY、HZ的酸性从强到弱的顺序为___________ ;
(4)室温下,已知 的
的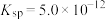 ,向0.05
,向0.05  的
的 溶液中滴加浓NaOH溶液,刚好出现沉淀时,溶液的pH约为
溶液中滴加浓NaOH溶液,刚好出现沉淀时,溶液的pH约为___________ ;
(5)常温下, 和
和 的电离平衡常数如下:
的电离平衡常数如下:
①根据以上信息可知, 溶液呈
溶液呈___________ (填“酸”、“碱”或“中”)性,
②少量 溶液与过量
溶液与过量 溶液反应的离子方程式为
溶液反应的离子方程式为______ ;
③室温下,pH=1的 溶液中,
溶液中,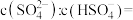
______ 。
(1)室温下pH相等的①
 ②
② 和③NaOH溶液,物质的量浓度从大到小的顺序为
和③NaOH溶液,物质的量浓度从大到小的顺序为(2)室温下浓度均为0.1
 的①
的① ②
② 和③
和③ 溶液中,
溶液中, 物质的量浓度从大到小的顺序为:
物质的量浓度从大到小的顺序为:(3)室温下0.1
 的NaX、NaY,NaZ溶液pH依次增大,可知HX、HY、HZ的酸性从强到弱的顺序为
的NaX、NaY,NaZ溶液pH依次增大,可知HX、HY、HZ的酸性从强到弱的顺序为(4)室温下,已知
 的
的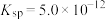 ,向0.05
,向0.05  的
的 溶液中滴加浓NaOH溶液,刚好出现沉淀时,溶液的pH约为
溶液中滴加浓NaOH溶液,刚好出现沉淀时,溶液的pH约为(5)常温下,
 和
和 的电离平衡常数如下:
的电离平衡常数如下:| 化学式 |  |  |
| 电离平衡常数 | 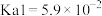 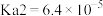 |  |
 溶液呈
溶液呈②少量
 溶液与过量
溶液与过量 溶液反应的离子方程式为
溶液反应的离子方程式为③室温下,pH=1的
 溶液中,
溶液中,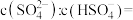
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】25℃时,取浓度均为0.1mol/L的醋酸溶液和氨水溶液各20mL,分别用0.1mol/LNaOH溶液、0.1mol/L盐酸进行中和滴定。滴定过程中pH随滴加溶液的体积变化关系如图所示。回答下列问题:
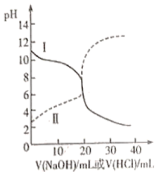
(1)表示氨水滴定过程中pH变化情况的是曲线___________ (填“Ⅰ”或“Ⅱ”)。由图中信息可知,25℃时0.1mol/L醋酸溶液的电离程度___________ (填“大于”“小于”或“等于”,下同)10%。当横坐标为20mL时,曲线Ⅰ对应的纵坐标应___________ 7。
(2)滴加溶液到10mL时,曲线Ⅱ所表示的溶液中c(H+)-c(OH-)___________ (结果中不能包含阳离子浓度)。

(1)表示氨水滴定过程中pH变化情况的是曲线
(2)滴加溶液到10mL时,曲线Ⅱ所表示的溶液中c(H+)-c(OH-)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下,将某一元酸HX和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,若a___ 7(填“>”“<”或“=”),则HX为强酸;若a ____ 7(填“>”“<”或“=”),则HX为弱酸。
(2)在乙组混合溶液中离子浓度c(X-)与c(Na+)的大小关系是____ 。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HX是___ 酸(填“强”或“弱”)。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=__ mol/L。
实验 编号 | HX物质的量 浓度(mol/L) | NaOH物质的 量浓度(mol/L) | 混合溶液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c1 | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | c2 | c2 | pH=10 |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,若a
(2)在乙组混合溶液中离子浓度c(X-)与c(Na+)的大小关系是
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HX是
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)氯化铁水溶液呈酸性,原因是(用离子方程式表示)___________ 。实验室在临时配制一些氯化铁溶液时,常将氯化铁固体先溶于较浓的___________ 中,然后再用蒸馏水稀释到所需要的浓度,是为了抑制其水解。
(2)25℃时,浓度为0.1 mol/L的6种溶液:①HCl;②CH3COOH ;③Ba(OH)2 ;④ Na2CO3 ;⑤ KCl ;⑥NH4Cl,溶液的pH由小到大的顺序为___________ (填序号)[已知Kb(NH3·H2O)=1.8×10-5,Ka(CH3COOH)=1.75×10-5]。
(3)写出1mol/L的NaH2PO4溶液中的电荷守恒表达式:___________
(4)泡沫灭火器(里面装饱和NaHCO3溶液和Al2(SO4)3)的工作原理(用离子方程式表示)___________
(5)不断加热FeCl3溶液蒸干其水分并灼烧,得到的固体是___________ 。
(1)氯化铁水溶液呈酸性,原因是(用离子方程式表示)
(2)25℃时,浓度为0.1 mol/L的6种溶液:①HCl;②CH3COOH ;③Ba(OH)2 ;④ Na2CO3 ;⑤ KCl ;⑥NH4Cl,溶液的pH由小到大的顺序为
(3)写出1mol/L的NaH2PO4溶液中的电荷守恒表达式:
(4)泡沫灭火器(里面装饱和NaHCO3溶液和Al2(SO4)3)的工作原理(用离子方程式表示)
(5)不断加热FeCl3溶液蒸干其水分并灼烧,得到的固体是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】化学与生活息息相关,请回答下列问题:
(1)人体摄入___________ 元素不足或过量都会引起甲状腺疾病。
(2)水的净化方法中,净化程度最高的是___________ 。
(3)用汽油可洗去衣服上的油污,利用了汽油对油污的___________ 作用。
(4)生产不锈钢炊具所使用的材料属于___________ (选填“合金”或“合成材料”)。
(5)熟石灰、小苏打、烧碱三种物质中,可用于防止树木冻伤、并防止害虫生卵的是___________ 。
(6)家庭厨房用的纯碱的化学式是___________ 。
(7)厨房燃气灶中天然气燃烧的化学方程式是___________ 。
(8)在野外被蚊虫叮咬,可以涂抹___________ ,以减轻痛痒。
(9)长久放置的盛放生石灰的塑料瓶胀裂,原因是___________ 。
(10)古老的西方炼金术是要“把贱金属转化成纯金”,他们不能达到目的的原因是违背了___________ 。
(1)人体摄入
(2)水的净化方法中,净化程度最高的是
(3)用汽油可洗去衣服上的油污,利用了汽油对油污的
(4)生产不锈钢炊具所使用的材料属于
(5)熟石灰、小苏打、烧碱三种物质中,可用于防止树木冻伤、并防止害虫生卵的是
(6)家庭厨房用的纯碱的化学式是
(7)厨房燃气灶中天然气燃烧的化学方程式是
(8)在野外被蚊虫叮咬,可以涂抹
(9)长久放置的盛放生石灰的塑料瓶胀裂,原因是
(10)古老的西方炼金术是要“把贱金属转化成纯金”,他们不能达到目的的原因是违背了
您最近一年使用:0次



