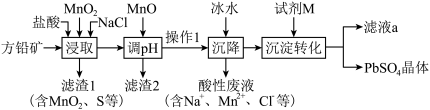
硫酸铅广泛应用于制造铅蓄电池、白色颜料以及精细化工产品等。工业生产中利用方铅矿(主要成分为PbS,含有FeS2等杂质)制备PbSO4晶体,工艺流程如下:
已知:①PbCl2难溶于冷水,易溶于热水;②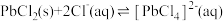 △H>0;
△H>0;
③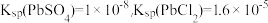 。
。
(1)Pb元素位于周期表的___________ (填“p”“d”或“ds”)区。
(2)“浸取”时,由PbS转化为[PbC14]2-的离子方程式为___________ 。
(3)“滤渣2”的主要成分是___________ 。
(4)“沉降”时加入冰水的作用是___________ 。
(5)滤液a可循环利用,试剂M是___________ 。(填化学式)
(6)“沉淀转化”过程发生反应为
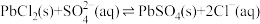 ,则该反应达平衡时,溶液中
,则该反应达平衡时,溶液中
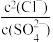 =
=___________ 。
(7)铅蓄电池中的正极材料是___________ (填“Pb”或“PbO2”);充电时,与电源负极相连的电极反应式为___________ 。

已知:①PbCl2难溶于冷水,易溶于热水;②
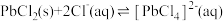 △H>0;
△H>0;③
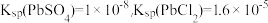 。
。(1)Pb元素位于周期表的
(2)“浸取”时,由PbS转化为[PbC14]2-的离子方程式为
(3)“滤渣2”的主要成分是
(4)“沉降”时加入冰水的作用是
(5)滤液a可循环利用,试剂M是
(6)“沉淀转化”过程发生反应为
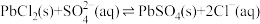 ,则该反应达平衡时,溶液中
,则该反应达平衡时,溶液中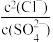 =
=(7)铅蓄电池中的正极材料是
更新时间:2023-10-31 00:33:27
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】(1)刘安《淮南万毕术》中“曾青得铁则化为铜”是古代湿法炼铜的真实写照。除去CuSO4溶液中少量的Fe2+,可以按照下面的流程进行:
已知:Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如下表:
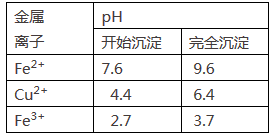
①下列物质中适合作为试剂X的是____________
②加入的Y及调节的pH范围是_____________
(2)已知常温下,Ksp[Cu(OH)2]=2×10-20,通过上述流程得到的CuSO4溶液中,c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于_________ 。
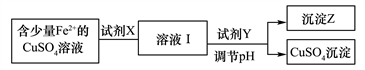
已知:Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如下表:

①下列物质中适合作为试剂X的是
A.H2O2 B.KMnO4
C.HNO3 D.Cl2
②加入的Y及调节的pH范围是
A.Cu(OH)2 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH3·H2O 3.7~4.0
(2)已知常温下,Ksp[Cu(OH)2]=2×10-20,通过上述流程得到的CuSO4溶液中,c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】以含钴废料(主要成分为Co2O3,含有少量MnO2、NiO、Fe3O4)为原料制备Co2O3的流程如图所示:
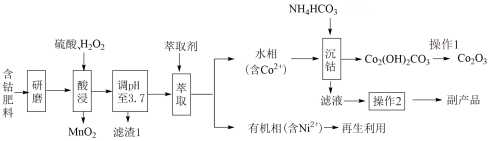
(1)为了提高“酸浸”步骤的浸出率,可采取的措施有_______ (任答一点)。“滤渣1”的化学式为_______ 。
(2)“酸浸”时Co2O3与H2O2反应的化学方程式为_______ 。
(3)“操作2”所得副产品的一种用途为_______ 。 已知该物质的溶液加热到100°C时会分解,该物质的溶解度见表:
操作2是_______ (填字母)。
A.蒸发结晶 B.降温结晶 C.减压蒸发结晶
(4)“沉钴”时温度不能太低也不能太高,原因是_______ 。
(5)“沉钴”步骤中发生反应的离子方程式为_______ 。
(6)已知常温下Ksp(CoC2O4)=6.4×10-8、Ksp(CoCO3)=1.6×10-13,向浓度相同的Na2CO3和Na2C2O4的混合溶液中加入足量CoSO4固体,则所得溶液中c( ):c(
):c( )=
)=_______ 。
(7)有机相提取的Ni2+再生时可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH。则放电时负极的电极反应式为_______ 。

(1)为了提高“酸浸”步骤的浸出率,可采取的措施有
(2)“酸浸”时Co2O3与H2O2反应的化学方程式为
(3)“操作2”所得副产品的一种用途为
| 温度/°C | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 88.0 |
A.蒸发结晶 B.降温结晶 C.减压蒸发结晶
(4)“沉钴”时温度不能太低也不能太高,原因是
(5)“沉钴”步骤中发生反应的离子方程式为
(6)已知常温下Ksp(CoC2O4)=6.4×10-8、Ksp(CoCO3)=1.6×10-13,向浓度相同的Na2CO3和Na2C2O4的混合溶液中加入足量CoSO4固体,则所得溶液中c(
 ):c(
):c( )=
)=(7)有机相提取的Ni2+再生时可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH。则放电时负极的电极反应式为
您最近一年使用:0次
【推荐3】钒和铬都是重要的战略金属,利用钒、铬废渣(主要成分为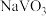 和
和 ,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。
,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。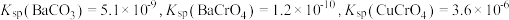 。
。
回答下列问题:
(1)基态铬原子价电子轨道表示式为_______ 。
(2)钒、铬废渣“水浸”前,先要进行粉碎处理,为提高浸取效率,还可采取的措施有_______ (任写一点)。
(3)“沉钒”的含钒产物为钒酸钙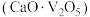 ,该过程中发生反应的化学方程式是
,该过程中发生反应的化学方程式是_______ 。
(4)“沉铬”时,铬转化为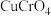 沉淀,“转化”过程中发生反应的离子方程式为
沉淀,“转化”过程中发生反应的离子方程式为_______ 。
(5)向“沉钒后液”中加入足量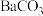 ,可将其中的铬转化为
,可将其中的铬转化为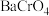 沉淀,铬的理论转化率为
沉淀,铬的理论转化率为_______ (保留三位有效数字) 。
。
(6)复合材料氧铬酸钙的立方晶胞如下图所示。_______ 。
②已知该晶体的密度为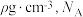 为阿伏加德罗常数的值,则相邻
为阿伏加德罗常数的值,则相邻 与
与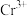 之间的最短距离为
之间的最短距离为_______ 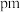 (列出计算式即可)。
(列出计算式即可)。
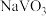 和
和 ,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。
,还含有其他难溶物)分离回收钒、铬的工艺流程如下图所示。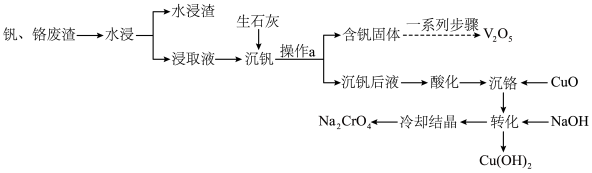
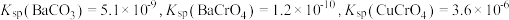 。
。回答下列问题:
(1)基态铬原子价电子轨道表示式为
(2)钒、铬废渣“水浸”前,先要进行粉碎处理,为提高浸取效率,还可采取的措施有
(3)“沉钒”的含钒产物为钒酸钙
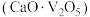 ,该过程中发生反应的化学方程式是
,该过程中发生反应的化学方程式是(4)“沉铬”时,铬转化为
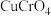 沉淀,“转化”过程中发生反应的离子方程式为
沉淀,“转化”过程中发生反应的离子方程式为(5)向“沉钒后液”中加入足量
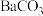 ,可将其中的铬转化为
,可将其中的铬转化为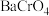 沉淀,铬的理论转化率为
沉淀,铬的理论转化率为 。
。(6)复合材料氧铬酸钙的立方晶胞如下图所示。
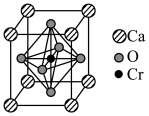
②已知该晶体的密度为
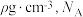 为阿伏加德罗常数的值,则相邻
为阿伏加德罗常数的值,则相邻 与
与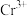 之间的最短距离为
之间的最短距离为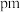 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】本次亚运会火炬燃料甲醇是利用焦炉气中的氢气(H2)与从工业尾气中捕集的二氧化碳(CO2)合成,并由远程甲醇动力重卡提供运输保障。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:
Ⅰ.
Ⅱ.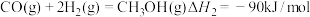
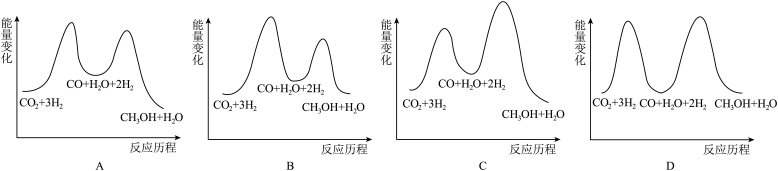
若反应Ⅰ为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
(2)甲醇可作为燃料使用,下图是一个电化学过程的装置示意图。
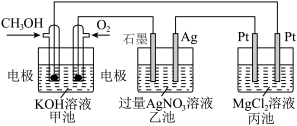
①甲池中通入 的电极电极反应方程式为
的电极电极反应方程式为___________ 。
②丙池中总反应的离子方程式为___________ 。
③当乙池中Ag极的质量增加1.08g时,甲池中理论上消耗
___________  (标准状况)。
(标准状况)。
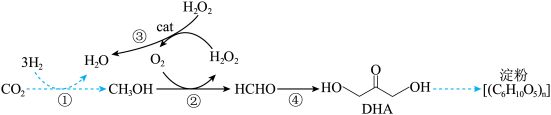
(3)回收并利用 一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化
一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设
合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设 为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
(4)利用两种金属催化剂,在水溶液体系中将 分别转化为
分别转化为 和
和 的反应过程示意图如图所示。
的反应过程示意图如图所示。
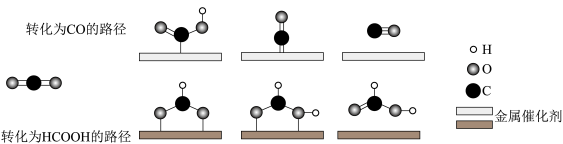
下列说法错误的是___________(填标号)。
(1)二氧化碳加氢制甲醇的总反应可表示为:
 ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:Ⅰ.

Ⅱ.
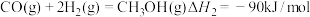
若反应Ⅰ为慢反应,下列示意图中能体现上述反应能量变化的是

(2)甲醇可作为燃料使用,下图是一个电化学过程的装置示意图。

①甲池中通入
 的电极电极反应方程式为
的电极电极反应方程式为②丙池中总反应的离子方程式为
③当乙池中Ag极的质量增加1.08g时,甲池中理论上消耗

 (标准状况)。
(标准状况)。(3)回收并利用
 一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化
一直是科研人员研究的热点。中科院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设
合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设 为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
为阿伏加德罗常数的值。下列说法正确的是___________(填标号)。
A.反应①中消耗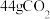 ,转移电子数为 ,转移电子数为 |
| B.淀粉与纤维素的分子式相同,互为同分异构体 |
C. 与 与 的混合物中所含氧原子数为 的混合物中所含氧原子数为 |
D.反应③中cat为催化剂,实验室常用 催化该反应 催化该反应 |
(4)利用两种金属催化剂,在水溶液体系中将
 分别转化为
分别转化为 和
和 的反应过程示意图如图所示。
的反应过程示意图如图所示。
下列说法错误的是___________(填标号)。
A.在转化为 的路径中,只涉及碳氧键的断裂和氧氢键的形成 的路径中,只涉及碳氧键的断裂和氧氢键的形成 |
B.在转化为 的路径中, 的路径中, 被氧化为 被氧化为 |
| C.两个转化路径均无非极性键的形成 |
| D.上述反应过程说明催化剂具有选择性 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)2004年美国圣路易斯大学研制了一种新型乙醇电池,该电池采用磺酸类质子溶剂,在200℃左右时供电,电池示意图如下所示:
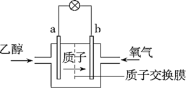
①___ 极(填“a”或“b”)为电池的正极,电池工作时电子的流向为____ (填“a→b”或“b→a”)。
②写出该电池负极的电极反应式:_______________ 。
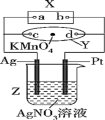
(2)图中X为电源,Y为浸透滴有酚酞试液的饱和食盐水的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。
①Y中总反应的化学方程式为________ ,滤纸上c点附近会变_____ 色。
②电解一段时间后,Z产生280 mL的气体(标准状况下),此时Z中溶液的体积为500 mL,假设溶液中还有AgNO3存在,则溶液中氢离子的物质的量是______ ,需加入____ g的____ (填化学式)可使溶液复原。
(3)氧化还原反应与生产、生活、科技密切相关。请回答下列问题:
①银制器皿久置表面变黑是因为表面生成了Ag2S,该现象属于____ 腐蚀。
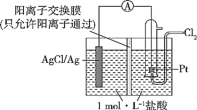
②在如图所示的原电池装置中,负极的电极反应为_________ ,电池总反应为__________ ,当电路中通过0.1 mol e-时,交换膜左侧溶液中离子减少的物质的量为____ 。

①
②写出该电池负极的电极反应式:

(2)图中X为电源,Y为浸透滴有酚酞试液的饱和食盐水的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。
①Y中总反应的化学方程式为
②电解一段时间后,Z产生280 mL的气体(标准状况下),此时Z中溶液的体积为500 mL,假设溶液中还有AgNO3存在,则溶液中氢离子的物质的量是
(3)氧化还原反应与生产、生活、科技密切相关。请回答下列问题:
①银制器皿久置表面变黑是因为表面生成了Ag2S,该现象属于
②在如图所示的原电池装置中,负极的电极反应为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.H2S是石油化工行业广泛存在的污染性气体,但同时也是重要的氢源和硫源,工业上可以采取多种方式处理。
干法脱硫:
(1)已知H2S的燃烧热为a kJ·mol-1,S的燃烧热为b kJ·mol-1,则常温下空气直接氧化脱除H2S的反应:2H2S(g)+O2(g) = 2S(s)+2H2O(l) ∆H=_______ kJ·mol-1。
(2)常用脱硫剂的脱硫效果及反应条件如表,最佳脱硫剂为_______ 。
间接电解法脱硫:
间接电解法是通过FeCl3溶液吸收并氧化H2S气体,将反应后溶液通过电解再生,实现循环使用,该法处理过程如图。
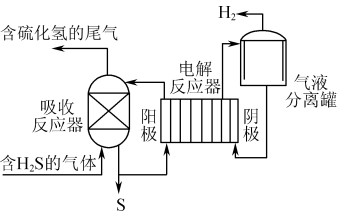
(3)吸收反应器中的离子方程式为_______ 。
(4)电解反应器中阳极的电极反应式为_______ 。
Ⅱ.图为双阴极微生物燃料电池,可同步实现除污脱氮和产生电能。

(5)理论上,厌氧室消耗15gC6H12O6,外电路转移e-数目为_______ 。
(6)缺氧室中得电极反应式为_______ 。
干法脱硫:
(1)已知H2S的燃烧热为a kJ·mol-1,S的燃烧热为b kJ·mol-1,则常温下空气直接氧化脱除H2S的反应:2H2S(g)+O2(g) = 2S(s)+2H2O(l) ∆H=
(2)常用脱硫剂的脱硫效果及反应条件如表,最佳脱硫剂为
| 脱硫剂 | 出口硫(mg·m-3) | 脱硫温度(℃) | 操作压力(MPa) | 再生条件 |
| 一氧化碳 | <1.33 | 300~400 | 0~3.0 | 蒸汽再生 |
| 活性炭 | <1.33 | 常温 | 0~3.0 | 蒸汽再生 |
| 氧化锌 | <1.33 | 350~400 | 0~5.0 | 不再生 |
| 锰矿 | <3.99 | 400 | 0~2.0 | 不再生 |
间接电解法脱硫:
间接电解法是通过FeCl3溶液吸收并氧化H2S气体,将反应后溶液通过电解再生,实现循环使用,该法处理过程如图。

(3)吸收反应器中的离子方程式为
(4)电解反应器中阳极的电极反应式为
Ⅱ.图为双阴极微生物燃料电池,可同步实现除污脱氮和产生电能。

(5)理论上,厌氧室消耗15gC6H12O6,外电路转移e-数目为
(6)缺氧室中得电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】一种从分银渣(含CuO、 、
、 、
、 、
、 、Ag、
、Ag、 等)回收金属资源的工艺流程如下:
等)回收金属资源的工艺流程如下:
Ⅰ.CuCl难溶于水,但溶于浓盐酸。
Ⅱ.“富锑铋铜液”中含 (铋离子)、
(铋离子)、 (锑离子)、
(锑离子)、 、
、 。
。
Ⅲ.该工艺条件下,有关金属离子沉淀时的相关pH见下表:
回答下列问题:
(1)写出分银渣中的Ag与盐酸、溶解氧反应的离子方程式:___________________ 。
(2)“酸浸”时,盐酸浓度对锑、铋、铜浸出率的影响如图1所示,温度对锑、铋、铜浸出率的影响如图2所示。______ ;浸出时温度以80℃为宜,其原因是_____________________ 。
(3)①已知“滤渣2”的主要成分是 ,则“一次水解”时主要发生反应的化学方程式为
,则“一次水解”时主要发生反应的化学方程式为________ 。
②已知“滤渣3”的主要成分是BiOCl和 ,则“二次水解”时调节pH的范围应该是
,则“二次水解”时调节pH的范围应该是______ 。
(4)“滤渣1”中的AgCl可用硫酸-硫脲(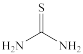 )浸出,生成配合物
)浸出,生成配合物 ,写出该反应的化学方程式:
,写出该反应的化学方程式:________________ ;该配合物中不存在__________ (填标号)。
A.离子键 B.极性共价键 C.配位键 D.范德华力 E.非极性共价键
(5)写出一种从“富铜溶液”中回收金属资源的方法:_________________ 。
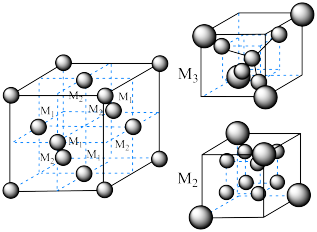
(6)尖晶石属于立方晶系,其晶胞可视为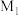 、
、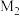 两种结构交替无隙并置而成(如图所示),其中
两种结构交替无隙并置而成(如图所示),其中 可以为
可以为 、
、 、
、 、
、 等,
等, 可以为
可以为 、
、 、
、 等。已知尖晶石型
等。已知尖晶石型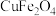 的晶胞参数为842pm,则该晶体的密度为
的晶胞参数为842pm,则该晶体的密度为________  。(列出计算式,阿伏加德罗常数的值为
。(列出计算式,阿伏加德罗常数的值为 )
)
 、
、 、
、 、
、 、Ag、
、Ag、 等)回收金属资源的工艺流程如下:
等)回收金属资源的工艺流程如下: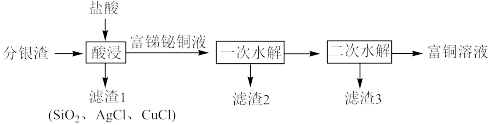
Ⅰ.CuCl难溶于水,但溶于浓盐酸。
Ⅱ.“富锑铋铜液”中含
 (铋离子)、
(铋离子)、 (锑离子)、
(锑离子)、 、
、 。
。Ⅲ.该工艺条件下,有关金属离子沉淀时的相关pH见下表:
金属离子 |
|
|
|
|
开始沉淀时( | 0.5 | 1.5 | 4.7 | 1.5 |
完全沉淀时( | 1.4 | 2.5 | 6.7 | 3.2 |
(1)写出分银渣中的Ag与盐酸、溶解氧反应的离子方程式:
(2)“酸浸”时,盐酸浓度对锑、铋、铜浸出率的影响如图1所示,温度对锑、铋、铜浸出率的影响如图2所示。
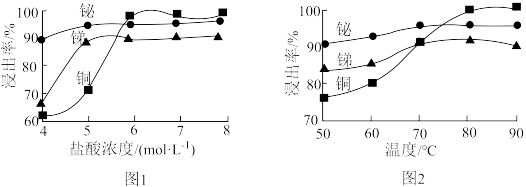
(3)①已知“滤渣2”的主要成分是
 ,则“一次水解”时主要发生反应的化学方程式为
,则“一次水解”时主要发生反应的化学方程式为②已知“滤渣3”的主要成分是BiOCl和
 ,则“二次水解”时调节pH的范围应该是
,则“二次水解”时调节pH的范围应该是(4)“滤渣1”中的AgCl可用硫酸-硫脲(
 )浸出,生成配合物
)浸出,生成配合物 ,写出该反应的化学方程式:
,写出该反应的化学方程式:A.离子键 B.极性共价键 C.配位键 D.范德华力 E.非极性共价键
(5)写出一种从“富铜溶液”中回收金属资源的方法:
(6)尖晶石属于立方晶系,其晶胞可视为
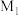 、
、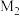 两种结构交替无隙并置而成(如图所示),其中
两种结构交替无隙并置而成(如图所示),其中 可以为
可以为 、
、 、
、 、
、 等,
等, 可以为
可以为 、
、 、
、 等。已知尖晶石型
等。已知尖晶石型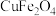 的晶胞参数为842pm,则该晶体的密度为
的晶胞参数为842pm,则该晶体的密度为 。(列出计算式,阿伏加德罗常数的值为
。(列出计算式,阿伏加德罗常数的值为 )
)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】三氯化钌(RuCl3 )和硫化铋(Bi2S3)用途广泛。利用某含钌、铋的废催化剂(主要成分为Ru、Bi2O3、SiO2)回收RuCl3和Bi2S3的工艺流程如下:

已知:
I.滤液1中溶质的主要成分为Na2 RuO4、NaBiO2、NaCl和Na2SiO3;
Ⅱ.RuO4的沸点为40℃,易挥发,微溶于水,极易溶于CCl4,RuO4有强氧化性,超过100℃时,RuO4就爆炸分解,室温下与乙醇接触也易爆炸;
Ⅲ.Ksp(Bi2S3)=1.0×10-20。
回答下列问题:
(1)“氧化碱浸”时,为提高反应速率,可采取的措施有_______ (写出两条)。
(2)向滤液1中加入乙醇生成Ru(OH)4沉淀和乙醛,则“转化”过程中乙醇作_______ (填“氧化剂”或“还原剂”)。
(3)①Ru(OH)4与NaClO发生反应的化学方程式为_______ ;反应过程中NaClO的利用率与温度的关系如图所示,温度高于25℃时NaClO的利用率开始下降,主要原因可能是_______ 。
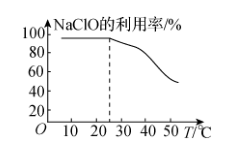
②“蒸馏”过程中常采用的加热方式为_______ 。
(4)盐酸“吸收”RuO4过程中产生的Cl2经进一步处理可以转化为_______ 、 _______ (填两种物质的名称),在本工艺流程中循环利用。
(5)滤渣3的主要成分为_______ (填化学式)。
(6)“沉淀”时,向1L 1.0 mol· L-1BiCl3溶液中加入0.2L Na2S溶液,反应后混合溶液中c(S2-)为1×10-6mol·L-1,则Bi3+的沉淀率为_______ (忽略溶液体积变化)。

已知:
I.滤液1中溶质的主要成分为Na2 RuO4、NaBiO2、NaCl和Na2SiO3;
Ⅱ.RuO4的沸点为40℃,易挥发,微溶于水,极易溶于CCl4,RuO4有强氧化性,超过100℃时,RuO4就爆炸分解,室温下与乙醇接触也易爆炸;
Ⅲ.Ksp(Bi2S3)=1.0×10-20。
回答下列问题:
(1)“氧化碱浸”时,为提高反应速率,可采取的措施有
(2)向滤液1中加入乙醇生成Ru(OH)4沉淀和乙醛,则“转化”过程中乙醇作
(3)①Ru(OH)4与NaClO发生反应的化学方程式为

②“蒸馏”过程中常采用的加热方式为
(4)盐酸“吸收”RuO4过程中产生的Cl2经进一步处理可以转化为
(5)滤渣3的主要成分为
(6)“沉淀”时,向1L 1.0 mol· L-1BiCl3溶液中加入0.2L Na2S溶液,反应后混合溶液中c(S2-)为1×10-6mol·L-1,则Bi3+的沉淀率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】草酸铁铵[(NH4)3Fe(C2O4)3]是一种常用的金属着色剂,易溶于水, 常温下其水溶液pH介于4.0 ~5.0之间。某化学兴趣小组设计实验制备草酸铁铵并测定其纯度。
(1)由HNO3氧化葡萄糖(C6H12O6)制取草酸,实验装置如图:
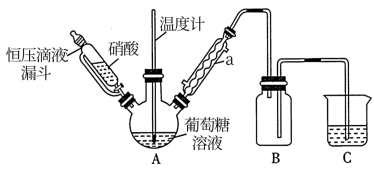
①仪器a的名称是___________ 。
②在55~60℃下,装置A中生成H2C2O4,同时生成NO和NO2,且物质的量之比为1:3,该反应的化学方程式为___________ 。
③装置B的作用是___________ 。
(2)提纯上述所得的草酸溶液后,制备草酸铁铵的流程如下:
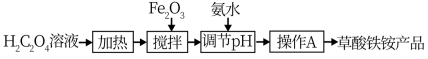
“操作A”包括___________ 、 过滤、 洗涤和干燥。
(3)测定所得草酸铁铵产品的纯度。
准确称量5.000g所得产品配成100 mL溶液,取10.00 mL于锥形瓶中,加入足量0.1000mol·L-1稀硫酸酸化后,再用0.1000 mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液的体积为12.00 mL。
[已知滴定反应原理为:H2C2O4+MnO +H+→Mn2++CO2↑+H2O(未配平)
+H+→Mn2++CO2↑+H2O(未配平)
①滴定终点的现象是___________ 。
②计算产品中(NH4)3Fe(C2O4)3的质量分数___________ 。[写出计算过程。(NH4)3Fe(C2O4)3的摩尔质量为374 g·mol-1]
(1)由HNO3氧化葡萄糖(C6H12O6)制取草酸,实验装置如图:

①仪器a的名称是
②在55~60℃下,装置A中生成H2C2O4,同时生成NO和NO2,且物质的量之比为1:3,该反应的化学方程式为
③装置B的作用是
(2)提纯上述所得的草酸溶液后,制备草酸铁铵的流程如下:

“操作A”包括
(3)测定所得草酸铁铵产品的纯度。
准确称量5.000g所得产品配成100 mL溶液,取10.00 mL于锥形瓶中,加入足量0.1000mol·L-1稀硫酸酸化后,再用0.1000 mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液的体积为12.00 mL。
[已知滴定反应原理为:H2C2O4+MnO
 +H+→Mn2++CO2↑+H2O(未配平)
+H+→Mn2++CO2↑+H2O(未配平)①滴定终点的现象是
②计算产品中(NH4)3Fe(C2O4)3的质量分数
您最近一年使用:0次

 )的pH
)的pH )的pH
)的pH

