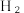 是一种理想的清洁能源,
是一种理想的清洁能源,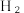 的制取与储存是氢能源利用领域的研究热点,探索绿色化制氢是化学界的一个热门话题。
的制取与储存是氢能源利用领域的研究热点,探索绿色化制氢是化学界的一个热门话题。(1)氧缺位铁酸铜
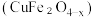 可用作太阳能热化学循环分解
可用作太阳能热化学循环分解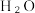 制取
制取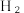 的催化剂。
的催化剂。①氧缺位铁酸铜分解水制氢分为两步。已知第一步反应为:
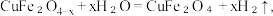 ,写出第二步反应的化学方程式
,写出第二步反应的化学方程式②下图为电化学方法获得
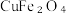 的原理装置图,写出其阳极的电极反应式
的原理装置图,写出其阳极的电极反应式
(2)一种利用
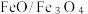 之间的相互转化,来裂解水制取
之间的相互转化,来裂解水制取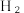 ,的工艺流程如下图所示。该工艺制氢的总反应为
,的工艺流程如下图所示。该工艺制氢的总反应为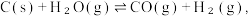 相比于水和碳在高温下直接接触反应来制氢,分析该工艺制氢的最大优点为
相比于水和碳在高温下直接接触反应来制氢,分析该工艺制氢的最大优点为
(3)硼氢化钠
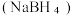 的强碱溶液在催化剂作用下可与水反应可获取
的强碱溶液在催化剂作用下可与水反应可获取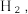 ,其可能的反应机理如下图所示。
,其可能的反应机理如下图所示。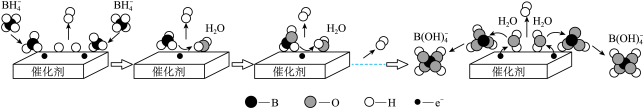
已知:常温下,NaB(OH)₄在水中的溶解度不大,易以
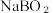 ₂形式结晶析出。
₂形式结晶析出。①写出图示最后一个步骤的反应机理
②用
 来代替
来代替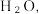 根据上述反应机理,反应后生成的气体中应含有
根据上述反应机理,反应后生成的气体中应含有③其他条件相同时,测得平均每克催化剂使用量下,
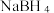 的浓度和放氢速率的变化关系如图所示。解释当
的浓度和放氢速率的变化关系如图所示。解释当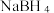 浓度大于
浓度大于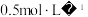 时,放氢速率减小的原因可能是
时,放氢速率减小的原因可能是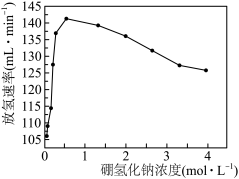
更新时间:2023-11-22 14:50:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按照题目要求完成下列离子方程式
(1)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式:_____________________________ 。
(2)含氯消毒剂可防甲型H1N1流感。二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式:_______________________________ 。
(3)FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)_________________________________ 。
(4)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:____________________________ 。
(1)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式:
(2)含氯消毒剂可防甲型H1N1流感。二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式:
(3)FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)
(4)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:
您最近一年使用:0次
【推荐2】KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯。其反应可表述为:
________ KClO3+________ HCl(浓) ===________ KCl+________ ClO2↑+________ Cl2↑+________ H2O
(1)配平以上化学方程式(写出各物质的化学计量数)。
(2)ClO2是反应的_________ (填“氧化”或“还原”)产物。浓盐酸在反应中显示出来的性质是________ (填字母)。
a.还原性 b.氧化性 c.酸性 d.碱性
(3)反应产生0.1 mol Cl2,则转移的电子的物质的量为________ mol。
(4)ClO2具有很强的氧化性,因此可被用来做消毒剂,若ClO2作消毒剂后其自身转化为Cl−,则其消毒的效率(以单位质量得到电子数表示)是Cl2的________ 倍(保留2位小数)。
(1)配平以上化学方程式(写出各物质的化学计量数)。
(2)ClO2是反应的
a.还原性 b.氧化性 c.酸性 d.碱性
(3)反应产生0.1 mol Cl2,则转移的电子的物质的量为
(4)ClO2具有很强的氧化性,因此可被用来做消毒剂,若ClO2作消毒剂后其自身转化为Cl−,则其消毒的效率(以单位质量得到电子数表示)是Cl2的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式_______ (如果系数是1,不用填写):

(2)整个过程中的还原剂是_______ 。
(3)把KI换成KBr,则CCl4层变为_______ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)500kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2_______ L(标准状况,保留2位小数)。
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式

(2)整个过程中的还原剂是
(3)把KI换成KBr,则CCl4层变为
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)500kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
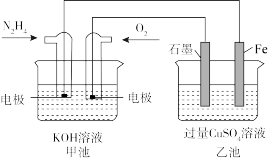
【推荐1】图中甲池的电池总反应式为N2H4+O2=N2+2H2O,回答下列问题:_______ ,其发生氧化反应的电极上的电极反应式为_______ 。
(2)常温下,乙池中CuSO4溶液的体积为0.04L,甲池中通入标准状况下22.4mL的O2时,乙池中CuSO4溶液的pH为_________ (忽略溶液体积变化)。
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的______ (填字母)。
(4)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中铁电极增加的质量为________ g。
(5)已知:2H++2CrO (黄色)
(黄色) Cr2O
Cr2O (橙色)+H2O。利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7,的总反应方程式为4Na2CrO4+4H2O
(橙色)+H2O。利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7,的总反应方程式为4Na2CrO4+4H2O 2Na2Cr2O7+4NaOH+2H2↑+O2↑,则Na2Cr2O7在
2Na2Cr2O7+4NaOH+2H2↑+O2↑,则Na2Cr2O7在______ (填“阴”或“阳”)极室制得,电解时通过膜的离子主要为_______ (填离子符号)。
(2)常温下,乙池中CuSO4溶液的体积为0.04L,甲池中通入标准状况下22.4mL的O2时,乙池中CuSO4溶液的pH为
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的
| A.CuO | B.Cu(OH)2 | C.CuCO3 | D.CuSO4 |
(4)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中铁电极增加的质量为
(5)已知:2H++2CrO
 (黄色)
(黄色) Cr2O
Cr2O (橙色)+H2O。利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7,的总反应方程式为4Na2CrO4+4H2O
(橙色)+H2O。利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7,的总反应方程式为4Na2CrO4+4H2O 2Na2Cr2O7+4NaOH+2H2↑+O2↑,则Na2Cr2O7在
2Na2Cr2O7+4NaOH+2H2↑+O2↑,则Na2Cr2O7在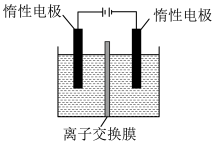
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图所示,p、q为直流电源的两极,A由金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D上产生气泡,试回答:
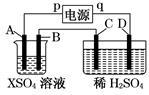
(1)p为________ 极,A极发生了________________ 反应。
(2)C为________ 极,可收集到_________________ ;
D为________ 极,可收集到___________________ 。
(3)C极的电极反应式为________________________ 。
(4)在电解过程中,测C、D两极上产生气体的体积,实验数据如下表:
仔细分析以上实验数据,请说出变化的可能原因是___________________ 。
(5) 当电路中通过0.004 mol电子时,B极上沉积的金属X为0.128 g,则此金属的摩尔质量为_______

(1)p为
(2)C为
D为
(3)C极的电极反应式为
(4)在电解过程中,测C、D两极上产生气体的体积,实验数据如下表:
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极产生气体的体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极产生气体的体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
仔细分析以上实验数据,请说出变化的可能原因是
(5) 当电路中通过0.004 mol电子时,B极上沉积的金属X为0.128 g,则此金属的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)固体氧化物燃料电池的工作原理如图所示,已知电池中电解质为熔融固体氧化物,O2-可以在其中自由移动。当燃料气为C2H4时,其正极、负极反应式分别为
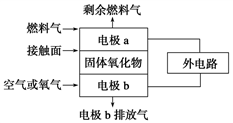
正极:______________________ ;
负极:____________________ 。
(2)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则Co2+在阳极的电极反应式为__________________ ;除去甲醇的离子方程式为___________ 。
(3)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。
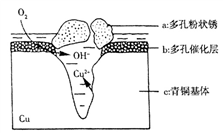
①环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为______________________ ;
②若生成4.29 g Cu2(OH)3Cl,则理论上耗氧气体积为___________ L(标准状况)。

正极:
负极:
(2)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如图所示装置模拟上述过程,则Co2+在阳极的电极反应式为
(3)如图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

①环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为
②若生成4.29 g Cu2(OH)3Cl,则理论上耗氧气体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】超酸是一类比纯硫酸更强的酸,在石油重整中用作高效催化剂。某实验小组对超酸HSbF6的制备及性质进行了探究。由三氯化锑(SbCl3)制备HSbF6的反应如下: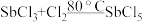 、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
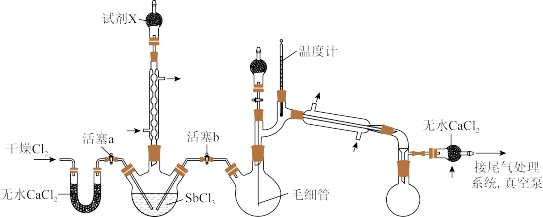
相关性质如表:
回答下列问题:
(1)实验小组在由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为_______ (写化学反应方程式)。
(2)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为_______ 。
(3)实验小组在探究实验中发现蜡烛可以溶解于HSbF6中,同时放出氢气。已知烷烃分子中碳氢键的活性大小顺序为:甲基(—CH3)<亚甲基(—CH2—)<次甲基(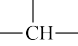 )。写出2-甲基丙烷与HSbF6反应的离子方程式
)。写出2-甲基丙烷与HSbF6反应的离子方程式_______ 。
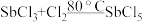 、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
相关性质如表:
| 物质 | 熔点 | 沸点 | 性质 |
| SbCl3 | 73.4℃ | 220.3℃ | 极易水解 |
| SbCl5 | 3.5℃ | 140℃分解79℃/2.9kPa | 极易水解 |
回答下列问题:
(1)实验小组在由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为
(2)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为
(3)实验小组在探究实验中发现蜡烛可以溶解于HSbF6中,同时放出氢气。已知烷烃分子中碳氢键的活性大小顺序为:甲基(—CH3)<亚甲基(—CH2—)<次甲基(
 )。写出2-甲基丙烷与HSbF6反应的离子方程式
)。写出2-甲基丙烷与HSbF6反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。
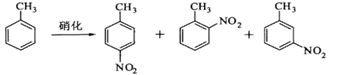
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(1)上述实验中过滤的目的是________________________ 。
(2)滤液在分液漏斗中洗涤静置后,有机层处于______ 层(填“上”或'下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有_______________ 。
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为______________ 。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是___________________ 。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有____________ 。
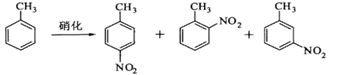
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(1)上述实验中过滤的目的是
(2)滤液在分液漏斗中洗涤静置后,有机层处于
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
| 催化剂 | n(催化剂) n(甲苯) | 硝化产物中各种异构体质量分数(%) | 总产率(%) | ||
| 对硝基甲苯 | 邻硝基甲苯 | 间硝基甲苯 | |||
| 浓H2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 98.0 |
| 1.2 | 36.5 | 59.5 | 4.0 | 99.8 | |
| NaHSO4 | 0.15 | 44.6 | 55.1 | 0.3 | 98.9 |
| 0.25 | 46.3 | 52.8 | 0.9 | 99.9 | |
| 0.32 | 47.9 | 51.8 | 0.3 | 99.9 | |
| 0.36 | 45.2 | 54.2 | 0.6 | 99.9 | |
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】非金属元素在化工生产中扮演着重要的角色。在众多的化工原料和产品中,都能见到硅、硫和氮等元素的踪迹。
I.利用下列物品回答问题:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片
(1)直接使用了硅单质的是_______ (填标号,下同)。
(2)直接使用了二氧化硅的是_______ 。
II.硫、氮的氧化物是大气的主要污染物,汽车尾气、工业废气、烟道气等中均含有硫或氮元素的氧化物,主要以 和
和 的形式存在。
的形式存在。
(3)下列关于 和
和 的叙述中正确的是_______(填标号)。
的叙述中正确的是_______(填标号)。
(4)质量相同的 和
和 的物质的量之比为
的物质的量之比为_______ 。
(5) 能被酸性
能被酸性 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:_______ 。
(6)利用氨水可以将 和
和 吸收,其原理如图所示:
吸收,其原理如图所示:
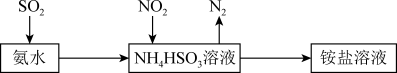
用氨水吸收 能得到含
能得到含 和
和 的吸收液,写出生成
的吸收液,写出生成 反应的离子方程式:
反应的离子方程式:_______ 。若向吸收液中通入过量 ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,此反应中氧化剂与还原剂的物质的量之比为
,此反应中氧化剂与还原剂的物质的量之比为_______ 。
I.利用下列物品回答问题:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片
(1)直接使用了硅单质的是
(2)直接使用了二氧化硅的是
II.硫、氮的氧化物是大气的主要污染物,汽车尾气、工业废气、烟道气等中均含有硫或氮元素的氧化物,主要以
 和
和 的形式存在。
的形式存在。(3)下列关于
 和
和 的叙述中正确的是_______(填标号)。
的叙述中正确的是_______(填标号)。| A.两种气体都无色有毒,且都可用水吸收以消除对空气的污染 |
B.实验室制备 、 、 时,均可用向上排空气的方法收集 时,均可用向上排空气的方法收集 |
| C.两种气体都具有强氧化性,因此都能够使品红溶液褪色 |
D. 与 与 反应转化为 反应转化为 ,属于氮的固定 ,属于氮的固定 |
 和
和 的物质的量之比为
的物质的量之比为(5)
 能被酸性
能被酸性 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:(6)利用氨水可以将
 和
和 吸收,其原理如图所示:
吸收,其原理如图所示:
用氨水吸收
 能得到含
能得到含 和
和 的吸收液,写出生成
的吸收液,写出生成 反应的离子方程式:
反应的离子方程式: ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,此反应中氧化剂与还原剂的物质的量之比为
,此反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次



