已知反应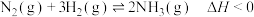 ,平衡时
,平衡时 的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是

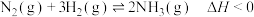 ,平衡时
,平衡时 的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
的体积百分数随温度的变化曲线如图所示,下列相关描述正确的是
A.平衡常数值: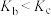 |
B. 温度下,若由a点达到 温度下,若由a点达到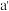 ,可以采取减小压强的方法 ,可以采取减小压强的方法 |
C.d点: |
D.从b点变为 点,增加 点,增加 的物质的量 的物质的量 |
更新时间:2023-12-14 12:34:39
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】反应N2O4(g)⇌2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
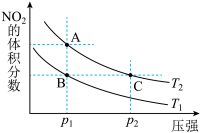

| A.A、C两点的反应速率:A>C |
| B.A、C两点气体的颜色:A、C两点一样颜色 |
| C.由状态A到状态B,可以用降温的方法 |
| D.A、C两点气体的平均相对分子质量:A>C |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验事实可以用平衡移动原理解释的是
| A.“NO2”球浸泡在热水中,颜色变深 |
B.H2(g)+ I2 (g)  2HI(g),加压后颜色变深 2HI(g),加压后颜色变深 |
| C.过量铁和稀硝酸反应,溶液变成浅绿色 |
| D.合成氨工业中使用铁触媒作催化剂 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】NO氧化反应2NO(g)+O2(g) ⇌2NO2(g)分两步进行:I.2NO(g) ⇌N2O2(g) ∆H1;II.N2O2(g)+O2(g) ⇌2NO2(g) ∆H2,其反应过程能量变化示意图如图,下列说法不正确的是
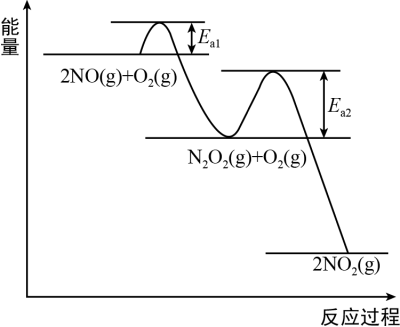

| A.由于 Ea1<Ea2,决定化学反应速率快慢的是反应Ⅱ |
| B.图示过程中,反应物断键吸收的能量小于生成物形成所释放的能量 |
| C.其它条件不变,升高温度,2NO(g)+O2(g) ⇌2NO2(g)反应速率一定加快 |
| D.其它条件不变,升高温度,2NO(g)+O2(g) ⇌2NO2(g)平衡一定逆向移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中,不能用勒夏特列原理解释的是
| A.90℃纯水的pH<7 |
| B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 |
| C.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
D.溴水中存在如下平衡: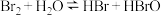 ,当加入NaOH溶液后颜色变浅 ,当加入NaOH溶液后颜色变浅 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】对已达化学平衡的下列反应 2X(g)+Y(g) 2Z(g),增大容积,减小压强时,对反应产生的影响是( )
2Z(g),增大容积,减小压强时,对反应产生的影响是( )
 2Z(g),增大容积,减小压强时,对反应产生的影响是( )
2Z(g),增大容积,减小压强时,对反应产生的影响是( )| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向正反应方向移动 |
| D.正、逆反应速率都减小,平衡向逆反应方向移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】反应mX(g)=nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示。下列说法错误的是
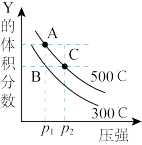

| A.m<n+p |
| B.该反应的ΔH<0 |
| C.A、C两点化学平衡常数:KA=KC |
| D.A、C两点的反应速率:v(A)<v(C) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在某密闭容器中发生:2SO2(g)+O2(g)⇌2SO3(g),反应混合体系在平衡状态时 SO3 的百分含量与温度的关系如图所示。下列说法不正确的是


| A.在 D 点时 v正>v逆 |
| B.反应 2SO2(g)+O2(g)⇌2SO3(g)的∆H>0 |
| C.A、B、C 三点反应速率最快的是 C 点 |
| D.恒温恒压下向平衡体系中通入氦气,平衡向左移动 |
您最近半年使用:0次




