类别万千的酸碱溶液共同构筑了化学世界的丰富多彩。
(1)现有常温下pH=2的盐酸(甲)、pH=2的醋酸溶液(乙)和0.1mol/L NH3∙H2O (丙),请根据下列操作回答:
①常温下,将丙溶液加水稀释,下列数值一定变小的是_____ (填字母)。
A. B.
B. C.
C. D.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙_____ 甲(填“>”“<”或“=”)。
(2)①某温度时,测得0.01mol/LNaOH溶液pH为11,则该温度_____ 25℃。(填“>”“<”或“=”)
②相同条件下,取等体积、等pH的Ba(OH)2、NaOH和NH3∙H2O三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 、
、 、
、 ,则三者的大小关系为
,则三者的大小关系为_____ 。
③某温度下,测得0.001mol/L的HCl溶液中水电离出的c(H+)=1×10-9mol∙L-1,将VaLpH=4HCl溶液和VbLpH=9的Ba(OH)2溶液混合均匀,测得溶液的pH=7,则Va:Vb=_____ 。
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
①将SO2通入氨水中,当c(OH-)降至1.0×10-7mol∙L-1时,溶液中的 =
=_____ 。
②下列微粒在溶液中不能大量共存的是_____ 。
A. 、
、 B.
B. 、
、 C.
C. 、
、 D.
D. 、
、
(1)现有常温下pH=2的盐酸(甲)、pH=2的醋酸溶液(乙)和0.1mol/L NH3∙H2O (丙),请根据下列操作回答:
①常温下,将丙溶液加水稀释,下列数值一定变小的是
A.
 B.
B. C.
C. D.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙
(2)①某温度时,测得0.01mol/LNaOH溶液pH为11,则该温度
②相同条件下,取等体积、等pH的Ba(OH)2、NaOH和NH3∙H2O三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
 、
、 、
、 ,则三者的大小关系为
,则三者的大小关系为③某温度下,测得0.001mol/L的HCl溶液中水电离出的c(H+)=1×10-9mol∙L-1,将VaLpH=4HCl溶液和VbLpH=9的Ba(OH)2溶液混合均匀,测得溶液的pH=7,则Va:Vb=
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
| 弱电解质 | H2SO3 | H2CO3 | HClO | NH3∙H2O |
| 电离平衡常数 |   |   |  |  |
 =
=②下列微粒在溶液中不能大量共存的是
A.
 、
、 B.
B. 、
、 C.
C. 、
、 D.
D. 、
、
更新时间:2023-11-23 18:40:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】水在25℃和95℃时电离平衡曲线如图。

(1)25℃时水的电离平衡曲线应为___________ (“A”或“B”)。25℃时,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为___________ 。
(2)95℃时,若100体积 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性;则a与b之间应满足的关系是
的某强碱溶液混合后溶液呈中性;则a与b之间应满足的关系是___________ 。
(3)在曲线A所对应的温度下, 的
的 溶液和
溶液和 的某
的某 溶液中,若水的电离程度分别用
溶液中,若水的电离程度分别用 、
、 表示,则
表示,则
___________  (填“大于”“小于”“等于”“无法确定”)
(填“大于”“小于”“等于”“无法确定”)
(4)在曲线B所对应的温度下,将 的
的 溶液与等物质的量浓度的
溶液与等物质的量浓度的 溶液等体积混合,所得混合液的
溶液等体积混合,所得混合液的
___________ 。

(1)25℃时水的电离平衡曲线应为
 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为(2)95℃时,若100体积
 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性;则a与b之间应满足的关系是
的某强碱溶液混合后溶液呈中性;则a与b之间应满足的关系是(3)在曲线A所对应的温度下,
 的
的 溶液和
溶液和 的某
的某 溶液中,若水的电离程度分别用
溶液中,若水的电离程度分别用 、
、 表示,则
表示,则
 (填“大于”“小于”“等于”“无法确定”)
(填“大于”“小于”“等于”“无法确定”)(4)在曲线B所对应的温度下,将
 的
的 溶液与等物质的量浓度的
溶液与等物质的量浓度的 溶液等体积混合,所得混合液的
溶液等体积混合,所得混合液的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】水是生命的源泉、工业的血液、城市的血脉。要保护好河流,因为河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和灌溉农田间接危及健康。请回答下列问题:
(1)纯水在T ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=________ mol·L-1。
(2)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其主要水解反应的离子方程式为____________________ ,由水电离出的c(OH-)=________ mol·L-1。
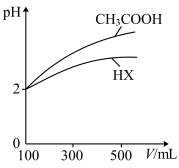
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________ (填“大于”“小于”或“等于”)CH3COOH的电离平衡常数。
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
在25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为________ (用化学式表示)。

(1)纯水在T ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=
(2)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其主要水解反应的离子方程式为
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
| 化学式 | 电离常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
在25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)相同浓度的下列溶液中:①CH3COONH4②CH3COONa③CH3COOH中,其中c(CH3COO-)由大到小的顺序是___ ;浓度均为0.1mol/L的①H2S②NaHS③Na2S④H2S和NaHS混合液,溶液的pH从大到小的顺序是___ 。
(2)常温下,pH=11的CH3COONa溶液,其中水电离出来的c(OH-)=___ ,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=___ 。
(3)25℃时,若Ksp[Fe(OH)3]=2.8×10-39,该温度下Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数K=___ ;若H2SO3⇌HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=___ ,向NaHSO3溶液中加入少量的I2,则溶液中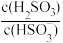 将
将___ (填“增大”“减小”或“不变”)。
(2)常温下,pH=11的CH3COONa溶液,其中水电离出来的c(OH-)=
(3)25℃时,若Ksp[Fe(OH)3]=2.8×10-39,该温度下Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数K=
 +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=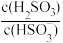 将
将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】填空题
(1)KHSO4溶液的pH______ (填“>”“<”或“=”)7,用离子方程式表示为___________ 。
(2)KHCO3溶液的pH_____ (填“>”“<”或“=”)7,用离子方程式表示为____________ 。
(3)将上述两种溶液混合,现象是_______________ ,用离子方程式表示为___________ 。
(1)KHSO4溶液的pH
(2)KHCO3溶液的pH
(3)将上述两种溶液混合,现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空:
(1)在配制氯化铁溶液时,为了防止发生水解,可以加入少量的________________ 。
(2)氯化铝溶液具有净水的作用,原因是(用离子方程式表示):_______________ 。
(3)已知CO (g) + H2O (g) CO2 (g) + H2 (g),在800℃时,该反应的化学平衡常数K=1.0,某时刻在一密闭容器中含1.0molCO、1.2mol H2O、0.75molCO2、2mol H2 ,则上述条件下此反应v正
CO2 (g) + H2 (g),在800℃时,该反应的化学平衡常数K=1.0,某时刻在一密闭容器中含1.0molCO、1.2mol H2O、0.75molCO2、2mol H2 ,则上述条件下此反应v正________ v逆(填“>”“<”或“=”)。
(4)将25℃下pH=12的NaOH溶液a L与pH=1的HCl溶液b L混合。若所得混合液为中性,则a:b=_____________________ 。
(5)写出0.1mol/LNaOH溶液1L与标准状况下1.12LCO2完全反应后所得的溶液中各种离子浓度由大到小的顺序为____________________________ 。
(6)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为________________ 。用该原电池做电源,常温下,用惰性电极电解200 mL饱和食盐水(足量),消耗标准状况下的CO 的体积为224 mL,则溶液的pH = ___________ 。(不考虑溶液体积的变化)

(1)在配制氯化铁溶液时,为了防止发生水解,可以加入少量的
(2)氯化铝溶液具有净水的作用,原因是(用离子方程式表示):
(3)已知CO (g) + H2O (g)
 CO2 (g) + H2 (g),在800℃时,该反应的化学平衡常数K=1.0,某时刻在一密闭容器中含1.0molCO、1.2mol H2O、0.75molCO2、2mol H2 ,则上述条件下此反应v正
CO2 (g) + H2 (g),在800℃时,该反应的化学平衡常数K=1.0,某时刻在一密闭容器中含1.0molCO、1.2mol H2O、0.75molCO2、2mol H2 ,则上述条件下此反应v正(4)将25℃下pH=12的NaOH溶液a L与pH=1的HCl溶液b L混合。若所得混合液为中性,则a:b=
(5)写出0.1mol/LNaOH溶液1L与标准状况下1.12LCO2完全反应后所得的溶液中各种离子浓度由大到小的顺序为
(6)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)实验室中有一未知浓度的稀盐酸,某学生测定盐酸的浓度在实验室中进行实验。请完成下列填空:配制400mL0.10mol/LNaOH标准溶液,取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
①滴定达到终点的标志是_______ 。
②根据上述数据,可计算出该盐酸的浓度约为_______ (保留两位有效数字)。
(2)某温度(T)下的溶液中,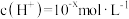 ,
,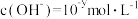 ,x与y的关系如图所示,请回答下列问题:
,x与y的关系如图所示,请回答下列问题:

在此温度下,将0.1 的
的 溶液与0.1
溶液与0.1 的
的 溶液按下表中甲、乙、丙、丁四种不同方式混合:
溶液按下表中甲、乙、丙、丁四种不同方式混合:
①按丁方式混合后,所得溶液显_______ (填“酸”“碱”或“中”)性。
②写出按乙方式混合反应的离子方程式:_______ 。
③按甲方式混合后所得溶液的pH为_______ 。
(3)25℃时,有甲、乙两瓶溶液,其pH分别为m、n,且m=2n(m、n均为小于14的正整数),则下列叙述正确的是_______ 。
a.若甲溶液呈碱性,则乙溶液可能呈碱性,且c(OH-)甲>c(OH-)乙
b.c(H+)甲=c2(H+)乙
c.若乙溶液呈酸性,则甲溶液必定呈酸性,且c(H+)甲>c(H+)乙
d.若甲溶液呈酸性,则乙溶液必定呈酸性,且c(OH-)甲>c(OH-)乙
(1)实验室中有一未知浓度的稀盐酸,某学生测定盐酸的浓度在实验室中进行实验。请完成下列填空:配制400mL0.10mol/LNaOH标准溶液,取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
| 实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 24.12 | 20.00 |
| 2 | 0.10 | 24.08 | 20.00 |
| 3 | 0.10 | 24.10 | 20.00 |
①滴定达到终点的标志是
②根据上述数据,可计算出该盐酸的浓度约为
(2)某温度(T)下的溶液中,
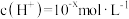 ,
,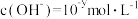 ,x与y的关系如图所示,请回答下列问题:
,x与y的关系如图所示,请回答下列问题:
在此温度下,将0.1
 的
的 溶液与0.1
溶液与0.1 的
的 溶液按下表中甲、乙、丙、丁四种不同方式混合:
溶液按下表中甲、乙、丙、丁四种不同方式混合:| 甲 | 乙 | 丙 | 丁 | |
0.1  溶液体积/mL 溶液体积/mL | 10 | 10 | 10 | 10 |
0.1  溶液体积/mL 溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显
②写出按乙方式混合反应的离子方程式:
③按甲方式混合后所得溶液的pH为
(3)25℃时,有甲、乙两瓶溶液,其pH分别为m、n,且m=2n(m、n均为小于14的正整数),则下列叙述正确的是
a.若甲溶液呈碱性,则乙溶液可能呈碱性,且c(OH-)甲>c(OH-)乙
b.c(H+)甲=c2(H+)乙
c.若乙溶液呈酸性,则甲溶液必定呈酸性,且c(H+)甲>c(H+)乙
d.若甲溶液呈酸性,则乙溶液必定呈酸性,且c(OH-)甲>c(OH-)乙
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度下,Kw=1×10-12。此温度下,将pH=11的苛性钠溶液V1L与pH=1的硫酸溶液V2L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=2,则V1:V2=____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】25 ℃时,将体积Va、pH=a的某一元强碱与体积为Vb、pH=b的某二元强酸混合。
(1)若所得溶液的pH=11,且a=13,b=2,则Va∶Vb=____________ 。
(2)若所得溶液的pH=7,且已知Va>Vb,b=0.5a,b值可否等于4________ (填“可”或“否”)。
(3)为了更好的表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG的定义为AG=lg 。25 ℃时,若溶液呈中性,则AG=
。25 ℃时,若溶液呈中性,则AG=________ ,溶液的pH与AG的换算公式为AG=__________________ 。
(1)若所得溶液的pH=11,且a=13,b=2,则Va∶Vb=
(2)若所得溶液的pH=7,且已知Va>Vb,b=0.5a,b值可否等于4
(3)为了更好的表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG的定义为AG=lg
 。25 ℃时,若溶液呈中性,则AG=
。25 ℃时,若溶液呈中性,则AG=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】水的电离平衡曲线如图所示。若以A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态为B点。
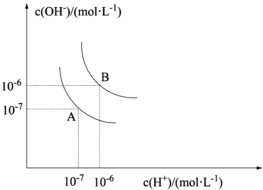
(1)在100℃时,Kw的表达式为_____ ,在此温度下,Kw的值为_____ mol2/L2.
(2)在室温下,将pH=9的Ba(OH)2溶液与pH=5的稀盐酸混合,欲使混合溶液pH=7,则Ba(OH)2溶液与盐酸的体积比为_____ ,物质的量浓度比为_____
(3)室温时将pH为3的硫酸溶液稀释5百万倍,稀释后溶液中,c( )和c(H+)之比约为
)和c(H+)之比约为_____ 。
Ⅱ.现有溶质为①CH3COOH,②HCl、③H2SO4的三种溶液,根据要求回答下列问题:
(4)写出①的电离方程式:_____ 。
(5)当它们pH相同时,其物质的量浓度最大的是_____ (填序号)。
(6)当它们的物质的量浓度相同时,其pH最小的是_____ (填序号)。
(7)在室温下,将c(H+)均为0.1mol/L的三种酸分别加水稀释至原来的10倍,c(H+)由大到小的顺序为_____ (填序号)。
(8)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积比为_____ 。
(9)三种酸溶液的pH相同时,若消耗等量的Zn,则需三种酸溶液的体积大小关系为_____ (填序号)。

(1)在100℃时,Kw的表达式为
(2)在室温下,将pH=9的Ba(OH)2溶液与pH=5的稀盐酸混合,欲使混合溶液pH=7,则Ba(OH)2溶液与盐酸的体积比为
(3)室温时将pH为3的硫酸溶液稀释5百万倍,稀释后溶液中,c(
 )和c(H+)之比约为
)和c(H+)之比约为Ⅱ.现有溶质为①CH3COOH,②HCl、③H2SO4的三种溶液,根据要求回答下列问题:
(4)写出①的电离方程式:
(5)当它们pH相同时,其物质的量浓度最大的是
(6)当它们的物质的量浓度相同时,其pH最小的是
(7)在室温下,将c(H+)均为0.1mol/L的三种酸分别加水稀释至原来的10倍,c(H+)由大到小的顺序为
(8)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积比为
(9)三种酸溶液的pH相同时,若消耗等量的Zn,则需三种酸溶液的体积大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)H2S分子中H-S键的键角为92°,说明H2S分子是_____ (选填“极性”“非极性”)分子。可用FeS与稀硫酸制取 H2S气体,而CuS不溶于稀硫酸,请据此比较FeS、H2S、CuS这三种物质电离或溶解出S2-的能力__________________ 。实验室制取并收集H2S气体,除FeS和稀硫酸外,还必需的试剂是___________ 。
(2)在NaOH和NaClO混合溶液中,多硫化钠(Na2Sx)会被氧化为Na2SO4,此时1mol Na2Sx失去的电子数为_________ mol;若Na2Sx与NaClO反应的物质的量之比为1:10,则 x = ______ 。
(3)往Na2S和Na2S2O3混合溶液中加入稀硫酸,指出反应现象_____________________________ 。
(4)已知25℃:H2S Ki1 = 9.1×10-8,Ki2 = 1.1×10-12;H2SO3Ki1 = 1.5×10-2,Ki2 = 1.0×10-7
将a mol SO2通入含b mol Na2S的溶液中完全反应,若没有硫化氢气体产生,则a:b的值为______ 。
(2)在NaOH和NaClO混合溶液中,多硫化钠(Na2Sx)会被氧化为Na2SO4,此时1mol Na2Sx失去的电子数为
(3)往Na2S和Na2S2O3混合溶液中加入稀硫酸,指出反应现象
(4)已知25℃:H2S Ki1 = 9.1×10-8,Ki2 = 1.1×10-12;H2SO3Ki1 = 1.5×10-2,Ki2 = 1.0×10-7
将a mol SO2通入含b mol Na2S的溶液中完全反应,若没有硫化氢气体产生,则a:b的值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】酸碱混合时可以得到滴定图象、物种分布图象等。
(1)室温下,用未知浓度NaOH溶液分别滴定20.00 mL物质的量浓度相同的盐酸和醋酸,所得溶液的pH随NaOH溶液体积的变化如下图甲所示。

①在滴定的某时刻,滴定管中液面如图乙所示,此时滴定管读数为_______ mL。
②A点时溶液中c(Na+)、c(CH3COOH)、c(CH3COO-)由大到小的顺序为_______ 。
③B点时溶液中由水电离出的c(H+)=_______ 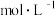 。
。
(2)已知25℃时,向 的
的 溶液中滴加NaOH溶液,各含磷微粒的分布系数δ随pH变化的关系如图丙所示。
溶液中滴加NaOH溶液,各含磷微粒的分布系数δ随pH变化的关系如图丙所示。
①酚酞的变色范围为8.2~10,若以酚酞为指示剂,当溶液由无色变为浅红色时主要反应的离子方程式为_______ 。
②25℃,磷酸的Ka1=_______ pH=3时溶液中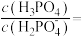
_______ 。
(1)室温下,用未知浓度NaOH溶液分别滴定20.00 mL物质的量浓度相同的盐酸和醋酸,所得溶液的pH随NaOH溶液体积的变化如下图甲所示。

①在滴定的某时刻,滴定管中液面如图乙所示,此时滴定管读数为
②A点时溶液中c(Na+)、c(CH3COOH)、c(CH3COO-)由大到小的顺序为
③B点时溶液中由水电离出的c(H+)=
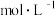 。
。(2)已知25℃时,向
 的
的 溶液中滴加NaOH溶液,各含磷微粒的分布系数δ随pH变化的关系如图丙所示。
溶液中滴加NaOH溶液,各含磷微粒的分布系数δ随pH变化的关系如图丙所示。①酚酞的变色范围为8.2~10,若以酚酞为指示剂,当溶液由无色变为浅红色时主要反应的离子方程式为
②25℃,磷酸的Ka1=
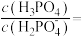
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知25℃时, 氨水(
氨水( )中,
)中, 为
为 。
。
(1)计算该溶液的
___________ 。
(2)氨水显弱碱性,其原因为___________ (用电离方程式表示),电离平衡常数的表达式为___________ 。
(3)25℃时, 的电离平衡常数约为。
的电离平衡常数约为。
(4)25℃时,向10mL0.1mol/L氨水中滴加相同浓度的 溶液,在滴加过程中
溶液,在滴加过程中 ___________(填字母)。
___________(填字母)。
 氨水(
氨水( )中,
)中, 为
为 。
。(1)计算该溶液的

(2)氨水显弱碱性,其原因为
(3)25℃时,
 的电离平衡常数约为。
的电离平衡常数约为。(4)25℃时,向10mL0.1mol/L氨水中滴加相同浓度的
 溶液,在滴加过程中
溶液,在滴加过程中 ___________(填字母)。
___________(填字母)。| A.始终减小 | B.始终增大 | C.先减小后增大 | D.先增大后减小 |
您最近一年使用:0次



