下列实验操作、装置图正确且能达到相应实验目的的是
| A | B | C | D |
 |  |  | 2NO2 N2O4(g) N2O4(g)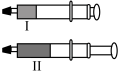 |
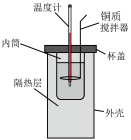
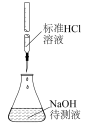
| 中和反应反应热的测定 | 用标准HCl溶液测定NaOH溶液的浓度 | 用已知浓度的FeCl3测定未知浓度的NaHSO3溶液 | 研究压强对平衡的影响,从Ⅰ状态拉到Ⅱ,压强减小平衡逆向移动,颜色加深 |
| A.A | B.B | C.C | D.D |
更新时间:2023-12-12 10:30:33
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验装置(固定装置略去)和操作正确的是
A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】选用下列仪器或装置不能达到实验目的的是
| A | B | C | D |
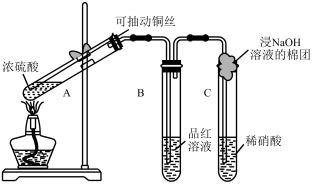 | 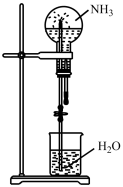 | 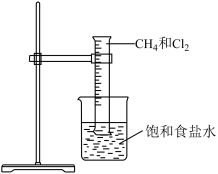 | 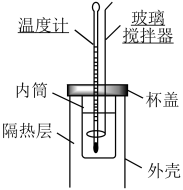 |
制取 并验证其氧化性 并验证其氧化性 | 氨气溶于水的喷泉实验 | 验证 与 与 的反应 的反应 | 利用简易量热计测定中和反应的反应热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】高中化学涉及的原理很多,掌握与应用好原理是学习好化学的理论基础。下列应用与对应原理不相符的是
| A.用CCl4 萃取碘水中的碘,应用了“相似相溶原理” |
B.反应2HI(g) H2(g)+ l2(g)达到平衡后,增大压强(减小体积),混合气体颜色加深,符合“平衡移动原理” H2(g)+ l2(g)达到平衡后,增大压强(减小体积),混合气体颜色加深,符合“平衡移动原理” |
| C.Fe的核外电子排布式:1s22s22p63s23p63d64s2,遵从“构造原理” |
D.3H2(g)+ N2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1;既符合“质量守恒原理”也遵从“能量守恒原理” 2NH3(g) ΔH=-92.4 kJ·mol-1;既符合“质量守恒原理”也遵从“能量守恒原理” |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
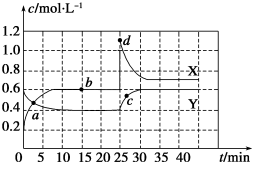
【推荐2】已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示。X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是
N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示。X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是
 N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示。X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是
N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示。X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是
| A.如混合气体的压强不再发生改变,说明反应已达化学平衡状态 |
| B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b点 |
| C.25~30 min内用NO2表示的平均化学反应速率是0.08 mol·L-1·min-1 |
| D.反应进行至25 min时,曲线发生变化的原因是增加N2O4的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用标准的盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验误差的是
| A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定 |
| B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定 |
| C.用蒸馏水洗净锥形瓶后,加入10.00mLNaOH溶液,再加入适量蒸馏水进行滴定 |
| D.用酚酞作指示剂滴至红色刚变无色时即停止加盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
A.保持温度不变,向稀氨水中缓慢通入适量 ,溶液中 ,溶液中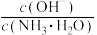 增大 增大 |
B.当过量的锌粉和盐酸反应时,为了减慢反应速率,又不影响产生 的总量,可向反应体系中加入少量的 的总量,可向反应体系中加入少量的 |
C.用标准 溶液滴定未知浓度的盐酸,滴定终点读数时俯视,所测结果偏高 溶液滴定未知浓度的盐酸,滴定终点读数时俯视,所测结果偏高 |
D.常温下,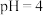 的 的 溶液与 溶液与 的 的 溶液中,前者水的电离程度大 溶液中,前者水的电离程度大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】完成下列实验所选择的装置或仪器不正确的是
| A | B | C | D | |
| 实验 | 实验分离水和酒精 | 用铵盐和碱制取氨气 | 用排空气法收集二氧化氮 | 用自来水制取蒸馏水 |
| 装置或仪器 | 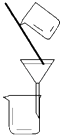 |  | 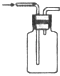 | 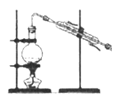 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法不正确的是
| A.双氧水不稳定,见光、遇热、遇大多数金属氧化物都会加快它的分解,但在碱性环境下分解较慢 |
| B.移液管和滴定管均标有使用温度,使用时均应进行润洗再装液 |
| C.除去NaCl晶体中的少量KNO3,可通过溶解、蒸发结晶、趁热过滤、洗涤、干燥 |
| D.实验室在取用药品时,多余的药品能否放回原试剂瓶要视具体情况而定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】三氯化铬(CrCl3)为紫色晶体,熔点为83℃,易潮解,易升华,不易水解,高温下易被氧气氧化,实验室用Cr2O3和CCl4(沸点76.8℃)在高温下制备三氯化铬,部分实验装置如图所示(夹持装置略),下列说法正确的是


| A.CCl4在反应中作氧化剂 |
| B.石棉绳的作用是保温,防止CrCl3凝华堵塞导管 |
| C.实验时应先点燃B处喷灯,再通X气体 |
| D.X气体可为空气 |
您最近一年使用:0次


 的反应为
的反应为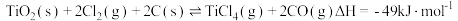 。下列说法正确的是
。下列说法正确的是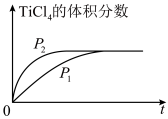
 值
值 减小,
减小, 增大
增大 ,达到新平衡时
,达到新平衡时 不变
不变 、时间变化曲线如图所示
、时间变化曲线如图所示

