“等效”是化学学科解决复杂体系问题的方法之一。密闭容器中充入4molSO2和2molO2,发生
 ,回答问题
,回答问题
(1)恒温恒容,达平衡时SO2的体积分数为a%,其他条件不变时,若按下列四种配比作为起始物质,平衡后SO2的体积分数仍为a%的是______。
(2)等体积的甲、乙、丙三个密闭容器,甲容器保持恒温恒容、乙容器保持恒温恒压、丙是恒容绝热容器,一段时间后三个容器均达到平衡,SO2的平衡转化率分别为 、
、 、
、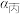 ,比较
,比较 、
、 、
、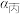 的大小
的大小______

 ,回答问题
,回答问题(1)恒温恒容,达平衡时SO2的体积分数为a%,其他条件不变时,若按下列四种配比作为起始物质,平衡后SO2的体积分数仍为a%的是______。
| A.2molSO3 | B.2molSO2+1molO2 |
| C.4molSO3 | D.2.5molSO2+1.25molO2+1.5molSO3 |
 、
、 、
、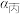 ,比较
,比较 、
、 、
、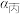 的大小
的大小
更新时间:2023-10-31 15:29:11
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,甲、乙、丙分别表示在不同条件下,可逆反应A(g)+B(g)  xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
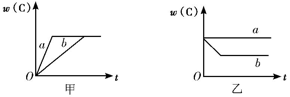
(1)若甲中两条曲线分别代表有催化剂和无催化剂的情况,则____ 曲线代表无催化剂时的情况。
(2)若乙表示反应达到平衡状态后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He后的情况,则___ 曲线表示恒温恒容的情况,且此时混合气体中w(C)___ (填“变大”“变小”或“不变”)。
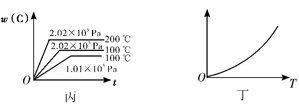
(3)根据丙可以判断该可逆反应的正反应是___ (填“放热”或“吸热”)反应,x的值为___ 。
(4)丁表示在某固定容积的密闭容器中,上述可逆反应达到平衡后,某物理量随温度(T)的变化情况,根据你的理解,丁的纵坐标可以是____ (填序号)。
①w(C) ②A的转化率 ③B的转化率 ④压强 ⑤c(A) ⑥c(B)
升高温度,平衡向____ (填“正反应”或“逆反应”)方向移动。
 xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。

(1)若甲中两条曲线分别代表有催化剂和无催化剂的情况,则
(2)若乙表示反应达到平衡状态后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He后的情况,则
(3)根据丙可以判断该可逆反应的正反应是
(4)丁表示在某固定容积的密闭容器中,上述可逆反应达到平衡后,某物理量随温度(T)的变化情况,根据你的理解,丁的纵坐标可以是
①w(C) ②A的转化率 ③B的转化率 ④压强 ⑤c(A) ⑥c(B)
升高温度,平衡向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】合成氨工业在工农业生产、生活中有着重要作用。反应原理为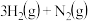 ⇌
⇌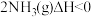 。
。
(1)在T℃时,将一定物质的量的 和
和 置于一容积不变的密闭容器中。
置于一容积不变的密闭容器中。
①下列各项能说明该反应已达到平衡状态的是_____ 填序号)。
a.容器内的压强不再随时间变化
b.3V正(N2)=2V逆(H2)
c.混合气体的密度保持不变
②上述反应达到平衡后,其他条件不变,升高温度,v逆_____ (填“增大”“不变”或“减小”),v正和v逆的关系为v正___________ v逆(填“>”“=”或“<”),最后二者相等。
③该条件下达到平衡时,向容器内充入惰性气体,增大容器内的压强, 的体积分数将(
的体积分数将( 填“变大”“不变”或“变小”)
填“变大”“不变”或“变小”)___________ 。
(2)在T℃时,将一定物质的量的 和
和 置于一容积可变的密闭容器中。达到平衡后,改变某一条件使反应速率发生了如图所示的变化,改变的条件可是 ___________。
置于一容积可变的密闭容器中。达到平衡后,改变某一条件使反应速率发生了如图所示的变化,改变的条件可是 ___________。
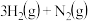 ⇌
⇌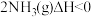 。
。(1)在T℃时,将一定物质的量的
 和
和 置于一容积不变的密闭容器中。
置于一容积不变的密闭容器中。①下列各项能说明该反应已达到平衡状态的是
a.容器内的压强不再随时间变化
b.3V正(N2)=2V逆(H2)
c.混合气体的密度保持不变
②上述反应达到平衡后,其他条件不变,升高温度,v逆
③该条件下达到平衡时,向容器内充入惰性气体,增大容器内的压强,
 的体积分数将(
的体积分数将( 填“变大”“不变”或“变小”)
填“变大”“不变”或“变小”)(2)在T℃时,将一定物质的量的
 和
和 置于一容积可变的密闭容器中。达到平衡后,改变某一条件使反应速率发生了如图所示的变化,改变的条件可是 ___________。
置于一容积可变的密闭容器中。达到平衡后,改变某一条件使反应速率发生了如图所示的变化,改变的条件可是 ___________。
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.保持温度、压强不变,增大反应物浓度 |
| D.保持温度、压强不变,减小生成物浓度 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g)  Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
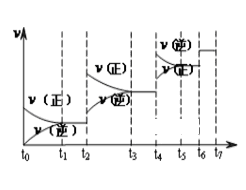
(1)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与 时间t的关系如图。图中t4时引起平衡移动的条件可能是______________________ ;图中表示平衡混合物中CO的含量最高的一段时间是____________ 。
(2)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是__________________ (提示:272 = 729)。
 Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)(1)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与 时间t的关系如图。图中t4时引起平衡移动的条件可能是
(2)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】完成下列问题
(1)某温度下,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
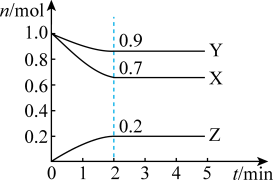
①该反应的化学方程式为:_______ 。
②反应开始至2min,以气体Z表示的平均反应速率为_______ 。
③2min反应达平衡容器内混合气体的平均相对分子质量是起始时的_______ 倍。
(2)反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率_______ (填“增大”“不变”或“减小”,下同),平衡 _______ 移动(填“不”“向正反应方向”或“向逆反应方向”,下同)。
②将容器的体积缩小一半,其正反应速率_______ ,平衡 _______ 移动。
③保持体积不变,充入N2使体系压强增大,其正反应速率_______ ,平衡 _______ 移动。
④保持体积不变,充入水蒸气,其正反应速率_______ ,平衡 _______ 移动。
(1)某温度下,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为:
②反应开始至2min,以气体Z表示的平均反应速率为
③2min反应达平衡容器内混合气体的平均相对分子质量是起始时的
(2)反应3Fe(s)+4H2O(g)
 Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一容积可变的密闭容器中进行,试回答:①增加Fe的量,其正反应速率
②将容器的体积缩小一半,其正反应速率
③保持体积不变,充入N2使体系压强增大,其正反应速率
④保持体积不变,充入水蒸气,其正反应速率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氨是最重要的氮肥,是产量最大的化工产品之一。其合成原理为:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ•mol-1。
2NH3(g) △H=-92.4kJ•mol-1。
(1)在密闭容器中,投入1molN2和3molH2在催化剂作用下发生反应,测得反应放出的热量_______ 92.4kJ(填“小于”、“大于”或“等于”)。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量_______ (填“变大”、“变小”或“不变”)。
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将_______ (填“正向”、“逆向”或“不移动”)。
(4)若容器恒容绝热,加热使容器内温度迅速升至原来的2倍,平衡将_______ (填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________ (填“大于”、“小于”或“等于”)原来的2倍。
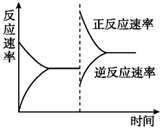
(5)若该反应在一密闭容器中发生,如图是某一时间段反应速率与反应进程的关系曲线图。
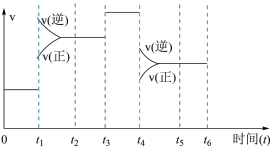
t1、t3、t4时刻体系中反应条件分别发生了什么变化?
t1:________ 。
t3:________ 。
t4:________ 。
 2NH3(g) △H=-92.4kJ•mol-1。
2NH3(g) △H=-92.4kJ•mol-1。(1)在密闭容器中,投入1molN2和3molH2在催化剂作用下发生反应,测得反应放出的热量
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将
(4)若容器恒容绝热,加热使容器内温度迅速升至原来的2倍,平衡将
(5)若该反应在一密闭容器中发生,如图是某一时间段反应速率与反应进程的关系曲线图。

t1、t3、t4时刻体系中反应条件分别发生了什么变化?
t1:
t3:
t4:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在某温度时,A+B⇌2C反应达到平衡。
(1)如果B为气态,增加体系的压强时,B的含量增加,则A为______ 态或______ 态,C为______ 态。
(2)如果升高温度,C的平衡浓度增大,则正反应方向是______ 热反应。
(3)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
H2O2(l)= H2O(l)+ 1/2O2(g) ΔH=-98.23kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为______ 。
(1)如果B为气态,增加体系的压强时,B的含量增加,则A为
(2)如果升高温度,C的平衡浓度增大,则正反应方向是
(3)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+=Cu2+(aq)+H2(g) ΔH=+64.39 kJ·mol-1
H2O2(l)= H2O(l)+ 1/2O2(g) ΔH=-98.23kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) ΔH=-285.84 kJ·mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】恒温、恒压下,在一个可变容积的容器中发生如下发应:A(g)+B(g) C(g)
C(g)
(1)若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为________ mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为________ mol。
(3)若在(2)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是__________ 。
 C(g)
C(g)(1)若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为
(3)若在(2)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ 某温度下,密闭容器中充入1 mol N2和3 mol H2,使之反应合成NH3,平衡后,测得NH3的体积分数为w,如果温度不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为w,N2、H2、NH3的物质的量分别用x、y、z表示。
(1)恒温恒容条件下:若x=0.75 mol, 则y=________ ,z=________ ;
(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是_____________ ;
Ⅱ 一定条件下,可逆反应X(g)+Y(g) 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) =0.1 mol /L;c (Z)=1.6 mol /L若用a、b、c分别表示X、Y、Z的初始浓度(mol/L)则a、b应满足的关系是
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) =0.1 mol /L;c (Z)=1.6 mol /L若用a、b、c分别表示X、Y、Z的初始浓度(mol/L)则a、b应满足的关系是____________ , a的取值范围为_______________ ;
Ⅲ 在10℃和4×105Pa的条件下,当反应aA(g) dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
(1)压强从4×105Pa增加到6×105Pa时,平衡向________ (填“正”或“逆”)方向移动,理由是____________ ;
(2)压强从10×105Pa增加到20×105Pa时,平衡向_______ (填“正”或“逆”)方向移动。
(1)恒温恒容条件下:若x=0.75 mol, 则y=
(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是
Ⅱ 一定条件下,可逆反应X(g)+Y(g)
 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) =0.1 mol /L;c (Z)=1.6 mol /L若用a、b、c分别表示X、Y、Z的初始浓度(mol/L)则a、b应满足的关系是
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) =0.1 mol /L;c (Z)=1.6 mol /L若用a、b、c分别表示X、Y、Z的初始浓度(mol/L)则a、b应满足的关系是Ⅲ 在10℃和4×105Pa的条件下,当反应aA(g)
 dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
(1)压强从4×105Pa增加到6×105Pa时,平衡向
(2)压强从10×105Pa增加到20×105Pa时,平衡向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】运用化学反应原理知识研究SO2与O2的反应对工业生产硫酸有重要意义。
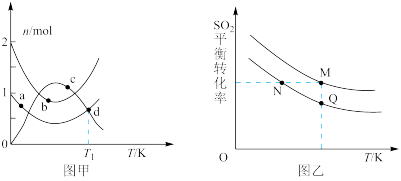
(1)向体积均为2L的恒容密闭容器中,分别加入2 mol SO2与1 mol O2,反应相同时间,不同温度下各容器中SO2、O2、SO3的物质的量如图甲所示。
①反应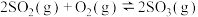 一定条件下能自发进行的原因是
一定条件下能自发进行的原因是___________ 。
②图中a、b、c三点中处于平衡状态的是___________ 点。
③T1温度时反应的平衡常数为___________ 。
(2)若在两个体积相等的容器内起始分别加入2 mol SO2和1 mol O2、1 mol SO2和0.5 mol O2,SO2的平衡转化率随温度的变化如图乙所示。
①M、Q两点容器内压强p(M)___________ 2p(Q)
②M、N两点的平衡常数K (M)___________ K(N)
③M、N、Q三点的正反应速率v(M)正、v(N)正、v(Q)正由大到小的顺序是___________ 。

(1)向体积均为2L的恒容密闭容器中,分别加入2 mol SO2与1 mol O2,反应相同时间,不同温度下各容器中SO2、O2、SO3的物质的量如图甲所示。
①反应
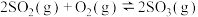 一定条件下能自发进行的原因是
一定条件下能自发进行的原因是②图中a、b、c三点中处于平衡状态的是
③T1温度时反应的平衡常数为
(2)若在两个体积相等的容器内起始分别加入2 mol SO2和1 mol O2、1 mol SO2和0.5 mol O2,SO2的平衡转化率随温度的变化如图乙所示。
①M、Q两点容器内压强p(M)
②M、N两点的平衡常数K (M)
③M、N、Q三点的正反应速率v(M)正、v(N)正、v(Q)正由大到小的顺序是
您最近一年使用:0次



