根据下列图示所得结论正确的是
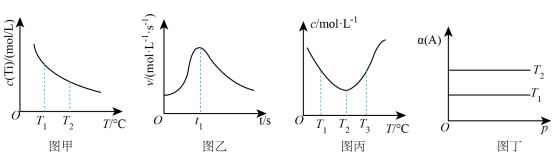

A.图甲是 中 中 的平衡浓度随温度变化的曲线,说明平衡常数 的平衡浓度随温度变化的曲线,说明平衡常数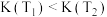 |
B.图乙是镁条与盐酸反应的化学反应速率随时间变化的曲线,说明 时刻溶液的温度最高 时刻溶液的温度最高 |
C.图丙中已知反应: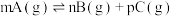 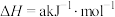 (c表示A的浓度),则可推断: (c表示A的浓度),则可推断: 、 、 均未达平衡状态 均未达平衡状态 |
D.图丁中已知反应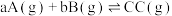 ( (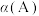 表示平衡转化率);若 表示平衡转化率);若 ,则该反应能自发进行 ,则该反应能自发进行 |
更新时间:2023-12-21 11:23:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化碳催化合成燃料甲醇过程中的主要反应为
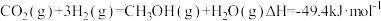


将一定比例 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、
的转化率、 的选择性
的选择性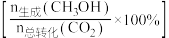 与温度的关系如图所示。下列说法
与温度的关系如图所示。下列说法不正确 的是
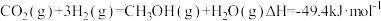


将一定比例
 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、
的转化率、 的选择性
的选择性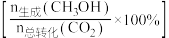 与温度的关系如图所示。下列说法
与温度的关系如图所示。下列说法
A. 的平衡选择性随温度的升高而减小 的平衡选择性随温度的升高而减小 |
B.其他条件不变,在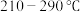 范围,随温度的升高,出口处 范围,随温度的升高,出口处 的量不断减小 的量不断减小 |
C.该条件下 催化合成 催化合成 的最佳反应温度应控制在 的最佳反应温度应控制在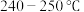 |
D.为提高 产率,需研发低温下 产率,需研发低温下 转化率高和 转化率高和 选择性高的催化剂 选择性高的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下,反应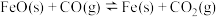 的平衡常数为0.5,在体积为2L的容器中充入
的平衡常数为0.5,在体积为2L的容器中充入
 、
、
 发生上述反应直至达到平衡,下列说法正确的是
发生上述反应直至达到平衡,下列说法正确的是
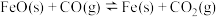 的平衡常数为0.5,在体积为2L的容器中充入
的平衡常数为0.5,在体积为2L的容器中充入
 、
、
 发生上述反应直至达到平衡,下列说法正确的是
发生上述反应直至达到平衡,下列说法正确的是A.该反应的平衡常数的表达式为: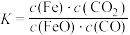 |
| B.CO的平衡转化率为80% |
C.达到平衡时再充入 和 和 各 各 ,平衡正向移动 ,平衡正向移动 |
| D.保持温度不变,将体系体积压缩,正、逆反应速率均加快而反应限度不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】吸热反应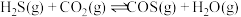 ,若在恒容绝热的容器中发生,下列情况下能判断反应一定达到平衡状态的是
,若在恒容绝热的容器中发生,下列情况下能判断反应一定达到平衡状态的是
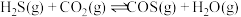 ,若在恒容绝热的容器中发生,下列情况下能判断反应一定达到平衡状态的是
,若在恒容绝热的容器中发生,下列情况下能判断反应一定达到平衡状态的是| A.容器内混合气体摩尔质量不再改变 | B.容器内的压强不再改变 |
| C.容器内各气体浓度相等时 | D.断开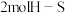 键的同时断裂 键的同时断裂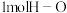 键 键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,按2:1加入反应物发生2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.恒压条件下的转化率高于恒容条件下的转化率 |
| B.平衡后各物质浓度之比为2:1:2 |
| C.恒容时按2:1再加入反应物,新平衡后SO2(g)和O2体积分数均增大 |
| D.恒容时平均分子量不变或密度不变均能证明该反应已达平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常压条件下,羰基化法精炼镍的原理为:Ni(s)+4CO(g)⇌Ni(CO)4(g) ΔH<0。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
已知:①230℃时,K=2×10-5;②将Ni(CO)4的沸点为42.2℃;③固体杂质不参与反应。
下列判断正确的是( )
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
已知:①230℃时,K=2×10-5;②将Ni(CO)4的沸点为42.2℃;③固体杂质不参与反应。
下列判断正确的是( )
| A.第一阶段,在30℃和50℃两者之间选择反应温度,选50℃ |
| B.第二阶段,由于反应有可逆性,Ni(CO)4分解率较低 |
| C.增加c(CO),平衡向正向移动,反应的平衡常数增大 |
| D.该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,
CO2(g)+H2(g) △H<0,
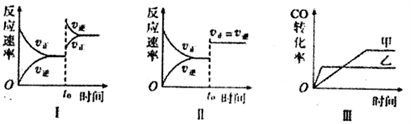
下列分析中正确的是
 CO2(g)+H2(g) △H<0,
CO2(g)+H2(g) △H<0, 
下列分析中正确的是
| A.图I研究的是t0时增大反应物浓度对反应速率的影响 |
| B.图II中t0时改变的条件只能是增大压强 |
| C.图III研究的是催化剂对化学平衡的影响,且乙使用了催化剂 |
| D.图III研究的是温度对化学平衡的影响,且乙的温度较高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】戊烷与2-甲基丁烷均可用作汽车和飞机燃料,在合适催化剂和一定压强下存在如下转化反应:CH3CH2CH2CH2CH3 (CH3)2CHCH2CH3,戊烷的平衡转化率(α)随温度变化如图示。
(CH3)2CHCH2CH3,戊烷的平衡转化率(α)随温度变化如图示。
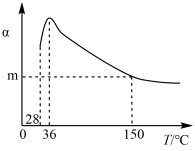
下列说法错误的是
 (CH3)2CHCH2CH3,戊烷的平衡转化率(α)随温度变化如图示。
(CH3)2CHCH2CH3,戊烷的平衡转化率(α)随温度变化如图示。| 名称 | 沸点/℃ | 燃烧热△H/kJ·mol-1 |
| 戊烷 | 36 | -3506.1 |
| 2-甲基丁烷 | 27.8 | -3504.1 |

下列说法错误的是
| A.25℃,101kPa时,根据燃烧热写出戊烷转化成2-甲基丁烷的热化学方程式为:CH3CH2CH2CH2CH3(l)=(CH3)2CHCH2CH3(l) △H=-2.0kJ·mol-1 |
| B.28~36℃时,随温度升高,2-甲基丁烷气化离开体系,平衡正向移动 |
| C.36℃~150℃时,随温度升高,戊烷转化为2-甲基丁烷的反应平衡常数增大 |
| D.150℃时,体系压强从101kPa升高到201kPa,戊烷的平衡转化率基本不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向平底烧瓶中放入氢氧化钡晶体[Ba(OH)2·8H2O]和氯化铵晶体,塞紧瓶塞。在瓶底和木板上滴少量水,如图所示。一段时间后,发现瓶内固态物质变成液体,瓶壁变冷,小木板粘在烧瓶底部。这时打开瓶塞,烧瓶中散发出刺鼻的气味。下列有关该实验的结论正确的是
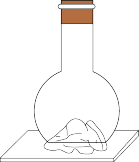

| A.自发反应一定是放热反应 | B.自发反应一定是吸热反应 |
| C.有的吸热反应也能自发进行 | D.吸热反应不能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
| A.CaCO3(s) =CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 |
| B.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
C.N2(g)+3H2(g) 2NH3(g) △H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 2NH3(g) △H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 |
| D.升高温度能使化学反应速率增大的主要原因是增加了反应物中活化分子的百分数 |
您最近一年使用:0次

 C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是
C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是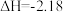 kJ
kJ ,
,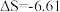 J
J

