回答下列问题。
(1)下列反应中,在高温下不能自发进行的是____________ (填字母)。
a.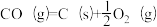
b .
c.
d.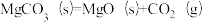
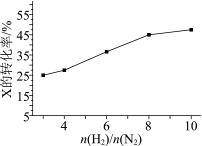
(2) △H<0。T°C时,在有催化剂的恒容密闭容器中充入N2和H2。下图为不同投料比[
△H<0。T°C时,在有催化剂的恒容密闭容器中充入N2和H2。下图为不同投料比[ ]时某反应物X的平衡转化率变化曲线。反应物X是
]时某反应物X的平衡转化率变化曲线。反应物X是_______________ (填“N2或H2”)。
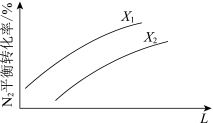
(3)在其他条件相同时,下图为分别测定不同压强、不同温度下,N2的平衡转化率。L表示_____________ ,其中X1__________ X2(填“>”或“<”)
(1)下列反应中,在高温下不能自发进行的是
a.
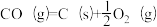
b .

c.

d.
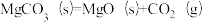
(2)
 △H<0。T°C时,在有催化剂的恒容密闭容器中充入N2和H2。下图为不同投料比[
△H<0。T°C时,在有催化剂的恒容密闭容器中充入N2和H2。下图为不同投料比[ ]时某反应物X的平衡转化率变化曲线。反应物X是
]时某反应物X的平衡转化率变化曲线。反应物X是
(3)在其他条件相同时,下图为分别测定不同压强、不同温度下,N2的平衡转化率。L表示

更新时间:2023-12-08 11:10:20
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如图所示,在容器A中装有20℃的水50mL,容器B中装有1mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2 ⇌ N2O4 △H=-57kJ/mol,当向A中加入50gNH4NO3晶体使之溶解;向B中加入2g苛性钠时:
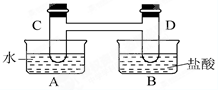
(1)C中的气体颜色______ ; (填“变浅” 或“变深”).
(2)若25℃时,起始时仅有NO2气体,达到平衡时,c(NO2)=0.0125mol/L,c(N2O4)=0.0321mol/L,则NO2的起始浓度为_____________ ,NO2的转化率为________ .

(1)C中的气体颜色
(2)若25℃时,起始时仅有NO2气体,达到平衡时,c(NO2)=0.0125mol/L,c(N2O4)=0.0321mol/L,则NO2的起始浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】温度对化学平衡移动的影响规律
(1)温度对化学平衡的影响是通过改变平衡常数实现的,升高温度,吸热反应的平衡常数___________ ,平衡向___________ 的方向移动。降低温度,放热反应的平衡常数___________ ,平衡向___________ 的方向移动。
(2)温度对化学平衡的影响是通过改变平衡常数实现的,升高温度,放热反应的平衡常数___________ ,平衡向___________ 的方向移动。降低温度,吸热反应的平衡常数___________ ,平衡向___________ 的方向移动。
(1)温度对化学平衡的影响是通过改变平衡常数实现的,升高温度,吸热反应的平衡常数
(2)温度对化学平衡的影响是通过改变平衡常数实现的,升高温度,放热反应的平衡常数
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】工业烟气中的 对环境和人体健康有极大的危害,若能合理的利用吸收,可以减少污染。请完成下列问题:
对环境和人体健康有极大的危害,若能合理的利用吸收,可以减少污染。请完成下列问题:
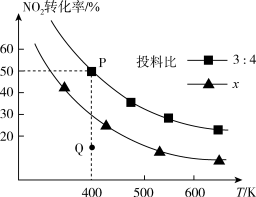
(1) 催化还原氮氧化物是目前应用广泛的烟气脱硝技术,发生的化学反应为:
催化还原氮氧化物是目前应用广泛的烟气脱硝技术,发生的化学反应为:

 ,向容积为
,向容积为 的恒容密闭容器中充入
的恒容密闭容器中充入 和
和 的混合气体
的混合气体 充分反应。不同投料比时,
充分反应。不同投料比时, 的平衡转化率与温度的关系如图中曲线所示[投料比
的平衡转化率与温度的关系如图中曲线所示[投料比 ]。
]。
①
___________ 0(填“>”“<”或“=”);
②x填___________  (填“>”“<”或“=”);
(填“>”“<”或“=”);
③投料比为 时,Q点
时,Q点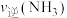
___________ (填“>”“<”或“=”)P点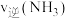 ;
;
④在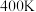 时,反应的平衡常数计算式为
时,反应的平衡常数计算式为___________ 。
(2)科学家正在研究利用催化技术将 和
和 和转变成
和转变成 和
和 ,其反应为:
,其反应为: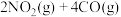
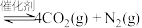
 ,反应的逆反应速率与时间的关系如图所示:
,反应的逆反应速率与时间的关系如图所示:

由图可知,反应在 、
、 、
、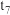 时都达到了平衡,而
时都达到了平衡,而 、
、 时都改变了一种条件,试判断改变的条件是(请列举一种可能):
时都改变了一种条件,试判断改变的条件是(请列举一种可能): 时
时___________ ; 时
时___________ ;若 时降压,
时降压, 时达到平衡,
时达到平衡,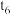 时增大反应物的浓度,在图中画出
时增大反应物的浓度,在图中画出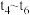 时逆反应速率与时间的关系线
时逆反应速率与时间的关系线_____ 。
 对环境和人体健康有极大的危害,若能合理的利用吸收,可以减少污染。请完成下列问题:
对环境和人体健康有极大的危害,若能合理的利用吸收,可以减少污染。请完成下列问题:
(1)
 催化还原氮氧化物是目前应用广泛的烟气脱硝技术,发生的化学反应为:
催化还原氮氧化物是目前应用广泛的烟气脱硝技术,发生的化学反应为:

 ,向容积为
,向容积为 的恒容密闭容器中充入
的恒容密闭容器中充入 和
和 的混合气体
的混合气体 充分反应。不同投料比时,
充分反应。不同投料比时, 的平衡转化率与温度的关系如图中曲线所示[投料比
的平衡转化率与温度的关系如图中曲线所示[投料比 ]。
]。①

②x填
 (填“>”“<”或“=”);
(填“>”“<”或“=”);③投料比为
 时,Q点
时,Q点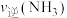
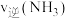 ;
;④在
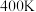 时,反应的平衡常数计算式为
时,反应的平衡常数计算式为(2)科学家正在研究利用催化技术将
 和
和 和转变成
和转变成 和
和 ,其反应为:
,其反应为: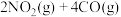
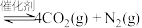
 ,反应的逆反应速率与时间的关系如图所示:
,反应的逆反应速率与时间的关系如图所示:
由图可知,反应在
 、
、 、
、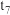 时都达到了平衡,而
时都达到了平衡,而 、
、 时都改变了一种条件,试判断改变的条件是(请列举一种可能):
时都改变了一种条件,试判断改变的条件是(请列举一种可能): 时
时 时
时 时降压,
时降压, 时达到平衡,
时达到平衡,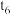 时增大反应物的浓度,在图中画出
时增大反应物的浓度,在图中画出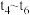 时逆反应速率与时间的关系线
时逆反应速率与时间的关系线
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】聚丙烯腈纤维俗名人造羊毛,由丙烯腈聚合而得。用丙烯合成丙烯腈的反应如下: 2C3H6(g)+2NH3(g)+3O2(g)  2C3H3N(g)+6H2O(g)+1030kJ
2C3H3N(g)+6H2O(g)+1030kJ
(1)碳在元素周期表中的位置是_______ ;C、N、O三种元素的原子半径由小到大的顺序为_______ ;
(2)某密闭容器中发生上述反应,生成丙烯腈的反应速率与反应时间的关系如下图所示。
t1时刻表示体系改变的反应条件为_______ ; t2时刻表示体系改变了另一反应条件,此时平衡_______ 移动(填“正向”、“逆向”或“不”)。
丙烯的转化率与反应温度的关系如图示:

(3)有利于提高丙烯平衡转化率的反应条件有_______ ;
(4)最大转化率所对应的温度为460℃。当温度低于460℃时,丙烯的转化率_______ (填“是”或“不是”)所对应温度下的平衡转化率,理由是_______ 。
(5)一定条件下,在2L恒容密闭容器中,通入84g C3H6、34g NH3、96g O2,若该反应5 min到达a点,则0~5min内丙烯的平均反应速率为_______ mol∙L−1∙min−1。
 2C3H3N(g)+6H2O(g)+1030kJ
2C3H3N(g)+6H2O(g)+1030kJ(1)碳在元素周期表中的位置是
(2)某密闭容器中发生上述反应,生成丙烯腈的反应速率与反应时间的关系如下图所示。

t1时刻表示体系改变的反应条件为
丙烯的转化率与反应温度的关系如图示:

(3)有利于提高丙烯平衡转化率的反应条件有
(4)最大转化率所对应的温度为460℃。当温度低于460℃时,丙烯的转化率
(5)一定条件下,在2L恒容密闭容器中,通入84g C3H6、34g NH3、96g O2,若该反应5 min到达a点,则0~5min内丙烯的平均反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】工业上合成氨工艺流程一般分三步:第一步为原料气的制备,将天然气等原料制成含氢和氮的粗原料气;第二步为净化,主要包括变换过程、脱硫脱碳过程以及气体精制过程;第三步为氨合成,将纯净的氢氮混合气压缩,增大压强,在催化剂的作用下合成氨。
(1)“一次转化”过程中 气体与水蒸气反应转化为
气体与水蒸气反应转化为 和
和 混合气体,已知几种物质的燃烧热如表所示:
混合气体,已知几种物质的燃烧热如表所示:
H2O(l)的汽化热为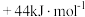 ,则“一次转化”过程中生成
,则“一次转化”过程中生成 的热化学方程式为
的热化学方程式为___________ 。
(2)“二步净化”过程中,原料 、
、 需要经过铜氨液处理净化,除去其中的
需要经过铜氨液处理净化,除去其中的 ,其反应为:
,其反应为: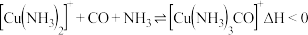 ,铜氨液吸收
,铜氨液吸收 适宜生产条件是
适宜生产条件是___________ (填字母)。
a.低温高压 b.高温高压 c.高温低压 d.低温低压
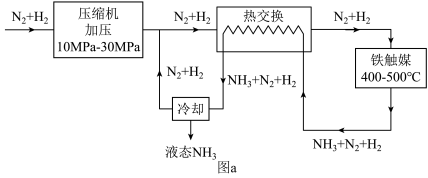
(3)第三步为氨合成,生产流程示意图如图a.已知: 。上述流程中有利于提高原料利用率的措施有
。上述流程中有利于提高原料利用率的措施有___________ 、___________ (请写出两点)。
(4)实验室研究是工业生产的基石。如图b中的实验数据是在其它条件不变时,向 密闭容器中充入
密闭容器中充入 和
和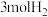 ,不同温度
,不同温度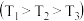 、不同压强下,达平衡时混合物中
、不同压强下,达平衡时混合物中 的物质的量分数的变化情况。
的物质的量分数的变化情况。
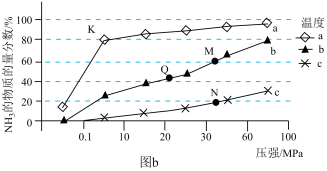
①曲线 对应的温度是
对应的温度是___________ ;
② 、
、 、
、 点平衡常数的大小关系是
点平衡常数的大小关系是___________ ; 点的平衡常数为
点的平衡常数为___________ ;
③ 点达平衡后再向容器中充入
点达平衡后再向容器中充入 和
和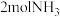 ,平衡将
,平衡将___________ (填“正向移动”、“逆向移动”或“不移动”)。
(1)“一次转化”过程中
 气体与水蒸气反应转化为
气体与水蒸气反应转化为 和
和 混合气体,已知几种物质的燃烧热如表所示:
混合气体,已知几种物质的燃烧热如表所示:| 物质 | 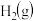 |  | 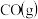 | 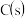 |
燃烧热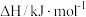 | 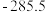 | 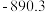 |  | 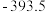 |
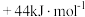 ,则“一次转化”过程中生成
,则“一次转化”过程中生成 的热化学方程式为
的热化学方程式为(2)“二步净化”过程中,原料
 、
、 需要经过铜氨液处理净化,除去其中的
需要经过铜氨液处理净化,除去其中的 ,其反应为:
,其反应为: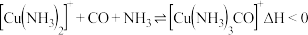 ,铜氨液吸收
,铜氨液吸收 适宜生产条件是
适宜生产条件是a.低温高压 b.高温高压 c.高温低压 d.低温低压
(3)第三步为氨合成,生产流程示意图如图a.已知:
 。上述流程中有利于提高原料利用率的措施有
。上述流程中有利于提高原料利用率的措施有
(4)实验室研究是工业生产的基石。如图b中的实验数据是在其它条件不变时,向
 密闭容器中充入
密闭容器中充入 和
和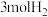 ,不同温度
,不同温度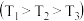 、不同压强下,达平衡时混合物中
、不同压强下,达平衡时混合物中 的物质的量分数的变化情况。
的物质的量分数的变化情况。
①曲线
 对应的温度是
对应的温度是②
 、
、 、
、 点平衡常数的大小关系是
点平衡常数的大小关系是 点的平衡常数为
点的平衡常数为③
 点达平衡后再向容器中充入
点达平衡后再向容器中充入 和
和 ,平衡将
,平衡将
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在一定温度下,体积为2 L的密闭容器中加入1.2molN2、3.2 molH2,N2和H2之间发生反应:N2(g)+3H2(g) 2NH3(g),如图所示。
2NH3(g),如图所示。
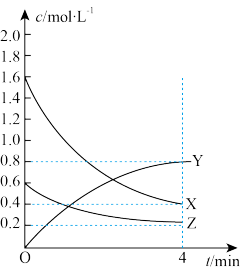
(1)曲线_________ (填“X”、“Y”或“Z”)表示NH3的物质的量浓度随时间的变化曲线。
(2)0~4min 内,以Z的浓度变化表示的平均反应速率为_______________ 。
(3)下列措施能使该反应的化学反应速率加快的是__________ (用序号回答)。
①通入H2②减小容 器体积 ③升高温度 ④通入Ar使压强增大
(4)下列叙述能说明该反应已达到化学平衡状态的是_________ (填标号)。
A.相同时间内消耗n mol的N2的同时生成3n mol的H2
B.容器内压强不再发生变化
C.容器内混合气体原子总数不变
D.2v(N2)=v(NH3)
E.H2的体积分数不再发生变化
 2NH3(g),如图所示。
2NH3(g),如图所示。
(1)曲线
(2)0~4min 内,以Z的浓度变化表示的平均反应速率为
(3)下列措施能使该反应的化学反应速率加快的是
①通入H2②减小容 器体积 ③升高温度 ④通入Ar使压强增大
(4)下列叙述能说明该反应已达到化学平衡状态的是
A.相同时间内消耗n mol的N2的同时生成3n mol的H2
B.容器内压强不再发生变化
C.容器内混合气体原子总数不变
D.2v(N2)=v(NH3)
E.H2的体积分数不再发生变化
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】已知反应Al2Br6(l) 2Al(g) +6Br(g) ΔH
2Al(g) +6Br(g) ΔH
①Al2Br6(s) Al2Br6(l) ΔH1
Al2Br6(l) ΔH1
②Al(s) Al(g) ΔH2
Al(g) ΔH2
③Br2(l) Br2(g) ΔH3
Br2(g) ΔH3
④Br2(g) 2Br(g) ΔH4
2Br(g) ΔH4
⑤2Al(s) + 3Br2(l) Al2Br6(s) ΔH5
Al2Br6(s) ΔH5
则ΔH=_______ 。
由图可知,若该反应自发,则该反应的_______ 。
 2Al(g) +6Br(g) ΔH
2Al(g) +6Br(g) ΔH①Al2Br6(s)
 Al2Br6(l) ΔH1
Al2Br6(l) ΔH1②Al(s)
 Al(g) ΔH2
Al(g) ΔH2③Br2(l)
 Br2(g) ΔH3
Br2(g) ΔH3④Br2(g)
 2Br(g) ΔH4
2Br(g) ΔH4⑤2Al(s) + 3Br2(l)
 Al2Br6(s) ΔH5
Al2Br6(s) ΔH5则ΔH=
由图可知,若该反应自发,则该反应的

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】合成氨反应的特点
合成氨反应:N2(g)+3H2(g)⇌2NH3(g)。已知298K时:ΔH=-92.4kJ·mol-1,ΔS=-198.2J·mol-1·K-1。
(1)自发性:常温(298K)下,___________ ,能自发进行。
(2)可逆性:反应为___________ 反应。
(3)体积变化(熵变):ΔS<0,正反应是气体体积___________ 的反应。
(4)焓变:ΔH<0,是___________ 反应。
合成氨反应:N2(g)+3H2(g)⇌2NH3(g)。已知298K时:ΔH=-92.4kJ·mol-1,ΔS=-198.2J·mol-1·K-1。
(1)自发性:常温(298K)下,
(2)可逆性:反应为
(3)体积变化(熵变):ΔS<0,正反应是气体体积
(4)焓变:ΔH<0,是
您最近一年使用:0次

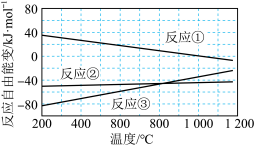
 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为: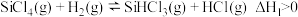
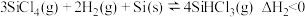
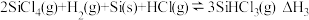
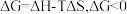 时反应自发进行。三个氢化反应的
时反应自发进行。三个氢化反应的 与温度的关系如图所示,可知:反应①能自发进行的最低温度是
与温度的关系如图所示,可知:反应①能自发进行的最低温度是