常温下,关于pH=11的氨水溶液,下列说法不正确的是
A.溶液中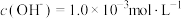 |
B.加水稀释100倍后,溶液的 |
C.与等体积pH=3的 溶液充分混合后,溶液呈碱性 溶液充分混合后,溶液呈碱性 |
D.此溶液中由水电离出的 和 和 浓度均为 浓度均为 |
更新时间:2023-12-12 14:50:16
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】25℃,将浓度均为0.1mol/L的HA溶液Va mL和BOH溶液Vb mL混合,保持Va+Vb=100mL,生成物BA易溶于水。Va、Vb与混合液pH的关系如下图。下列叙述错误的是


| A.HA一定是弱酸 |
| B.BOH可能是强碱 |
| C.z点时,水的电离被促进 |
| D.x、y、z点时,溶液中都存在c(A-)+c(OH-)=c(B+)+c(H+) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】已知室温时,0.1 mol·L-1的某一元酸HA的pH=4,下列叙述错误的是
| A.HA在水溶液中部分电离 | B.加水时,HA的电离程度增大 |
| C.升高温度,溶液的pH增大 | D.此溶液中由水电离出的c(H+)约为1.0×10-10 mol·L-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】常温下,若1体积 溶液与2体积
溶液与2体积 的
的 溶液混合所得溶液的
溶液混合所得溶液的 (溶液体积变化不计),则
(溶液体积变化不计),则 与
与 物质的量浓度之比应为
物质的量浓度之比应为
 溶液与2体积
溶液与2体积 的
的 溶液混合所得溶液的
溶液混合所得溶液的 (溶液体积变化不计),则
(溶液体积变化不计),则 与
与 物质的量浓度之比应为
物质的量浓度之比应为A. | B. | C.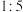 | D.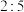 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】七彩神仙鱼在pH为6.2~6.8的环境中能迅速生长,pH≤6则难以存活。常温下,若1000L某湖水含有0.5molH2SO4。下列说法正确的是
| A.当前湖水的环境适宜七彩神仙鱼生长 |
B.当前湖水中,水电离的 |
| C.若将该湖水稀释103倍,湖水环境不利于七彩神仙鱼生长 |
| D.若将该湖水稀释107倍,湖水pH变为10 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】下列说法不正确的是
A. 的硫酸中 的硫酸中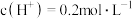 |
B.将 溶液从常温加热至80℃,溶液的 溶液从常温加热至80℃,溶液的 变小但仍保持中性 变小但仍保持中性 |
C.常温下, 溶液呈碱性,说明 溶液呈碱性,说明 是弱电解质 是弱电解质 |
D.常温下, 为3的醋酸溶液中加入醋酸钠固体,溶液 为3的醋酸溶液中加入醋酸钠固体,溶液 增大 增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】现有常温下四种溶液,有关叙述正确的是
| 序号 | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 硫酸 |
| A.③④中分别加入适量的醋酸钠晶体后,③pH增大,④pH不变 |
| B.分别取③、④溶液等体积加入足量的锌粒,产生氢气的量③>④ |
C.将等体积的①②混合,则 的电离平衡向逆向移动 的电离平衡向逆向移动 |
D.取等体积①与④混合,则混合后溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列叙述正确的是
| A.25℃时,将pH=4的盐酸稀释1000倍后,溶液的pH=7 |
| B.常温下,某溶液中由水电离的c(OH-) = 10-13mol/L,则此溶液一定呈酸性 |
| C.某醋酸溶液的pH=a,将此溶液稀释100倍后,溶液的pH=b,则a > b-2 |
| D.25℃时,pH=13强碱溶液与pH=2的强酸溶液混合,若所得混合液的pH=7,则强碱与强酸的体积比是10:1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】醋酸的下列性质中,可以证明它是弱电解质的是( )
①1 mol/L的醋酸溶液中c(H+)=0.01 mol/L②醋酸以任意比与水互溶③10 mL 1mol/L的醋酸溶液恰好与10 mL 1 mol/L的NaOH溶液完全反应④在相同条件下,醋酸溶液的导电性比盐酸弱
①1 mol/L的醋酸溶液中c(H+)=0.01 mol/L②醋酸以任意比与水互溶③10 mL 1mol/L的醋酸溶液恰好与10 mL 1 mol/L的NaOH溶液完全反应④在相同条件下,醋酸溶液的导电性比盐酸弱
| A.④ | B.①③④ | C.①④ | D.②④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列性质中可以证明醋酸是弱电解质的是
| A.醋酸与水以任意比例互溶 |
| B.10 mL 1 mol·L-1 醋酸恰好与 10 mL 1 mol·L-1NaOH 溶液完全反应 |
| C.醋酸的导电性比盐酸的弱 |
| D.1 mol·L -1 的醋酸溶液的 c(H+)约为 0.01 mol·L-1 |
您最近一年使用:0次

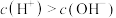 的操作是。
的操作是。
 的NaOH溶液中,滴加10VmL
的NaOH溶液中,滴加10VmL  的稀硫酸,所得溶液中
的稀硫酸,所得溶液中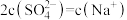 ,则
,则 的值是
的值是

