短周期元素X、Y、Z原子序数依次增大,其中Y元素的一种同位素可用于文物年代的断定,且其最外层电子数等于X、Z最外层电子总和的一半。Y、Z可形成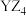 型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:
型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:

注:△、□、○分别表示X、Y、Z形成的化合物。回答下列问题:
(1) 与水反应生成氢气的化学方程式为
与水反应生成氢气的化学方程式为_______ ;
(2)X在空气中燃烧可获得4,而与X相邻的同主族金属元素Q在空气中燃烧可获得_______ (填化学式),由此可以判断,X、Q金属性较强的是_______ (填元素符号);
(3)向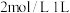 的NaOH溶液中通入a mol
的NaOH溶液中通入a mol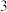 可获得含溶质
可获得含溶质 的溶液,若
的溶液,若 是两种盐的混合物,则a的取值范围是
是两种盐的混合物,则a的取值范围是_______ mol,不使用其它试剂,可将固体 转化为纯净物的化学反应为
转化为纯净物的化学反应为_______ (写化学方程式);
(4)用合适的方程式证明 的酸性强于⑥
的酸性强于⑥_______ ,依据该事实_______ (填“能”或“不能”)判断出Y、Z的非金属性强弱,理由是_______ 。
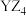 型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:
型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:
注:△、□、○分别表示X、Y、Z形成的化合物。回答下列问题:
(1)
 与水反应生成氢气的化学方程式为
与水反应生成氢气的化学方程式为(2)X在空气中燃烧可获得4,而与X相邻的同主族金属元素Q在空气中燃烧可获得
(3)向
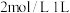 的NaOH溶液中通入a mol
的NaOH溶液中通入a mol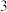 可获得含溶质
可获得含溶质 的溶液,若
的溶液,若 是两种盐的混合物,则a的取值范围是
是两种盐的混合物,则a的取值范围是 转化为纯净物的化学反应为
转化为纯净物的化学反应为(4)用合适的方程式证明
 的酸性强于⑥
的酸性强于⑥
更新时间:2023-12-14 10:40:27
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】由短周期元素组成的中学常见的含钠元素的物质A、B、C、D,存在如图转化关系(部分生成物和反应条件已略去)。

(1)若A为金属钠,A与水反应的离子方程式为_______________ 。
(2)若A为淡黄色的固体化合物,A________ (填“是”或“不是”)碱性氧化物,A与CO2反应的化学方程式为_________________ 。
(3)A不论是Na还是淡黄色的固体化合物,依据转化关系判断物质C是________ ,物质D是________ 。

(1)若A为金属钠,A与水反应的离子方程式为
(2)若A为淡黄色的固体化合物,A
(3)A不论是Na还是淡黄色的固体化合物,依据转化关系判断物质C是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F、G为六种短周期元素,且原子序数依次增大。A与B、C、D均能形成10电子化合物,C的气态氢化物能使紫色石蕊溶液变蓝,A、D能形成两种液态化合物A2D和A2D2,F元素的周期序数与主族序数相等,A、G和C、E的原子序数之和相等。
(1)D与E组成的某种化合物呈淡黄色,写出其电子式____ ,所含的化学键类型为____ 。
(2)比较B和C的简单气态氢化物的沸点大小____ 。(用化学式表示)
(3)在一定条件下,E元素的单质能与A元素的单质化合生成EA,EA能与水反应放氢气,则其化学方程式为____ 。
(4)CD2是常见的大气污染物,工业生产中可用C的气态氢化物通过催化还原消除其污染,写出相关化学方程式____ 。
(1)D与E组成的某种化合物呈淡黄色,写出其电子式
(2)比较B和C的简单气态氢化物的沸点大小
(3)在一定条件下,E元素的单质能与A元素的单质化合生成EA,EA能与水反应放氢气,则其化学方程式为
(4)CD2是常见的大气污染物,工业生产中可用C的气态氢化物通过催化还原消除其污染,写出相关化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某学习小组用下图所示的装置(C中盛放的是过氧化钠)进行实验,证明过氧化钠可在呼吸面具和潜水艇中做供氧剂。
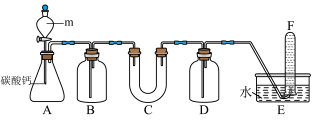
(1) 是实验室中制取CO2的装置,其中仪器
是实验室中制取CO2的装置,其中仪器 的名称是
的名称是______ ;
(2)B中盛装的试剂是______ 溶液,其作用是______ ;
(3)写出 中发生反应的化学方程式
中发生反应的化学方程式______ 、______ ;
(4)D中盛装的试剂为______ ;
(5)能证明“过氧化钠可在呼吸面具和潜水艇中做供氧剂”的实验现象有______ 。
A.C装置中的淡黄色固体变为白色
B.D装置中无明显现象
C.F中收集到无色气体,该气体可以使带火星的木条复燃

(1)
 是实验室中制取CO2的装置,其中仪器
是实验室中制取CO2的装置,其中仪器 的名称是
的名称是(2)B中盛装的试剂是
(3)写出
 中发生反应的化学方程式
中发生反应的化学方程式(4)D中盛装的试剂为
(5)能证明“过氧化钠可在呼吸面具和潜水艇中做供氧剂”的实验现象有
A.C装置中的淡黄色固体变为白色
B.D装置中无明显现象
C.F中收集到无色气体,该气体可以使带火星的木条复燃
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E五种物质的焰色反应都呈黄色,A、B与水反应都有气体放出,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,同时都生成C的溶液,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能生成D。
(1)写出下列物质的化学式:B____________ ,E_____________ 。
(2)写出A→C的化学方程式,并标出电子转移的方向和数目:_______________
(3)写出C→D的离子方程式:________________________________ 。
(4)写出E→D的化学方程式:________________________________ 。
(1)写出下列物质的化学式:B
(2)写出A→C的化学方程式,并标出电子转移的方向和数目:
(3)写出C→D的离子方程式:
(4)写出E→D的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某实验小组拟验证CO2与Na2O2反应的产物,现设计以下实验装置进行实验:
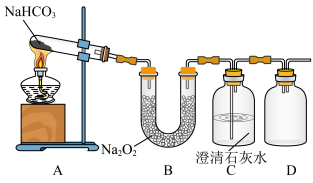
(1)写出装置A中反应的化学方程式_____________________________________ 。
(2)写出装置B中反应的化学方程式_____________________________________ 。
(3)C装置的作用是______________________ 。
(4)拟用装置D收集气体产物,请将装置补充完整________________ 。
(5)检验气体产物的方法_______________________________________ 。
(6)检验固体产物的方法:从B装置中取少量固体,溶于水配成溶液,____________ 。
(7)有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么________ 。

(1)写出装置A中反应的化学方程式
(2)写出装置B中反应的化学方程式
(3)C装置的作用是
(4)拟用装置D收集气体产物,请将装置补充完整
(5)检验气体产物的方法
(6)检验固体产物的方法:从B装置中取少量固体,溶于水配成溶液,
(7)有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】如图中每一个方格表示有关的一种反应物或生成物,其中A、C为无色气体。
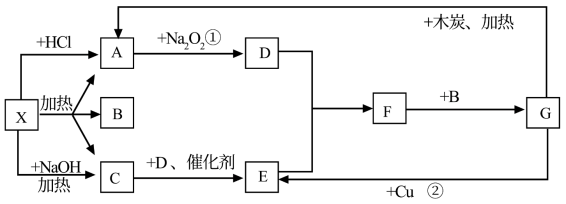
(1)写出有关物质的化学式X:___ ;F__ 。
(2)写出A→D的化学方程式___ 。
(3)写出实验室制备C的化学方程式___ 。
(4)分别取两份50mLNaOH溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入0.1mol/L的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl的体积之间的关系如图所示,试分析:
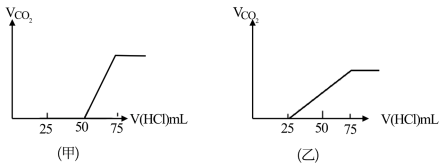
①NaOH在吸收A气体后,乙图所示溶液中存在的溶质是:___ ,其物质的量之比是:__ 。
②原NaOH溶液的物质的量浓度是___ mol/L。

(1)写出有关物质的化学式X:
(2)写出A→D的化学方程式
(3)写出实验室制备C的化学方程式
(4)分别取两份50mLNaOH溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入0.1mol/L的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl的体积之间的关系如图所示,试分析:

①NaOH在吸收A气体后,乙图所示溶液中存在的溶质是:
②原NaOH溶液的物质的量浓度是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】元素化合物知识不是散乱的,含有相同元素的物质在一定条件下是有规律转化的。某金属单质A及其化合物间的转化关系如图(某些产物和反应条件已略去),其中C为淡黄色的固体,D是一种无色无味的气体,能使澄清石灰水变浑浊,常温下E为液体,完成下列问题:
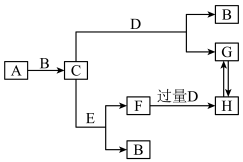
请回答:
(1)C的化学式为___ ,写出C的任意一种用途___ 。
(2)写出C与D反应的化学方程式:___ 。
(3)向G的饱和溶液中通入过量D的离子方程式为___ 。
(4)若用如图所示装置验证G和H的热稳定性,则试管乙中装入的固体最好是___ (填化学式)。

(5)加热5.00gG和H的固体混合物,使H完全分解,固体混合物的质量减少了1.24g,则原混合物中G的质量为___ 。

请回答:
(1)C的化学式为
(2)写出C与D反应的化学方程式:
(3)向G的饱和溶液中通入过量D的离子方程式为
(4)若用如图所示装置验证G和H的热稳定性,则试管乙中装入的固体最好是

(5)加热5.00gG和H的固体混合物,使H完全分解,固体混合物的质量减少了1.24g,则原混合物中G的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下图中的每一个方格表示有关的一种反应物或生成物,其中A、C为无色气体
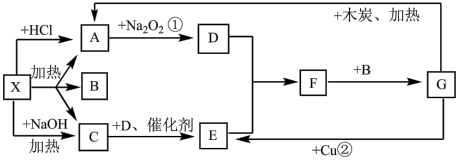
(1)写出有关物质的化学式X:_________ ;F_________ 。
(2)写出F→G的化学方程式_________ 。
(3)写出实验室制备C的化学方程式_________ 。
(4)分别取两份
 溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入
溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入 的
的 溶液,产生的A气体体积(标准状况下)与所加入的
溶液,产生的A气体体积(标准状况下)与所加入的 的体积之间的关系如图所示,试分析:
的体积之间的关系如图所示,试分析:
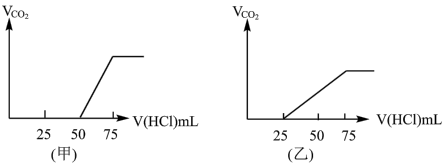
① 在吸收A气体后,乙图所示溶液中存在的溶质是:
在吸收A气体后,乙图所示溶液中存在的溶质是:_________ ,其物质的量之比是:_________ 。
②原 溶液的物质的量浓度是
溶液的物质的量浓度是_______  ,甲图所示溶液最多还能吸收A体积为
,甲图所示溶液最多还能吸收A体积为_______ mL(标准状况)

(1)写出有关物质的化学式X:
(2)写出F→G的化学方程式
(3)写出实验室制备C的化学方程式
(4)分别取两份

 溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入
溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入 的
的 溶液,产生的A气体体积(标准状况下)与所加入的
溶液,产生的A气体体积(标准状况下)与所加入的 的体积之间的关系如图所示,试分析:
的体积之间的关系如图所示,试分析:
①
 在吸收A气体后,乙图所示溶液中存在的溶质是:
在吸收A气体后,乙图所示溶液中存在的溶质是:②原
 溶液的物质的量浓度是
溶液的物质的量浓度是 ,甲图所示溶液最多还能吸收A体积为
,甲图所示溶液最多还能吸收A体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】I.如表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语 回答下列问题:
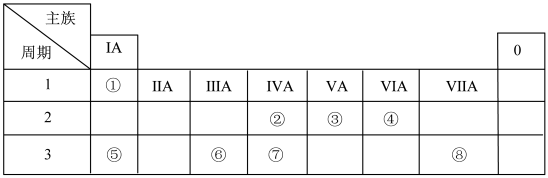
(1)②的最简单气态氢化物分子的电子式:______ 。
(2)③的气态氢化物稳定性比④的气态氢化物______ 。(填“强”、“弱”或“相同”)
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______ 。(填化学式)
(4)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:_______ 。
(5)⑦的原子结构示意图为_______ 。
(6)⑥的最高价氧化物与⑤的最高价氧化物对应水化物溶液反应的离子 方程式为______ 。
(7)用电子式表示HCl分子的形成过程:______ 。
II.如表为元素周期表的一部分,根据下面的要求回答问题:
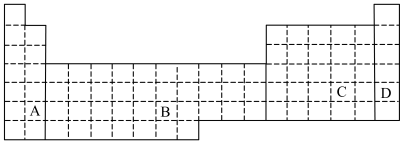
(8)在上面元素周期表中A、B、C、D四个区域中全部是金属元素的区域为______ 。
(9)现有Al、甲和乙三种同周期短周期金属元素,甲元素原子核外M电子层比K电子层上的电子数少1。
①写出Al元素在周期表中的位置______ 。
②为了比较三种金属单质的活泼性,下列实验操作描述不正确的是______ (填序号)。
a.将绿豆粒大小的甲和未用砂纸打磨的乙单质分别放入冷水中,并都滴入2滴酚酞溶液
b.将铝和乙这两种元素的块状单质先用砂纸磨去表面氧化膜后分别和同浓度的盐酸反应
c.将Al和乙这两种元素的块状单质先用砂纸磨去表面氧化膜,再分别和等量氢氧化钠作用
d.比较这三种金属元素形成的氢氧化物的碱性

(1)②的最简单气态氢化物分子的电子式:
(2)③的气态氢化物稳定性比④的气态氢化物
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(4)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:
(5)⑦的原子结构示意图为
(6)⑥的最高价氧化物与⑤的最高价氧化物对应水化物溶液反应的
(7)用电子式表示HCl分子的形成过程:
II.如表为元素周期表的一部分,根据下面的要求回答问题:

(8)在上面元素周期表中A、B、C、D四个区域中全部是金属元素的区域为
(9)现有Al、甲和乙三种同周期短周期金属元素,甲元素原子核外M电子层比K电子层上的电子数少1。
①写出Al元素在周期表中的位置
②为了比较三种金属单质的活泼性,下列实验操作描述不正确的是
a.将绿豆粒大小的甲和未用砂纸打磨的乙单质分别放入冷水中,并都滴入2滴酚酞溶液
b.将铝和乙这两种元素的块状单质先用砂纸磨去表面氧化膜后分别和同浓度的盐酸反应
c.将Al和乙这两种元素的块状单质先用砂纸磨去表面氧化膜,再分别和等量氢氧化钠作用
d.比较这三种金属元素形成的氢氧化物的碱性
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】工业上可用微生物处理含KCN的废水。第一步是微生物在氧气充足的条件下,将KCN转化成KHCO3和NH3(最佳pH:6.7~7.2);第二步是把氨转化为硝酸:NH3+2O2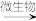 HNO3+H2O。请完成下列填空:
HNO3+H2O。请完成下列填空:
(1)写出第一步反应的化学反应方程式____ ,第二步反应的还原产物是_____ (填写化学式)。
(2)在KCN中,属于短周期且原子半径最大的元素是_____ ,氮原子最外层电子的运动状态有_____ 种。NH3的电子式是______ 。
(3)可以比较碳和氮元素非金属性强弱的化学反应方程式为_____ 。
(4)室温下,0.1mol/L K2CO3、KCN、KHCO3溶液均呈碱性且pH依次减小,在含等物质的量的KCN、KHCO3混合溶液中,阴离子(除OH-)浓度由大到小的顺序是_____ 。
(5)工业上还常用氯氧化法处理含KCN的废水:KCN+2KOH+Cl2=KOCN+2KCl+H2O,2KOCN+4KOH+3Cl2=N2+6KCl+2CO2+2H2O。两者相比,微生物处理法的优点与缺点是(各写一条)。优点:_____ ,缺点:______ 。
 HNO3+H2O。请完成下列填空:
HNO3+H2O。请完成下列填空:(1)写出第一步反应的化学反应方程式
(2)在KCN中,属于短周期且原子半径最大的元素是
(3)可以比较碳和氮元素非金属性强弱的化学反应方程式为
(4)室温下,0.1mol/L K2CO3、KCN、KHCO3溶液均呈碱性且pH依次减小,在含等物质的量的KCN、KHCO3混合溶液中,阴离子(除OH-)浓度由大到小的顺序是
(5)工业上还常用氯氧化法处理含KCN的废水:KCN+2KOH+Cl2=KOCN+2KCl+H2O,2KOCN+4KOH+3Cl2=N2+6KCl+2CO2+2H2O。两者相比,微生物处理法的优点与缺点是(各写一条)。优点:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】利用下列装置可进行物质或元素性质的探究实验。
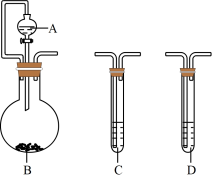
Ⅰ.验证氯、碳、硅元素的非金属性强弱
(1)已知圆底烧瓶B中装有 固体,试管C中装有
固体,试管C中装有 溶液,装置连接顺序为A→B→C,则A中所装试剂的化学式是
溶液,装置连接顺序为A→B→C,则A中所装试剂的化学式是______ 。
(2)仪器A的名称是______ 。
(3)C装置中发生反应的离子方程式是______ 。
(4)通过以上实验说明氯、碳、硅的非金属性依次减弱,其判断的理论依据是______ 。
Ⅱ.通过置换反应验证氯、硫的非金属性强弱,设计装置连接顺序为A→B→C→D。
(5)C试管中盛装的溶液不能选择______ (填正确答案标号)。
a.硫化钠溶液 b.亚硫酸钠溶液 c.氢硫酸
(6)圆底烧瓶B中产生气体(无需加热装置)的化学方程式为__________________ 。
(7)证明氯的非金属性比硫强的实验现象是__________________ 。
(8)D装置是盛有氢氧化钠溶液,该装置的作用是__________________ 。

Ⅰ.验证氯、碳、硅元素的非金属性强弱
(1)已知圆底烧瓶B中装有
 固体,试管C中装有
固体,试管C中装有 溶液,装置连接顺序为A→B→C,则A中所装试剂的化学式是
溶液,装置连接顺序为A→B→C,则A中所装试剂的化学式是(2)仪器A的名称是
(3)C装置中发生反应的离子方程式是
(4)通过以上实验说明氯、碳、硅的非金属性依次减弱,其判断的理论依据是
Ⅱ.通过置换反应验证氯、硫的非金属性强弱,设计装置连接顺序为A→B→C→D。
(5)C试管中盛装的溶液不能选择
a.硫化钠溶液 b.亚硫酸钠溶液 c.氢硫酸
(6)圆底烧瓶B中产生气体(无需加热装置)的化学方程式为
(7)证明氯的非金属性比硫强的实验现象是
(8)D装置是盛有氢氧化钠溶液,该装置的作用是
您最近一年使用:0次

 离子方程式:
离子方程式: 化学方程式:
化学方程式:

