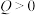在一容积可变的密闭容器中加入一定量的 ,发生如下反应:
,发生如下反应:
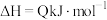 。反应达到平衡时,
。反应达到平衡时, 的物质的量浓度与温度
的物质的量浓度与温度 、容器体积
、容器体积 的关系如表所示,下列说法正确的是
的关系如表所示,下列说法正确的是
 ,发生如下反应:
,发生如下反应:
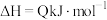 。反应达到平衡时,
。反应达到平衡时, 的物质的量浓度与温度
的物质的量浓度与温度 、容器体积
、容器体积 的关系如表所示,下列说法正确的是
的关系如表所示,下列说法正确的是V/L T/℃ | 1 | 2 | 4 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
A.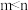 |
B.温度不变,压强增大(缩小容器体积), 的质量分数增大 的质量分数增大 |
C.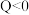 |
| D.体积不变,温度升高,平衡向逆反应方向移动 |
更新时间:2023-12-15 15:48:42
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】利用CO2—CH4超干法重整制合成气(CO+H2),主要反应如下。
反应Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g);ΔH1=+247 kJ·mol-1。
反应Ⅱ: CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g);ΔH2=+330 kJ·mol-1。
反应Ⅲ: CO(g)+H2O(g)⇌CO2(g)+H2(g);ΔH3=-41 kJ·mol-1。
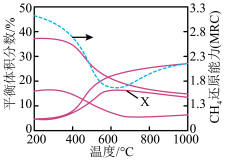
恒压条件下,n始(CO2)∶n始(CH4)=3.3时, 若仅考虑上述反应,平衡时CO2、CH4、CO、H2的体积分数和CH4的还原能力随温度的变化如图所示。已知:工业上将干重整反应中CH4的还原能力(MRC)定义为一个CH4分子消耗的CO2分子的数量。数量越大,还原能力越强。下列说法正确的是
反应Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g);ΔH1=+247 kJ·mol-1。
反应Ⅱ: CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g);ΔH2=+330 kJ·mol-1。
反应Ⅲ: CO(g)+H2O(g)⇌CO2(g)+H2(g);ΔH3=-41 kJ·mol-1。
恒压条件下,n始(CO2)∶n始(CH4)=3.3时, 若仅考虑上述反应,平衡时CO2、CH4、CO、H2的体积分数和CH4的还原能力随温度的变化如图所示。已知:工业上将干重整反应中CH4的还原能力(MRC)定义为一个CH4分子消耗的CO2分子的数量。数量越大,还原能力越强。下列说法正确的是

A.反应Ⅱ的平衡常数为K=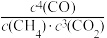 |
| B.图中曲线X表示平衡时H2的体积分数随温度的变化 |
| C.温度在600~1 000 ℃间,升高温度对反应Ⅰ的影响程度大于反应Ⅱ |
| D.其他条件不变,增大压强或选择合适的催化剂均能提高CO的平衡产率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】在保持体系总压为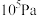 的条件下进行反应
的条件下进行反应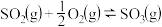 ,原料气中
,原料气中 和
和 的物质的量之比
的物质的量之比 不同时,
不同时, 的平衡转化率与温度(T)的关系如图所示。图中A点原料气的成分是
的平衡转化率与温度(T)的关系如图所示。图中A点原料气的成分是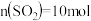 ,
,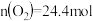 ,
,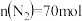 ,下列有关说法正确的是(已知:用分压表示的平衡常数为
,下列有关说法正确的是(已知:用分压表示的平衡常数为 ,分压=总压×物质的量分数)
,分压=总压×物质的量分数)

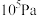 的条件下进行反应
的条件下进行反应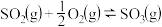 ,原料气中
,原料气中 和
和 的物质的量之比
的物质的量之比 不同时,
不同时, 的平衡转化率与温度(T)的关系如图所示。图中A点原料气的成分是
的平衡转化率与温度(T)的关系如图所示。图中A点原料气的成分是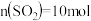 ,
,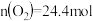 ,
,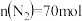 ,下列有关说法正确的是(已知:用分压表示的平衡常数为
,下列有关说法正确的是(已知:用分压表示的平衡常数为 ,分压=总压×物质的量分数)
,分压=总压×物质的量分数)
| A.该反应是吸热反应 |
B.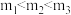 |
C.A点时 分压 分压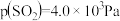 |
D.在500℃、 的条件下,该反应的平衡常数 的条件下,该反应的平衡常数 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
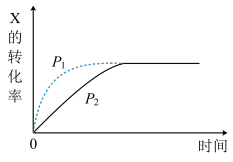
【推荐1】图中曲线分别表示相同温度下,压强为P1、P2条件下发生可逆反应:mX(g)+nY(g) 2Z(g)+W(s)的过程。下列说法不正确的是( )
2Z(g)+W(s)的过程。下列说法不正确的是( )
 2Z(g)+W(s)的过程。下列说法不正确的是( )
2Z(g)+W(s)的过程。下列说法不正确的是( )
| A.P1>P2 | B.m+n=2 |
| C.m+n=3 | D.P1、P2下平衡常数相同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用传感技术可探究压强对反应 化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入适量
化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入适量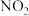 气体,当活塞位置不变时。分别在t1、t2s时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
气体,当活塞位置不变时。分别在t1、t2s时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
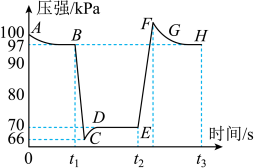
压强随时间变化的曲线
 化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入适量
化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入适量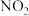 气体,当活塞位置不变时。分别在t1、t2s时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
气体,当活塞位置不变时。分别在t1、t2s时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
压强随时间变化的曲线
| A.由B点到D点观察到注射器内气体颜色先变浅后逐渐变深 |
| B.E点的操作是压缩注射器 |
| C.B、H两点对应的正反应速率相等 |
D.该反应的 ,反应能自发进行的原因是 ,反应能自发进行的原因是 |
您最近半年使用:0次


 pC(g) ΔH(m、n、p化学计量系数,A、B、C是物质) ,各物理量关系都符合下列两个图像,其中图1中T1、T2代表不同的温度,α(A)表示物质A的转化率,则
pC(g) ΔH(m、n、p化学计量系数,A、B、C是物质) ,各物理量关系都符合下列两个图像,其中图1中T1、T2代表不同的温度,α(A)表示物质A的转化率,则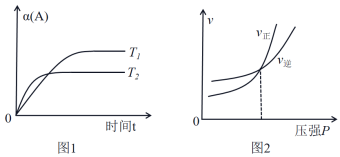

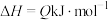 ,反应过程中,当其他条件不变时,物质C的质量(m)与温度(T),反应速率(v)与压强(p)的关系如图所示。据图分析,以下说法正确的是
,反应过程中,当其他条件不变时,物质C的质量(m)与温度(T),反应速率(v)与压强(p)的关系如图所示。据图分析,以下说法正确的是
 ,
,