某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及氧化物 、
、 ,还有少量其他不溶于酸溶液和碱溶液的物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体
,还有少量其他不溶于酸溶液和碱溶液的物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体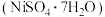 :
:
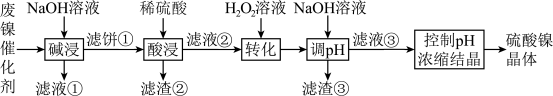
室温下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”时需要充分搅拌,其目的是________ 。
(2)“碱浸”中NaOH的作用除去除催化剂表面的油脂外,还与催化剂中Al和 反应生成
反应生成________ (填物质的化学式),使Al元素进入“滤液①”。
(3)“滤液②”中主要含有金属离子“ ”和“
”和“ ”,则“转化”中加入
”,则“转化”中加入 的主要作用是
的主要作用是________ (用离子方程式表示)。
(4)写出 的溶度积常数的表达式
的溶度积常数的表达式
________ ,利用上述表格数据,计算 的溶度积常数
的溶度积常数
________ (列出计算式即可,不用化简)。如果“转化”后的溶液中 浓度为
浓度为 ,则“调pH”应控制pH不超过
,则“调pH”应控制pH不超过________ (填数值)。
 、
、 ,还有少量其他不溶于酸溶液和碱溶液的物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体
,还有少量其他不溶于酸溶液和碱溶液的物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体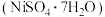 :
:
室温下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 |
|
|
|
|
开始沉淀时 | 7 | 4 | 2 | 8 |
沉淀完全时 | 9 | 5 | 3 | 9 |
(1)“碱浸”时需要充分搅拌,其目的是
(2)“碱浸”中NaOH的作用除去除催化剂表面的油脂外,还与催化剂中Al和
 反应生成
反应生成(3)“滤液②”中主要含有金属离子“
 ”和“
”和“ ”,则“转化”中加入
”,则“转化”中加入 的主要作用是
的主要作用是(4)写出
 的溶度积常数的表达式
的溶度积常数的表达式
 的溶度积常数
的溶度积常数
 浓度为
浓度为 ,则“调pH”应控制pH不超过
,则“调pH”应控制pH不超过
更新时间:2023-12-17 21:17:27
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】我国科学家研制的第二代“彩虹鱼”万米级深海着陆器所用的金属材料主要是钛合金。以钛铁矿(成分:FeTiO3及少量Fe2O3、FeO等杂质)为主要原料制钛的流程如下:
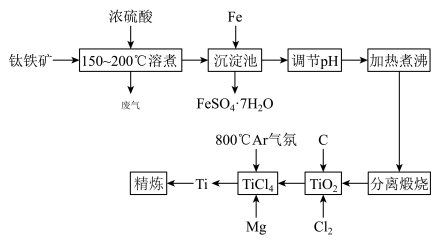
已知:①钛在常温下不与强酸、强碱反应:
②Ti4+易水解生成TiO2+,TiO2+进一步水解可得H2TiO3。
(1)“废气”中含有少量空气污染物,其分子式为___________ 。
(2)“150-200°C溶煮”时生成Fe2(SO4)3和TiOSO4且有气体产生,写出生成TiOSO4反应的化学方程式___________ 。
(3)沉淀池中加入Fe时,开始无气泡,溶液由棕黄色变浅绿色,片刻后有无色无味气体产生。写出Fe参与的离子反应方程式___________ 。
(4)“加热煮沸”操作的主要目的是___________ 。
(5)简述“精炼”阶段,从Ti、Mg混合物获得Ti的实验方案是___________ 。

已知:①钛在常温下不与强酸、强碱反应:
②Ti4+易水解生成TiO2+,TiO2+进一步水解可得H2TiO3。
(1)“废气”中含有少量空气污染物,其分子式为
(2)“150-200°C溶煮”时生成Fe2(SO4)3和TiOSO4且有气体产生,写出生成TiOSO4反应的化学方程式
(3)沉淀池中加入Fe时,开始无气泡,溶液由棕黄色变浅绿色,片刻后有无色无味气体产生。写出Fe参与的离子反应方程式
(4)“加热煮沸”操作的主要目的是
(5)简述“精炼”阶段,从Ti、Mg混合物获得Ti的实验方案是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】赤泥含有Sc2O3(氧化钪)、Al2O3、Fe2O3、SiO2等,以赤泥为原料提取钪(Sc)、氧化钪(Sc2O3)的流程如下:
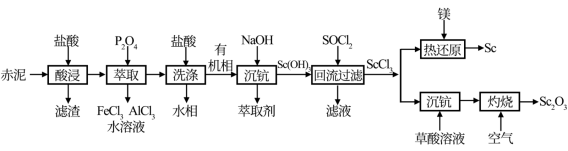
已知:①P2O4为磷酸酯萃取剂(密度小于水);②常温下Ksp[Sc(OH)3]=8.0×10-31。
请回答下列问题:
(1)滤渣的主要成分是___________ (填化学式)。
(2)酸浸”时温度过高,酸浸速率反而减慢,其原因是___________ 。
(3)将盐酸洗涤后所得混合溶液分离的具体操作过程为___________ 。
(4)热还原”的化学方程式为___________ 。
(5)在空气中灼烧草酸钪得到Sc2O3的化学方程式为___________ 。
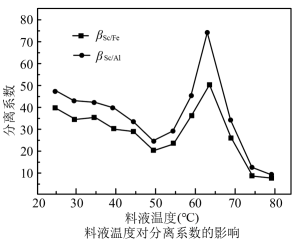
(6)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如下所示,萃取时P2O4最佳浓度及料液温度分别为___________ 、___________ 。(①如表为某温度下所测数据,如图为某浓度P2O4时所测数据。②分离系数β表示物料中两种物质经分离后相对含量的比值)
(7)常温下,已知:c(Sc3+)≤1.0×10-5mol·L-1时表明沉淀完全,加入NaOH沉钪后的萃取剂混合液的pH为6时,是否完全沉淀?___________ (通过计算判断)。

已知:①P2O4为磷酸酯萃取剂(密度小于水);②常温下Ksp[Sc(OH)3]=8.0×10-31。
请回答下列问题:
(1)滤渣的主要成分是
(2)酸浸”时温度过高,酸浸速率反而减慢,其原因是
(3)将盐酸洗涤后所得混合溶液分离的具体操作过程为
(4)热还原”的化学方程式为
(5)在空气中灼烧草酸钪得到Sc2O3的化学方程式为
(6)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如下所示,萃取时P2O4最佳浓度及料液温度分别为

| 试验编号 | P2O4浓度/% | 分相情况 | 钪萃取率/% | 铁萃取率/% |
| 1-1 | 1 | 分相快 | 90.76 | 15.82 |
| 1-2 | 2 | 分相容易 | 91.53 | 19.23 |
| 1-3 | 3 | 分相容易 | 92.98 | 13.56 |
| 1-4 | 4 | 有第三相 | 90.69 | 30.12 |
| 1-5 | 5 | 轻微乳化 | 91.74 | 39.79 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】由于雾霾严重,长沙市19年12月15、16日在部分路段施行了限行。已知汽车尾气排放出的 、
、 等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
(1)汽车尾气中的 和
和 在一定温度和催化剂条件下可发生如下反应:
在一定温度和催化剂条件下可发生如下反应:
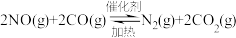

已知:① 燃烧热的
燃烧热的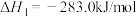
②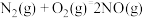
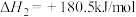 ,则
,则
__________ 。
(2)某研究小组对反应
 进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比
进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比 进行多组实验(各次实验的温度可能相同,也可能不同),测定
进行多组实验(各次实验的温度可能相同,也可能不同),测定 的平衡转化率
的平衡转化率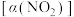 ,部分实验结果如图1所示。
,部分实验结果如图1所示。

①如果将图中 点的平衡状态改变为
点的平衡状态改变为 点的平衡状态,应采取的措施是
点的平衡状态,应采取的措施是__________ 。
②图中 、
、 两点对应的实验温度分别为
两点对应的实验温度分别为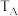 和
和 ,通过判断:
,通过判断: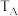
__________  (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(3)工业废气也是产生雾霾的重要原因,某厂采用湿法 氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
① 水解时生成
水解时生成 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:____________________ 。
②过二硫酸钾可通过电解 溶液的方法制得。电解液中含硫微粒主要存在形式与
溶液的方法制得。电解液中含硫微粒主要存在形式与 的关系如图2所示。
的关系如图2所示。
已知在阳极放电的离子主要是 ,阳极区电解质溶液的
,阳极区电解质溶液的 范围为
范围为__________ ;阳极的电极反应式为______________________________ 。
 、
、 等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。(1)汽车尾气中的
 和
和 在一定温度和催化剂条件下可发生如下反应:
在一定温度和催化剂条件下可发生如下反应: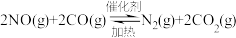

已知:①
 燃烧热的
燃烧热的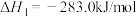
②
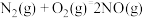
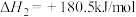 ,则
,则
(2)某研究小组对反应

 进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比
进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比 进行多组实验(各次实验的温度可能相同,也可能不同),测定
进行多组实验(各次实验的温度可能相同,也可能不同),测定 的平衡转化率
的平衡转化率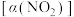 ,部分实验结果如图1所示。
,部分实验结果如图1所示。
①如果将图中
 点的平衡状态改变为
点的平衡状态改变为 点的平衡状态,应采取的措施是
点的平衡状态,应采取的措施是②图中
 、
、 两点对应的实验温度分别为
两点对应的实验温度分别为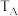 和
和 ,通过判断:
,通过判断: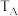
 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。(3)工业废气也是产生雾霾的重要原因,某厂采用湿法
 氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。①
 水解时生成
水解时生成 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:②过二硫酸钾可通过电解
 溶液的方法制得。电解液中含硫微粒主要存在形式与
溶液的方法制得。电解液中含硫微粒主要存在形式与 的关系如图2所示。
的关系如图2所示。
已知在阳极放电的离子主要是
 ,阳极区电解质溶液的
,阳极区电解质溶液的 范围为
范围为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】用含有 、
、 和少量
和少量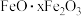 的铝灰制备
的铝灰制备 ,工艺流程如下(部分操作和条件略)。
,工艺流程如下(部分操作和条件略)。
I.向铝灰中加入过量稀 ,过滤;
,过滤;
Ⅱ.向滤液中加入过量 溶液,调节溶液的pH约为3;
溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入 至紫红色消失,过滤;
至紫红色消失,过滤;
V.再经过一系列操作 ,分离得到产品。
(1)步骤I中过滤所得滤渣主要成分是_______ (写化学式);  溶解
溶解 的离子方程式;
的离子方程式;_______ 。
(2)步骤Ⅱ中加入 时发生反应的离子方程式为:
时发生反应的离子方程式为:_______ 。
(3)已知:生成氢氧化物沉淀的pH。
注:金属离子的起始浓度均为 。
。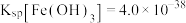 。
。
①根据表中数据解释步骤Ⅱ的目的_______ 。
②当 开始沉淀时,
开始沉淀时, 的浓度约为
的浓度约为_______  。
。
(4)已知:一定条件下, 可与
可与 反应生成
反应生成 。
。
①向一的沉淀中加入浓盐酸并加热,能说明沉淀中存在 的现象是:
的现象是:_______ 。
②步骤Ⅳ中加入 的目的是:
的目的是:_______ 。
(5)步骤V中“一系列操作 ”是_______ 。
 、
、 和少量
和少量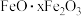 的铝灰制备
的铝灰制备 ,工艺流程如下(部分操作和条件略)。
,工艺流程如下(部分操作和条件略)。I.向铝灰中加入过量稀
 ,过滤;
,过滤;Ⅱ.向滤液中加入过量
 溶液,调节溶液的pH约为3;
溶液,调节溶液的pH约为3;Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入
 至紫红色消失,过滤;
至紫红色消失,过滤;V.再经过
(1)步骤I中过滤所得滤渣主要成分是
 溶解
溶解 的离子方程式;
的离子方程式;(2)步骤Ⅱ中加入
 时发生反应的离子方程式为:
时发生反应的离子方程式为:(3)已知:生成氢氧化物沉淀的pH。
| 化学式 |  |  |  |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
 。
。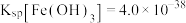 。
。①根据表中数据解释步骤Ⅱ的目的
②当
 开始沉淀时,
开始沉淀时, 的浓度约为
的浓度约为 。
。(4)已知:一定条件下,
 可与
可与 反应生成
反应生成 。
。①向一的沉淀中加入浓盐酸并加热,能说明沉淀中存在
 的现象是:
的现象是:②步骤Ⅳ中加入
 的目的是:
的目的是:(5)步骤V中“
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
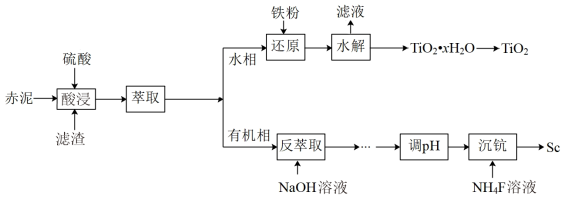
【推荐2】资源的综合利用具有重要战略作用,以废渣(主要成分为Fe2O3、SiO2、TiO2、Sc2O3)为原料回收Sc、SiO2、TiO2的流程如下:
已知:钪离子可以在不同pH下生成 (
(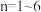 );
);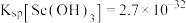 ,
,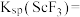
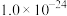 。回答下列问题:
。回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为_______ 。
(2)滤渣的主要成分为_______ (写化学式),加入铁粉的作用是_______ 。
(3)“反萃取”时若加入的氢氧化钠溶液过量,则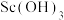 沉淀会溶解。写出
沉淀会溶解。写出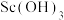 与过量NaOH溶液反应生成
与过量NaOH溶液反应生成 的含产物的化学方程式:
的含产物的化学方程式:_______ 。
(4)加入 溶液后,当溶液中
溶液后,当溶液中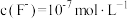 时,
时, 的最大值为
的最大值为_______  。
。
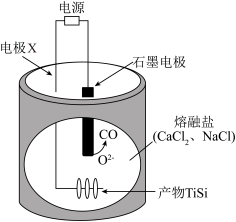
(5)在熔融盐体系中电解 、
、 可获得电池材料TiSi,装置如图所示。石墨电极附近可收集到黄绿色气体,写出该极的两个电极反应式:
可获得电池材料TiSi,装置如图所示。石墨电极附近可收集到黄绿色气体,写出该极的两个电极反应式:_______ 。
(6) 通过氮掺杂反应生成
通过氮掺杂反应生成 ,过程如下图所示。
,过程如下图所示。
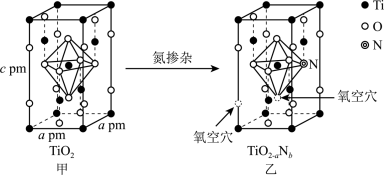
①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为_______  (写出计算式)。
(写出计算式)。
②图乙 晶体中
晶体中
_______ 。

已知:钪离子可以在不同pH下生成
 (
(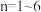 );
);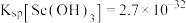 ,
,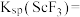
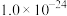 。回答下列问题:
。回答下列问题:(1)基态
 原子的电子排布式为
原子的电子排布式为(2)滤渣的主要成分为
(3)“反萃取”时若加入的氢氧化钠溶液过量,则
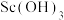 沉淀会溶解。写出
沉淀会溶解。写出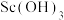 与过量NaOH溶液反应生成
与过量NaOH溶液反应生成 的含产物的化学方程式:
的含产物的化学方程式:(4)加入
 溶液后,当溶液中
溶液后,当溶液中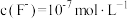 时,
时, 的最大值为
的最大值为 。
。(5)在熔融盐体系中电解
 、
、 可获得电池材料TiSi,装置如图所示。石墨电极附近可收集到黄绿色气体,写出该极的两个电极反应式:
可获得电池材料TiSi,装置如图所示。石墨电极附近可收集到黄绿色气体,写出该极的两个电极反应式:
(6)
 通过氮掺杂反应生成
通过氮掺杂反应生成 ,过程如下图所示。
,过程如下图所示。
①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为
 (写出计算式)。
(写出计算式)。②图乙
 晶体中
晶体中
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】钴周期表第四周期第Ⅷ族元素,其化合物用途广泛,如:LiCoO2做锂电池的正极材料;草酸钴可用于指示剂和催化剂制备。
Ⅰ.(1)LiCoO2中钴元素的化合价为_______
(2)工业上将废锂电池的正极材料与过氧化氢溶液,稀硫酸混合加热,可得到CoSO4回收,反应的化学方程式为:______________ ;可用盐酸代替H2SO4和H2O2的混合液,但缺点是____________
Ⅱ.利用一种含钴矿石[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(3)浸出液中加NaClO3的目的是:______________ .
(4)请用平衡移动原理说明加Na2CO3调pH至5.2所得沉淀的原因:____________
(5)滤液Ⅱ中加入萃取剂的作用是___________
(6)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=___________ 。
Ⅰ.(1)LiCoO2中钴元素的化合价为
(2)工业上将废锂电池的正极材料与过氧化氢溶液,稀硫酸混合加热,可得到CoSO4回收,反应的化学方程式为:
Ⅱ.利用一种含钴矿石[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:
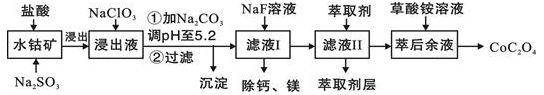
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(3)浸出液中加NaClO3的目的是:
(4)请用平衡移动原理说明加Na2CO3调pH至5.2所得沉淀的原因:
(5)滤液Ⅱ中加入萃取剂的作用是
(6)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=
您最近一年使用:0次
【推荐1】钒是一种熔点高、硬度大、无磁性的金属,广泛应用于钢铁、航空航天、能源、化工等领域。目前工业上使用一种新工艺,以便从冶炼铝的固体废料一赤泥中提取金属钒,赤泥主要含有Fe2O3、Al2O3、V2O5和CuO,具体工艺流程图如下:
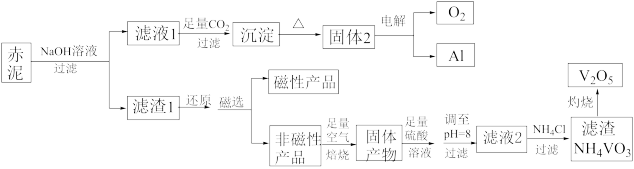
已知:钒有多种价态,其中+5 价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2O VO3-+2H+。回答下列问题:
VO3-+2H+。回答下列问题:
(1)磁性产品的化学式为_________________________ 。
(2)赤泥加入NaOH溶液,发生的离子反应方程式为___________________ 。能否用氨水代替NaOH溶液,___________ (填“能”或“不能”),理由是___________________________________________ 。
(3)滤液1生成沉淀的离子反应方程式为_________________________________________ 。
(4)调至pH=8的目的有两个,一是___________________ ,二是使VO2+转化为VO3-,此时溶液中VO2+和VO3-的物质的量之比为a:b,VO2++H2O VO3-+2H+的平衡常数K=
VO3-+2H+的平衡常数K=____________________ 。
(5)滤液2加氯化铵生成NH4VO3的离子方程式为__________________________ ,该反应能发生是因为__________________________________________ 。

已知:钒有多种价态,其中+5 价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,且存在平衡VO2++H2O
 VO3-+2H+。回答下列问题:
VO3-+2H+。回答下列问题:(1)磁性产品的化学式为
(2)赤泥加入NaOH溶液,发生的离子反应方程式为
(3)滤液1生成沉淀的离子反应方程式为
(4)调至pH=8的目的有两个,一是
 VO3-+2H+的平衡常数K=
VO3-+2H+的平衡常数K=(5)滤液2加氯化铵生成NH4VO3的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:

CO的制备原理: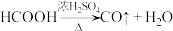 ,并设计出原料气的制备装置(如图),
,并设计出原料气的制备装置(如图),

回答下列问题:
(1)若用以上装置制备干燥纯净的CO。装置b的作用是___________ ,c和d中盛装的试剂分别是___________ 、_____ 。若用以上装置制备 ,在方框内画出收集干燥
,在方框内画出收集干燥 的装置图
的装置图_____ 。
(2)丙烯性质与乙烯类似,如能被酸性 溶液氧化成
溶液氧化成 ,是因为丙烯与乙烯都含有
,是因为丙烯与乙烯都含有___________ (写出具体官能团的名称),两者是___________ 的关系。可推出实验室制备丙烯的化学反应方程式为___________ 。
(3)制丙烯时还产生少量 、
、 ,该小组用以下试剂检验这三种气体,混合气体通过试剂的顺序是
,该小组用以下试剂检验这三种气体,混合气体通过试剂的顺序是___________ (填序号)。
①饱和 溶液 ②酸性
溶液 ②酸性 溶液 ③石灰水 ④品红溶液
溶液 ③石灰水 ④品红溶液
(4)正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,查阅文献得知:
①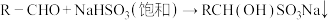 ;②沸点:乙醚34℃,1-丁醇118℃。设计提纯路线如下:
;②沸点:乙醚34℃,1-丁醇118℃。设计提纯路线如下:

其中,试剂1为___________ ,操作2为___________ ,操作3为___________ 。

CO的制备原理:
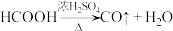 ,并设计出原料气的制备装置(如图),
,并设计出原料气的制备装置(如图),
回答下列问题:
(1)若用以上装置制备干燥纯净的CO。装置b的作用是
 ,在方框内画出收集干燥
,在方框内画出收集干燥 的装置图
的装置图(2)丙烯性质与乙烯类似,如能被酸性
 溶液氧化成
溶液氧化成 ,是因为丙烯与乙烯都含有
,是因为丙烯与乙烯都含有(3)制丙烯时还产生少量
 、
、 ,该小组用以下试剂检验这三种气体,混合气体通过试剂的顺序是
,该小组用以下试剂检验这三种气体,混合气体通过试剂的顺序是①饱和
 溶液 ②酸性
溶液 ②酸性 溶液 ③石灰水 ④品红溶液
溶液 ③石灰水 ④品红溶液(4)正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,查阅文献得知:
①
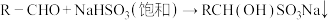 ;②沸点:乙醚34℃,1-丁醇118℃。设计提纯路线如下:
;②沸点:乙醚34℃,1-丁醇118℃。设计提纯路线如下:
其中,试剂1为
您最近一年使用:0次
【推荐3】钛合金在国防、医用器材领域有重要应用,某研究小组利用钛铁矿[主要成分偏钛酸亚铁(FeTiO3),含SiO2、FeO 杂质]制取TiCl4,然后进一步制备金属钛,流程如下∶

已知∶
a.发生的主要反应方程式如下∶
FeTiO3+2H2SO4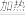 TiOSO4+FeSO4+2H2O TiOSO4+2H2O
TiOSO4+FeSO4+2H2O TiOSO4+2H2O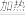 H2TiO3↓+H2SO4
H2TiO3↓+H2SO4
H2TiO3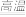 TiO2+H2O
TiO2+H2O
b.部分物质的性质∶
请回答∶
(1)步骤II抽滤时选用了玻璃砂漏斗,请说明选择的理由______ 。
(2)步骤III为了除去浸取液中的铁元素杂质并回收FeSO4∙7H2O。往浸取液中加入铁粉至溶液中的Fe3+完全转化,然后抽滤,滤液用冰盐水快速冷却至FeSO4∙7H2O结晶析出,再次抽滤并洗涤。下列说法正确的是____ 。
A.杂质Fe3+可能是在实验过程中氧化生成的
B.再次抽滤获得的滤液中的溶质是TiOSO4和FeSO4
C.利用冰盐水快速冷却有利于形成较大的晶体颗粒
D.再次抽滤后的洗涤应选用蒸馏水进行多次洗涤
(3)步骤IV包括钛盐的水解、产物的分离和物质的转化。操作步骤如下∶取一部分步骤III获得的滤液→( ) →( ) →( ) →( ) →抽滤得偏钛酸(H2TiO3),将偏钛酸在坩埚中加热得到二氧化钛(TiO2)。
①将下列操作按合理顺序填入以上空格。
a.静置沉降后,用倾析法除去上层水;
b.逐滴加入到沸水中并不停搅拌,继续煮沸约10 min;
c.用热的稀硫酸洗涤沉淀2~3次,然后用热水洗涤沉淀;
d.慢慢加入其余全部滤液,继续煮沸约30 min (过程中适当补充水至原体积);
②写出操作c中用热水洗涤沉淀的具体过程_____ 。
(4)①另一种生产TiCl4的方法是用天然TiO2晶体为原料,利用步骤V的反应原理获得TiCl4.。产品中含有SiCl4、FeCl3等杂质,可通过精馏的方法获得高纯TiCl4,以下说法正确的是______ 。
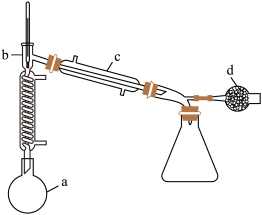
A.收集TiCl4时,仪器a中的温度应控制为136.4°C
B. b处温度计的水银球的上沿和支管口的下沿齐平
C.精馏结束时留在圆底烧瓶中的主要成分是FeCl3和Si
D.装置c中的冷凝水应该“下口进、上口出”
E.可以用水浴加热的方法精馏获得TiCl4
②d处装有碱石灰的干燥管,作用是________ 。

已知∶
a.发生的主要反应方程式如下∶
FeTiO3+2H2SO4
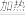 TiOSO4+FeSO4+2H2O TiOSO4+2H2O
TiOSO4+FeSO4+2H2O TiOSO4+2H2O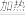 H2TiO3↓+H2SO4
H2TiO3↓+H2SO4H2TiO3
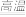 TiO2+H2O
TiO2+H2O b.部分物质的性质∶
| TiCl4 | SiCl4 | FeCl3 | TiO2 | |
| 沸点/°C | 136.4 | 57.6 | 315 | / |
| 其它性质 | 极易水解 | / | / | 不溶于水 |
请回答∶
(1)步骤II抽滤时选用了玻璃砂漏斗,请说明选择的理由
(2)步骤III为了除去浸取液中的铁元素杂质并回收FeSO4∙7H2O。往浸取液中加入铁粉至溶液中的Fe3+完全转化,然后抽滤,滤液用冰盐水快速冷却至FeSO4∙7H2O结晶析出,再次抽滤并洗涤。下列说法正确的是
A.杂质Fe3+可能是在实验过程中氧化生成的
B.再次抽滤获得的滤液中的溶质是TiOSO4和FeSO4
C.利用冰盐水快速冷却有利于形成较大的晶体颗粒
D.再次抽滤后的洗涤应选用蒸馏水进行多次洗涤
(3)步骤IV包括钛盐的水解、产物的分离和物质的转化。操作步骤如下∶取一部分步骤III获得的滤液→
①将下列操作按合理顺序填入以上空格。
a.静置沉降后,用倾析法除去上层水;
b.逐滴加入到沸水中并不停搅拌,继续煮沸约10 min;
c.用热的稀硫酸洗涤沉淀2~3次,然后用热水洗涤沉淀;
d.慢慢加入其余全部滤液,继续煮沸约30 min (过程中适当补充水至原体积);
②写出操作c中用热水洗涤沉淀的具体过程
(4)①另一种生产TiCl4的方法是用天然TiO2晶体为原料,利用步骤V的反应原理获得TiCl4.。产品中含有SiCl4、FeCl3等杂质,可通过精馏的方法获得高纯TiCl4,以下说法正确的是

A.收集TiCl4时,仪器a中的温度应控制为136.4°C
B. b处温度计的水银球的上沿和支管口的下沿齐平
C.精馏结束时留在圆底烧瓶中的主要成分是FeCl3和Si
D.装置c中的冷凝水应该“下口进、上口出”
E.可以用水浴加热的方法精馏获得TiCl4
②d处装有碱石灰的干燥管,作用是
您最近一年使用:0次

 的pH
的pH 的pH
的pH

