碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1) 可作为碱使用的原因是
可作为碱使用的原因是________ (用离子方程式表示)。
(2) 的
的 溶液中由水电离的
溶液中由水电离的
________ 。
(1)
 可作为碱使用的原因是
可作为碱使用的原因是(2)
 的
的 溶液中由水电离的
溶液中由水电离的
更新时间:2023-12-21 21:45:47
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在不同温度下的水溶液中,c(H+)和c(OH-)的关系如图所示:

(1)A点水的离子积为_____________ ,C点水的离子积为_____________ ,对纯水由25℃升高温度至100℃时水的离子积__________ (填“增大”、“减小”或“不变”),各离子浓度由______ 点(填A、B、C、D)变为______ 点(填A、B、C、D)。
(2)100 ℃时,若向B点溶液中滴加硫酸,体系将由B点移向_____ 点(填C或D),为什么_____________________________________ 。
(3)25 ℃时,0.001mol/L的盐酸溶液pH=_______ ;0.001mol/L的氢氧化钠溶液pH=_________ ;若将二者温度都升高至100 ℃,________________ (填“盐酸”、“氢氧化钠”或“盐酸和氢氧化钠”)的pH会改变。

(1)A点水的离子积为
(2)100 ℃时,若向B点溶液中滴加硫酸,体系将由B点移向
(3)25 ℃时,0.001mol/L的盐酸溶液pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】完成下列问题。
(1)一定条件下,在水的电离平衡中,c(H+)和c(OH-)的关系如下图所示。25℃时,Kw=_______ ,100℃时,Kw=_______ ,100℃若盐酸中c(H+)=1.0×10-4mol/L,则由水电离产生的c(H+)=_______ 。B点时pH=2的盐酸与pH=10的氢氧化钠溶液等体积混合后,溶液显_______ 性。

(2)如图所示,一定温度下,冰醋酸加水稀释过程中溶液的导电能力曲线图,请回答。
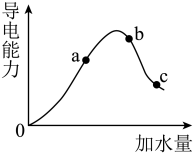
①“O”点为什么不导电_______ 。
②a、b、c三点醋酸的电离程度由大到小的顺序为_______ 。
③在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是_______ 。
A.H+个数 B.c(H+) C.c(H+)/c(CH3COOH) D.CH3COOH分子数
(1)一定条件下,在水的电离平衡中,c(H+)和c(OH-)的关系如下图所示。25℃时,Kw=

(2)如图所示,一定温度下,冰醋酸加水稀释过程中溶液的导电能力曲线图,请回答。

①“O”点为什么不导电
②a、b、c三点醋酸的电离程度由大到小的顺序为
③在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是
A.H+个数 B.c(H+) C.c(H+)/c(CH3COOH) D.CH3COOH分子数
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】常温下,有下列五种溶液:① 、②
、② 、③HCl、④
、③HCl、④ 、⑤NaOH
、⑤NaOH
(1)pH相等的④和⑤溶液,稀释相同的倍数,稀释之后pH较大的是_______ (填字号)
(2)等浓度的上述溶液中,水电离的程度由大到小的顺序_______ (填序号,用>、<、=连接)
(3)向④中加入少量氯化铵固体,此时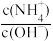 的值
的值_______ (填“增大”“减小”或“不变”)
(4)若将等浓度的③和④的溶液混合后溶液恰好呈中性,则混合前③的体积_______ ④的体积(填“大于”、“小于”或“等于”),此时溶液中离子度由大到小的顺序是_______ 。
(5)取0.1 mol∙L−1,10mL的溶液③,加水稀释到1000mL,则此时溶液中由水电离出的
_______ 。
(6)某学生用已知物质的量浓度的③来滴定未知物质的量浓度的⑤溶液用以测定⑤的浓度,选择甲基橙作指示剂,下列操作中可能使所测NaOH溶液的浓度数值偏低的是_______(填字母序号)。
 、②
、② 、③HCl、④
、③HCl、④ 、⑤NaOH
、⑤NaOH(1)pH相等的④和⑤溶液,稀释相同的倍数,稀释之后pH较大的是
(2)等浓度的上述溶液中,水电离的程度由大到小的顺序
(3)向④中加入少量氯化铵固体,此时
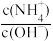 的值
的值(4)若将等浓度的③和④的溶液混合后溶液恰好呈中性,则混合前③的体积
(5)取0.1 mol∙L−1,10mL的溶液③,加水稀释到1000mL,则此时溶液中由水电离出的

(6)某学生用已知物质的量浓度的③来滴定未知物质的量浓度的⑤溶液用以测定⑤的浓度,选择甲基橙作指示剂,下列操作中可能使所测NaOH溶液的浓度数值偏低的是_______(填字母序号)。
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】欲同时施用N、P、K三种化肥,下列组合中最适当的是:__________
①K2CO3 ②KCl ③Ca(H2PO4)2 ④NH3·H2O ⑤NH4Cl
①K2CO3 ②KCl ③Ca(H2PO4)2 ④NH3·H2O ⑤NH4Cl
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:(单位省略)
(1)写出碳酸的第一步电离方程式_______ 。
(2)25℃时,等浓度的三种溶液①NaCN溶液、②Na2CO3溶液、③CH3COONa溶液,pH由大到小的顺序为_______ (填序号)。
(3)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为_______ 。
| 醋酸 | 碳酸 | 氢氰酸 |
| Ka=1.7×10-5 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka=6.2×10-10 |
(1)写出碳酸的第一步电离方程式
(2)25℃时,等浓度的三种溶液①NaCN溶液、②Na2CO3溶液、③CH3COONa溶液,pH由大到小的顺序为
(3)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)氯化铝水溶液呈__ 性,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):___ ;把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是__ 。
(2)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是___ 。
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
回答下列问题
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为___ 。
②向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:___ 。
(2)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为
②向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:
您最近一年使用:0次



