分析化学中以K2CrO4为指示剂,用AgNO3标准溶液滴定溶液中的Cl-,测定c(Cl-)。
已知:ⅰ.K2CrO4溶液中存在平衡:2 +2H+
+2H+
 +H2O
+H2O
ⅱ.25 °C时,Ksp (Ag2CrO4)=2. 0×10-12 (砖红色),Ksp(AgCl)=1.8×10-10(白色),Ksp(Ag2Cr2O7)=2×10-7(深红色);
ⅲ.离子浓度≤10-5mol/L时,认为其完全沉淀。
下列分析不正确的是
已知:ⅰ.K2CrO4溶液中存在平衡:2
 +2H+
+2H+
 +H2O
+H2Oⅱ.25 °C时,Ksp (Ag2CrO4)=2. 0×10-12 (砖红色),Ksp(AgCl)=1.8×10-10(白色),Ksp(Ag2Cr2O7)=2×10-7(深红色);
ⅲ.离子浓度≤10-5mol/L时,认为其完全沉淀。
下列分析不正确的是
| A.实验中先产生白色沉淀,滴定终点时产生砖红色沉淀 |
B.产生白色沉淀时,存在AgCl(s) Ag+ (aq)+C1-(aq)。 Ag+ (aq)+C1-(aq)。 |
C.当产生砖红色沉淀时,如果c( )=5.0×10-3mol/L,则C1-已沉淀完全 )=5.0×10-3mol/L,则C1-已沉淀完全 |
| D.滴定时应控制溶液pH在合适范围内,若pH过低,会导致测定结果偏低 |
更新时间:2024-02-02 10:34:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度下,分别向 浓度均为
浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液中
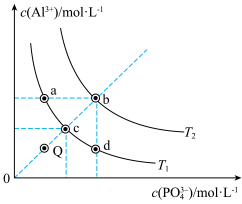
溶液,滴加过程中溶液中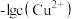 和
和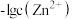 与
与 溶液体积
溶液体积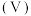 的关系如图所示[已知:
的关系如图所示[已知: ,
,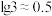 ]。下列说法正确的是
]。下列说法正确的是

 浓度均为
浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中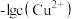 和
和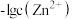 与
与 溶液体积
溶液体积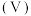 的关系如图所示[已知:
的关系如图所示[已知: ,
,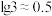 ]。下列说法正确的是
]。下列说法正确的是
A.溶液 : :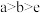 |
B.a点的 溶液中: 溶液中: |
C. 为滴定 为滴定 溶液的曲线 溶液的曲线 |
D. 点纵坐标约为33.9 点纵坐标约为33.9 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列化学方程式或离子方程式中,不能正确表达反应颜色变化的是
A.向 溶液中滴入 溶液中滴入 溶液,溶液变红: 溶液,溶液变红: |
B.澄清石灰水久置后溶液中出现白色固体: |
C. 放置在空气中后由淡黄色变为白色: 放置在空气中后由淡黄色变为白色: |
D.向 悬浊液中滴加足量 悬浊液中滴加足量 溶液后,溶液中出现黑色沉淀: 溶液后,溶液中出现黑色沉淀: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】锂电池具有广泛应用。用废铝渣(含金属铝、锂盐等)获得电池级 的一种工艺流程如图(部分物质已略去):
的一种工艺流程如图(部分物质已略去):

下列说法不正确 的是
 的一种工艺流程如图(部分物质已略去):
的一种工艺流程如图(部分物质已略去):
下列说法
A.用焰色试验检验①加热后得到滤液中的 ,是因为电子从激发态跃迁至基态或较低能级时以光的形式释放能量 ,是因为电子从激发态跃迁至基态或较低能级时以光的形式释放能量 |
B.②中生成 的离子方程式: 的离子方程式: |
C.由③推测溶解度: |
D.依据对角线规则, 微溶于水可以推测 微溶于水可以推测 在水中溶解度不大 在水中溶解度不大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列对应化学反应的离子方程式书写正确的是
A. 通入过量氨水中: 通入过量氨水中: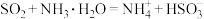 |
B.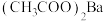 溶液中滴入稀硫酸: 溶液中滴入稀硫酸: |
C. 悬浊液中加入 悬浊液中加入 溶液: 溶液: |
D.用两个银电极,电解 溶液: 溶液: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温时,若Ca(OH)2和CaWO4 (钨酸钙)的沉淀溶解平衡曲线如图所示(已知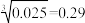 )。下列分析正确的是
)。下列分析正确的是

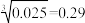 )。下列分析正确的是
)。下列分析正确的是
A.由图可知常温下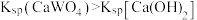 |
| B.室温下饱和Ca(OH)2溶液中加入少量CaO,溶液变浑浊,恢复至室温,Ca(OH)2的Ksp不变,钙离子浓度不变 |
C.饱和 Ca(OH)2溶液和饱和CaWO4溶液等体积混合: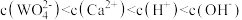 |
| D.d点的CaWO4溶液中,加入CaCl2固体,d点溶液组成沿da线c点移动(假设混合后溶液体积不变) |
您最近一年使用:0次
【推荐2】下列实验操作、现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 其他条件不变,将NO2气体压缩至原体积的一半 | NO2气体颜色逐渐变到比压缩前还浅 | 增大压强,平衡向体积缩小的方向移动 |
| B | 将收集满Cl2的集气瓶A口朝上,装满N2的集气瓶B口朝下对准A,移走玻璃片 | 一段时间后集气瓶AB均出现黄绿色 | 该实验中熵增的方向是自发进行的 |
| C | 在稀硫酸中加入少量的红色Cu2O粉末 | 产生蓝色溶液和红色固体 | Cu2O在该反应中没有体现还原性 |
| D | 在含S2-和 的溶液中滴加 的溶液中滴加 溶液 溶液 | 先生成黑色沉淀,后生成白色沉淀 | 溶度积: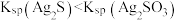 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知:室温下,Ksp(AgC1)=2.0×10-10;Ksp(AgBr)=5.4×10-13;Ksp(AgI)=8.3×10-17;Ksp(Ag2CrO4)=2.0×10-12,Ag2CrO4为难溶于水和酸的红色固体。下列说法不正确的是
| A.上面四种银盐饱和溶液中,c(Ag+)最大的是Ag2CrO4溶液 |
| B.用标准AgNO3溶液滴定某溶液中的氯离子含量,可选用K2CrO4作指示剂。 |
C.向NaCl和KI混合溶液中加入AgNO3溶液,当两种沉淀共存时,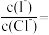 4.15×10-7 4.15×10-7 |
| D.向AgBr悬浊液加入一定量的NaCl固体后c(Cl-)=10-4mol/L,可使平衡AgBr(s)⇌Ag+(aq)+Br-(aq)正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是Ca(OH)2在温度分别为T1、T2时的两种沉淀溶解平衡曲线(图中浓度单位为mol·L-1,与曲线Ⅰ对应的Ksp=4×10-6,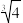 ≈1.6),下列说法中正确的是( )
≈1.6),下列说法中正确的是( )
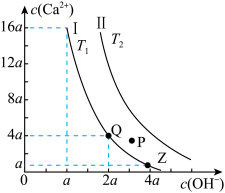
 ≈1.6),下列说法中正确的是( )
≈1.6),下列说法中正确的是( )
| A.温度:T1<T2 |
| B.在温度为T1时,P点分散系中分散质粒子直径<1nm |
| C.加水稀释时溶液碱性减弱,Z点溶液可转化为Q点溶液 |
| D.Q点的溶液中c(OH-)约为0.0125mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,几种硫化物的溶度积如表所示。
下列叙述错误的是
| 硫化物 |  |  |  |  |
 | 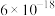 |  |  |  |
A.溶解度: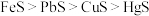 |
B.饱和 溶液中 溶液中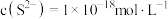 |
C.向含等浓度 和 和 的废水中通入 的废水中通入 气体,先生成 气体,先生成 沉淀 沉淀 |
D. 的平衡常数 的平衡常数 为 为 |
您最近一年使用:0次

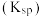 如下表:
如下表:





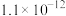

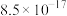
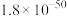
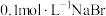 溶液,可完成沉淀的转化
溶液,可完成沉淀的转化 的平衡常数约为
的平衡常数约为
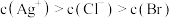
 +2H2O
+2H2O (aq)
(aq)