基于所学内容回答问题
(1)基态铜原子的价电子排布式为_________ ,其核外电子的空间运动状态有________ 种;As原子的价电子排布图为________________ 。
(2) 与
与 同周期,
同周期,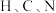 三种元素的电负性从小到大的顺序为
三种元素的电负性从小到大的顺序为________ ; 、
、 、
、 的第一电离能从大到小的顺序为
的第一电离能从大到小的顺序为________________ 。
(3) 的电子式
的电子式_________ , 的沸点高于
的沸点高于 的原因是
的原因是_________ 。
(4)已知 的熔点高于
的熔点高于 的熔点,其原因是
的熔点,其原因是__________________ 。
(5)铜的某种氧化物的晶胞结构如图所示,若该晶胞中 原子与
原子与 原子之间的最近距离为apm,设阿伏加德罗常数的值为
原子之间的最近距离为apm,设阿伏加德罗常数的值为 ,则该晶胞的密度为
,则该晶胞的密度为_________  (填含
(填含 的表达式)。
的表达式)。
(1)基态铜原子的价电子排布式为
(2)
 与
与 同周期,
同周期,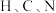 三种元素的电负性从小到大的顺序为
三种元素的电负性从小到大的顺序为 、
、 、
、 的第一电离能从大到小的顺序为
的第一电离能从大到小的顺序为(3)
 的电子式
的电子式 的沸点高于
的沸点高于 的原因是
的原因是(4)已知
 的熔点高于
的熔点高于 的熔点,其原因是
的熔点,其原因是(5)铜的某种氧化物的晶胞结构如图所示,若该晶胞中
 原子与
原子与 原子之间的最近距离为apm,设阿伏加德罗常数的值为
原子之间的最近距离为apm,设阿伏加德罗常数的值为 ,则该晶胞的密度为
,则该晶胞的密度为 (填含
(填含 的表达式)。
的表达式)。 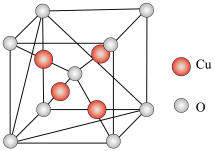
更新时间:2024-01-23 21:54:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求填空:
(1) 基态的电子排布式可表示为
基态的电子排布式可表示为___________ ,Mn在元素周期表中的位置为___________ ,属于___________ 区。
(2) 的空间构型是
的空间构型是___________ (用文字表述),N原子的轨道杂化方式为___________ 。
(3) 在酸性溶液中不稳定,可发生歧化反应生成
在酸性溶液中不稳定,可发生歧化反应生成 和Cu。但CuO在高温下会分解成
和Cu。但CuO在高温下会分解成 ,试从结构角度解释高温下CuO为何会生成
,试从结构角度解释高温下CuO为何会生成 的原因:
的原因:___________ 。
(4)某同学所画的电子轨道表示式为: 违背了
违背了___________ (填原理或规则名称)
(1)
 基态的电子排布式可表示为
基态的电子排布式可表示为(2)
 的空间构型是
的空间构型是(3)
 在酸性溶液中不稳定,可发生歧化反应生成
在酸性溶液中不稳定,可发生歧化反应生成 和Cu。但CuO在高温下会分解成
和Cu。但CuO在高温下会分解成 ,试从结构角度解释高温下CuO为何会生成
,试从结构角度解释高温下CuO为何会生成 的原因:
的原因:(4)某同学所画的电子轨道表示式为:
 违背了
违背了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示。________________________ 。
(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有__________ (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_______________ 。
(3)实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是_____________________________ 。
(4)向硫酸铜水溶液中逐滴加入氨水直至过量,反应的离子方程式为______________________ 。

(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
(3)实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是
(4)向硫酸铜水溶液中逐滴加入氨水直至过量,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】依据物质结构知识回答下列问题。
Ⅰ.硒是一种非金属,与氧、硫同主族,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为___________ 。
(2)根据价层电子对互斥理论,可以推知 的空间构型为
的空间构型为___________ ,其中Se原子采用的轨道杂化方式为___________ 。
(3)已知 与CO2结构相似,①
与CO2结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③SeO3分子内的键角
、③SeO3分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为___________ (填序号)。
Ⅱ.碳是一种重要元素,可形成多种单质及化合物。
(4)推算HCN分子中σ键与π键数目之比为___________ 。
(5)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。下列电子排布图能表示碳原子的最低能量状态的是___________。
Ⅰ.硒是一种非金属,与氧、硫同主族,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为
(2)根据价层电子对互斥理论,可以推知
 的空间构型为
的空间构型为(3)已知
 与CO2结构相似,①
与CO2结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③SeO3分子内的键角
、③SeO3分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为Ⅱ.碳是一种重要元素,可形成多种单质及化合物。
(4)推算HCN分子中σ键与π键数目之比为
(5)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。下列电子排布图能表示碳原子的最低能量状态的是___________。
A.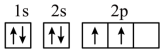 | B.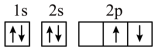 |
C.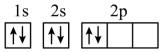 | D.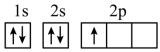 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有A、B、C、D、E五种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数;E元素位于A元素的下一周期,最外层电子数与A相同,价电子数比A多5个;R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1。请回答下列问题:
(1)周期表中元素E位于第____ 周期第_____ 族,E的原子核外电子排布式___________ ;
(2)化合物R的电子式为____ 。
(3)B—的电子排布式为__ ,在CB3分子中C元素原子的原子轨道发生的是___ 杂化。
(4)C的氢化物的空间构型为______ ,C的氢化物极易溶于水的原因是_____ 。
(5)B元素的电负性___ D元素的电负性(填“>”,“<”或“=”);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:____ 。
(1)周期表中元素E位于第
(2)化合物R的电子式为
(3)B—的电子排布式为
(4)C的氢化物的空间构型为
(5)B元素的电负性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯( )与四氟乙烯(
)与四氟乙烯( )的共聚物(
)的共聚物( )制成。回答下列问题:
)制成。回答下列问题:
(1)基态 原子的价电子排布图(轨道表示式)为
原子的价电子排布图(轨道表示式)为_______ ;下列表示氟原子激发态的电子排布式有_______ ,其中能量较高的是_______ 。(填标号)
a. B.
B. C.
C.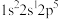 D.
D.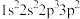
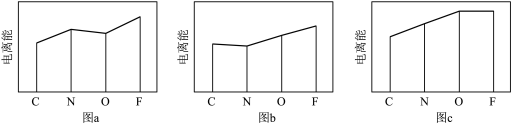
(2)图 、
、 、
、 分别表示
分别表示 、
、 、
、 和
和 的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是
的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填标号);第三电离能的变化图是_______ (填标号)。
(3)试写出 的结构简式
的结构简式_______ ; 中所含元素电负性由大到小的顺序是
中所含元素电负性由大到小的顺序是_______ 。
(4) 和
和 分子中
分子中 的杂化轨道类型分别为
的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
 )与四氟乙烯(
)与四氟乙烯( )的共聚物(
)的共聚物( )制成。回答下列问题:
)制成。回答下列问题:(1)基态
 原子的价电子排布图(轨道表示式)为
原子的价电子排布图(轨道表示式)为a.
 B.
B. C.
C.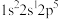 D.
D.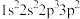
(2)图
 、
、 、
、 分别表示
分别表示 、
、 、
、 和
和 的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是
的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是
(3)试写出
 的结构简式
的结构简式 中所含元素电负性由大到小的顺序是
中所含元素电负性由大到小的顺序是(4)
 和
和 分子中
分子中 的杂化轨道类型分别为
的杂化轨道类型分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】短周期的元素在自然界中比较常见,尤其是非金属元素及其化合物在社会生活中有着很重要的作用。
(1)补全元素周期表中符号。
表中元素形成的最稳定氢化物是_____ ,该氢化物在CCl4中的溶解度比在水中的溶解度_____ (填“大”或“小”)。
(2)硅原子核外电子运动状态为_____ 种,其最外层电子排布式为_____ ,硅微粒非常坚硬,比较晶体硅与碳化硅的熔点高低并解释说明_____ 。
(3)碳元素的非金属性比硫_____ ,可由一复分解反应推测而得,其反应的化学方程式为_____ 。
(4)烟气中的NO与尿素[CO(NH2)2](C的化合价为+4)反应进行脱硝。反应的化学方程式是:2CO(NH2)2+8NO=2CO2+6N2+O2+4H2O。该反应的氧化产物为_____ ,若反应过程中有2.24L(标准状况下)NO反应,则电子转移的数目为_____ 。
(1)补全元素周期表中符号。
| C | N | O | F | |
| Al | Si | S | Cl |
表中元素形成的最稳定氢化物是
(2)硅原子核外电子运动状态为
(3)碳元素的非金属性比硫
(4)烟气中的NO与尿素[CO(NH2)2](C的化合价为+4)反应进行脱硝。反应的化学方程式是:2CO(NH2)2+8NO=2CO2+6N2+O2+4H2O。该反应的氧化产物为
您最近一年使用:0次
【推荐1】依据原子结构知识回答:
(1) 基态原子的电子排布式是
基态原子的电子排布式是_______________________________ ;S的价层电子排布式是_________________ 。
(2)基态的 原子有
原子有______ 个未成对电子, 的外围电子排布图为
的外围电子排布图为______________ 。
(3)四种元素 、K、O、
、K、O、 中第一电离能最小的是
中第一电离能最小的是 _____ ,电负性最大的是 ______ 。
(4)下列有关微粒性质的排列顺序中,错误的是______ 。
A.元素的电负性: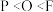
 元素的第一电离能:
元素的第一电离能: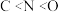
C.离子半径: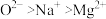
 原子的未成对电子数:
原子的未成对电子数:
(1)
 基态原子的电子排布式是
基态原子的电子排布式是(2)基态的
 原子有
原子有 的外围电子排布图为
的外围电子排布图为(3)四种元素
 、K、O、
、K、O、 中第一电离能最小的是
中第一电离能最小的是 (4)下列有关微粒性质的排列顺序中,错误的是
A.元素的电负性:
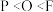
 元素的第一电离能:
元素的第一电离能: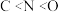
C.离子半径:
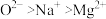
 原子的未成对电子数:
原子的未成对电子数:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】三草酸合铁酸钾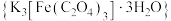 是制备铁触媒上的主要原料。在光照下分解:
是制备铁触媒上的主要原料。在光照下分解:
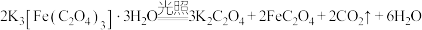 。回答下列问题:
。回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为___________ ,基态 与
与 中未成对电子的数目之比为
中未成对电子的数目之比为___________ 。
(2)三草酸合铁酸钾所含元素中,第一电离能最大的是___________ (填元素符号,下同),电负性最大的是___________ 。
(3)1个 与1个
与1个 分子中
分子中 键数目之比为
键数目之比为___________ , 分子的立体构型为
分子的立体构型为___________ 。
(4)金刚石的晶胞结构如图所示,碳原子分别位于顶点、面心和体内。

若图中原子1的坐标为 ,则原子2的坐标为
,则原子2的坐标为___________ 。
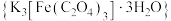 是制备铁触媒上的主要原料。在光照下分解:
是制备铁触媒上的主要原料。在光照下分解: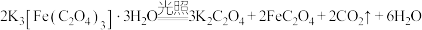 。回答下列问题:
。回答下列问题:(1)基态
 原子的电子排布式为
原子的电子排布式为 与
与 中未成对电子的数目之比为
中未成对电子的数目之比为(2)三草酸合铁酸钾所含元素中,第一电离能最大的是
(3)1个
 与1个
与1个 分子中
分子中 键数目之比为
键数目之比为 分子的立体构型为
分子的立体构型为(4)金刚石的晶胞结构如图所示,碳原子分别位于顶点、面心和体内。

若图中原子1的坐标为
 ,则原子2的坐标为
,则原子2的坐标为
您最近一年使用:0次
【推荐1】2022年北京冬季奥运会场馆建设使用了大量不锈钢材质,不锈钢属于铁碳合金,常含铬 、镍
、镍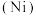 等元素。回答下列问题:
等元素。回答下列问题:
(1)碳的价电子排布式为_______ 碳的一种单质石墨是单层二维蜂窝状晶格结构的新材料(如图1),其中碳原子采取_______ 杂化,在层中碳原子的配位数为_______ 。

(2)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图2所示。晶体中每个镁原子周围距离最近的铁原子有_______ 个,该铁镁合金中原子个数比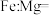
_______ ;原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ,C为
,C为 ,B点坐标参数为
,B点坐标参数为_______ 。

(3)金属铬晶胞如图3,已知其密度为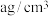 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中铬原子的半径为
,则晶体中铬原子的半径为_______ cm(用含 的表达式表示)。
的表达式表示)。
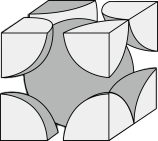
图3
 、镍
、镍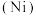 等元素。回答下列问题:
等元素。回答下列问题:(1)碳的价电子排布式为

(2)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图2所示。晶体中每个镁原子周围距离最近的铁原子有
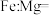
 ,C为
,C为 ,B点坐标参数为
,B点坐标参数为
(3)金属铬晶胞如图3,已知其密度为
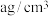 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中铬原子的半径为
,则晶体中铬原子的半径为 的表达式表示)。
的表达式表示)。
图3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】非金属元素及其化合物应用广泛,回答下列问题:
(1)元素的第一电离能:Al___________ Si(填“>”或“<”)。
(2)基态Si原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ 。
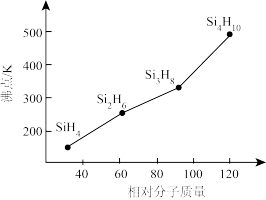
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是___________ 。
(4)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为___________ ,该材料的化学式为___________ 。

(5)如图EMIM+离子中,碳原子的杂化轨道类型为___________ 。分子中的大π键可用符号π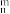 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ),则EMIM+离子中的大π键应表示为
),则EMIM+离子中的大π键应表示为___________ 。

(1)元素的第一电离能:Al
(2)基态Si原子中,电子占据的最高能层符号为
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是

(4)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为

(5)如图EMIM+离子中,碳原子的杂化轨道类型为
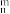 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ),则EMIM+离子中的大π键应表示为
),则EMIM+离子中的大π键应表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图为几种晶体或晶胞的结构示意图。
(1)CaCl2晶体属于___________ 晶体。
(2)微粒之间以共价键结合而形成晶体的是___________ (填写晶体名称)。
(3)冰、金刚石、MgO、碘单质四种晶体的熔点由高到低的顺序为___________ 。
(4)NaCl晶胞与MgO晶胞结构相同,而NaCl晶体的熔点小于MgO晶体的熔点,原因是___________ 。
(5)GaN是很好的半导体材料,晶体类型与金刚石晶体类似,晶胞结构如图1所示,已知六棱柱底边边长为acm。从GaN晶体中分割出的平行六面体如图2。若该平行六面体的体积为 a3cm3,GaN晶体的密度为
a3cm3,GaN晶体的密度为___________ g·cm-3(用a、NA表示,近似相对原子量:Ga70;N14)

(1)CaCl2晶体属于
(2)微粒之间以共价键结合而形成晶体的是
(3)冰、金刚石、MgO、碘单质四种晶体的熔点由高到低的顺序为
(4)NaCl晶胞与MgO晶胞结构相同,而NaCl晶体的熔点小于MgO晶体的熔点,原因是
(5)GaN是很好的半导体材料,晶体类型与金刚石晶体类似,晶胞结构如图1所示,已知六棱柱底边边长为acm。从GaN晶体中分割出的平行六面体如图2。若该平行六面体的体积为
 a3cm3,GaN晶体的密度为
a3cm3,GaN晶体的密度为
您最近一年使用:0次



