运用化学反应原理的相关知识,回答下列问题。
(1)铁管在潮湿环境中易发生吸氧腐蚀,其正极的反应式为___________ ,镶嵌锌块可减缓腐蚀,该法称为___________ 。
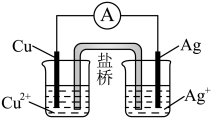
(2)如下图所示的原电池装置中,负极的电极反应式为___________ ,盐桥中的阳离子进入___________ (填“ ”或“
”或“ ”)电极溶液中。
”)电极溶液中。
(3)在一个容积不变的密闭容器中发生反应: ,其平衡常数
,其平衡常数 和温度
和温度 的关系如下表所示。
的关系如下表所示。
若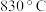 时,在某时刻反应混合物中
时,在某时刻反应混合物中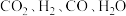 的浓度分别为
的浓度分别为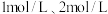 、
、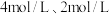 ,则此时上述反应的平衡移动方向为
,则此时上述反应的平衡移动方向为___________ (填“正反应方向”、“逆反应方向”或“不移动”)。
(4)常温下, 溶液的
溶液的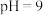 ,
,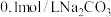 溶液的
溶液的 。
。
①由以上数据计算可知, 的电离常数
的电离常数
___________ 。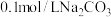 溶液中由水电离出的
溶液中由水电离出的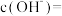
___________ ,该溶液可用于去除油污,用离子方程式说明其原因___________ 。
②下列不能在 溶液中大量存在的离子是
溶液中大量存在的离子是___________ (填标号)。
a. b.
b. c.
c. d.
d.
(1)铁管在潮湿环境中易发生吸氧腐蚀,其正极的反应式为
(2)如下图所示的原电池装置中,负极的电极反应式为
 ”或“
”或“ ”)电极溶液中。
”)电极溶液中。
(3)在一个容积不变的密闭容器中发生反应:
 ,其平衡常数
,其平衡常数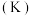 和温度
和温度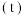 的关系如下表所示。
的关系如下表所示。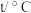 | 700 | 800 | 830 | 1000 | 1200 |
 | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
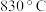 时,在某时刻反应混合物中
时,在某时刻反应混合物中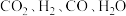 的浓度分别为
的浓度分别为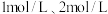 、
、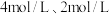 ,则此时上述反应的平衡移动方向为
,则此时上述反应的平衡移动方向为(4)常温下,
 溶液的
溶液的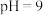 ,
,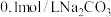 溶液的
溶液的 。
。①由以上数据计算可知,
 的电离常数
的电离常数
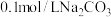 溶液中由水电离出的
溶液中由水电离出的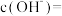
②下列不能在
 溶液中大量存在的离子是
溶液中大量存在的离子是a.
 b.
b. c.
c. d.
d.
更新时间:2024-02-04 21:16:44
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.研究氮和碳的化合物对工业生产和防治污染有重要意义,回答下列问题:
(1)化学键键能数据如下:
合成氨反应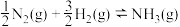 的活化能
的活化能 ,由此计算氨分解反应
,由此计算氨分解反应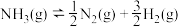 的活化能
的活化能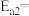
_______  。
。
(2)利用 的还原性可以消除氮氧化物的污染,其中除去
的还原性可以消除氮氧化物的污染,其中除去 的主要反应如下:
的主要反应如下:
 。某研究小组将
。某研究小组将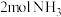 、
、 和一定量的
和一定量的 充入
充入 密闭容器中,在
密闭容器中,在 催化剂表面发生上述反应,
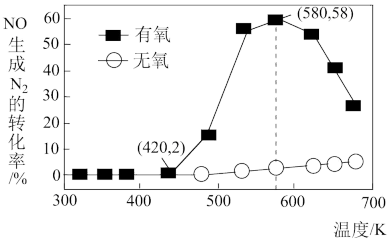
催化剂表面发生上述反应, 的转化率随温度变化的情况如图所示:
的转化率随温度变化的情况如图所示:
①温度从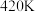 升高到
升高到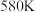 用时
用时 ,则此时段内
,则此时段内 的平均反应速率
的平均反应速率
_______ ;
②在有氧条件下,温度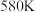 之后
之后 生成
生成 的转化率降低的原因可能是
的转化率降低的原因可能是_______ 。
Ⅱ. 目前有一种新的循环利用方案处理航天员呼吸产生的 ,是用
,是用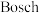 反应
反应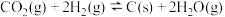
 ,再电解水实现
,再电解水实现 的循环利用。
的循环利用。
(3)若要此反应自发进行_______ (填“高温”或“低温”)更有利。
(4) 时,向体积为
时,向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入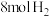 和
和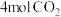 发生以上反应,若反应起始和平衡时温度相同(均为
发生以上反应,若反应起始和平衡时温度相同(均为 ),测得反应过程中压强随时间的变化如表所示:
),测得反应过程中压强随时间的变化如表所示:
① 时
时 反应的
反应的
_______ ( 为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
② 反应的速率方程:
反应的速率方程: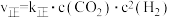 ,
,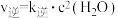 (k是速率常数,只与温度有关)。
(k是速率常数,只与温度有关)。
 时,
时,
_______ 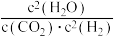 (填“
(填“ ”“
”“ ”或“
”或“ ”)
”)
(5)工业上常用氨水吸收二氧化硫,通过计算判断常温下 溶液的酸碱性并说明判断依据:
溶液的酸碱性并说明判断依据:_______ 。(已知: 的
的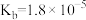 ;
; 的
的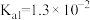 ,
,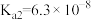 。)
。)
(1)化学键键能数据如下:
| 化学键 |  |  |  |
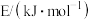 | 436 | 946 | 391 |
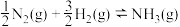 的活化能
的活化能 ,由此计算氨分解反应
,由此计算氨分解反应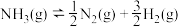 的活化能
的活化能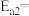
 。
。(2)利用
 的还原性可以消除氮氧化物的污染,其中除去
的还原性可以消除氮氧化物的污染,其中除去 的主要反应如下:
的主要反应如下:
 。某研究小组将
。某研究小组将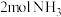 、
、 和一定量的
和一定量的 充入
充入 密闭容器中,在
密闭容器中,在 催化剂表面发生上述反应,
催化剂表面发生上述反应, 的转化率随温度变化的情况如图所示:
的转化率随温度变化的情况如图所示:
①温度从
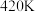 升高到
升高到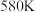 用时
用时 ,则此时段内
,则此时段内 的平均反应速率
的平均反应速率
②在有氧条件下,温度
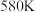 之后
之后 生成
生成 的转化率降低的原因可能是
的转化率降低的原因可能是Ⅱ. 目前有一种新的循环利用方案处理航天员呼吸产生的
 ,是用
,是用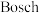 反应
反应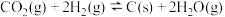
 ,再电解水实现
,再电解水实现 的循环利用。
的循环利用。(3)若要此反应自发进行
(4)
 时,向体积为
时,向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入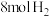 和
和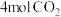 发生以上反应,若反应起始和平衡时温度相同(均为
发生以上反应,若反应起始和平衡时温度相同(均为 ),测得反应过程中压强随时间的变化如表所示:
),测得反应过程中压强随时间的变化如表所示:时间/ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强 |  |  | 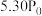 | 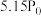 | 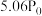 |  |  |
 时
时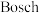 反应的
反应的
 为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)②
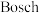 反应的速率方程:
反应的速率方程: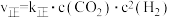 ,
,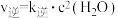 (k是速率常数,只与温度有关)。
(k是速率常数,只与温度有关)。 时,
时,
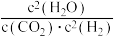 (填“
(填“ ”“
”“ ”或“
”或“ ”)
”)(5)工业上常用氨水吸收二氧化硫,通过计算判断常温下
 溶液的酸碱性并说明判断依据:
溶液的酸碱性并说明判断依据: 的
的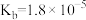 ;
; 的
的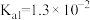 ,
,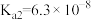 。)
。)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
真题
【推荐2】硼酸(H3BO3)在食品、医药领域应用广泛。
(1)请完成B2H6气体与水反应的化学方程式:B2H6+ 6H2O=2H3BO3+__________ 。
(2)在其他条件相同时,反应H3BO3+3CH3OH B(OCH3)3+3H2O中,H3BO3的转化率(
B(OCH3)3+3H2O中,H3BO3的转化率( )在不同温度下随反应时间(t)的变化见图12,由此图可得出:
)在不同温度下随反应时间(t)的变化见图12,由此图可得出:
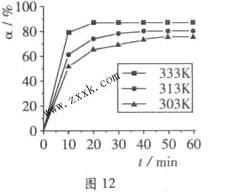
①温度对应该反应的反应速率和平衡移动的影响是_______________________ 。
②该反应的
_____ 0(填“<”、“=”或“>”)。
(3)H3BO3溶液中存在如下反应:H3BO3(aq)+H2O(l) [B(OH)4]-( aq)+H+(aq),已知0.70 mol·L-1H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0 × 10-5mol·L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
[B(OH)4]-( aq)+H+(aq),已知0.70 mol·L-1H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0 × 10-5mol·L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)__________
(1)请完成B2H6气体与水反应的化学方程式:B2H6+ 6H2O=2H3BO3+
(2)在其他条件相同时,反应H3BO3+3CH3OH
 B(OCH3)3+3H2O中,H3BO3的转化率(
B(OCH3)3+3H2O中,H3BO3的转化率( )在不同温度下随反应时间(t)的变化见图12,由此图可得出:
)在不同温度下随反应时间(t)的变化见图12,由此图可得出:
①温度对应该反应的反应速率和平衡移动的影响是
②该反应的

(3)H3BO3溶液中存在如下反应:H3BO3(aq)+H2O(l)
 [B(OH)4]-( aq)+H+(aq),已知0.70 mol·L-1H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0 × 10-5mol·L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
[B(OH)4]-( aq)+H+(aq),已知0.70 mol·L-1H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0 × 10-5mol·L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】 资源化利用有助于实现“双碳目标”。选择不同条件,利用
资源化利用有助于实现“双碳目标”。选择不同条件,利用 和
和 可获得甲醇、甲醛等多种有机物。回答下列问题:
可获得甲醇、甲醛等多种有机物。回答下列问题:
(1)工业上在 催化下利用
催化下利用 发生如下反应I生产甲醇,同时伴有反应Ⅱ发生。
发生如下反应I生产甲醇,同时伴有反应Ⅱ发生。
I.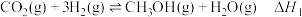
Ⅱ.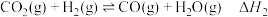
①已知反应过程中相关物质的相对能量如图所示,则反应I的
___________ 。 的
的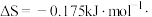
 ,则下列温度下该反应能自发进行的是
,则下列温度下该反应能自发进行的是___________ (填标号)。
A.5℃ B.10℃ C.50℃ D.500℃
③按照 投料,在恒容密闭容器中进行反应,
投料,在恒容密闭容器中进行反应, 的平衡转化率随温度和压强的变化如图所示,则压强
的平衡转化率随温度和压强的变化如图所示,则压强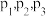 由大到小的顺序为
由大到小的顺序为___________ 。在 压强下,温度高于300℃之后,随着温度升高,
压强下,温度高于300℃之后,随着温度升高, 的平衡转化率增大,原因是
的平衡转化率增大,原因是___________ 。 时,向
时,向 恒容密闭容器中充入一定量的
恒容密闭容器中充入一定量的 和
和 ,使初始压强为
,使初始压强为 。在催化条件下发生反应:
。在催化条件下发生反应: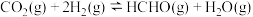 。反应达到平衡时,
。反应达到平衡时,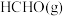 的分压
的分压 与起始时
与起始时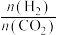 的关系如图所示。当起始时
的关系如图所示。当起始时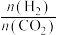
 ,反应达到平衡时,平衡常数
,反应达到平衡时,平衡常数
___________  (保留一位小数)。反应达到平衡后,若再向容器中加入
(保留一位小数)。反应达到平衡后,若再向容器中加入 和
和 ,使两者分压均增大
,使两者分压均增大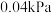 ,则达到新平衡时,
,则达到新平衡时, 的平衡转化率
的平衡转化率___________ (填“增大”“减小”或“不变”)。 的过程中发生如下反应:
的过程中发生如下反应:
I.
Ⅱ.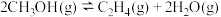
已知Arrhenius经验公式为 为活化能,
为活化能, 为速率常数,R和C为常数),反应I的Arrhenius经验公式的实验数据如图中直线a所示,则该反应的活化能
为速率常数,R和C为常数),反应I的Arrhenius经验公式的实验数据如图中直线a所示,则该反应的活化能
___________  。当改变外界条件时,实验数据如图中直线b所示,则实验可能改变的外界条件是
。当改变外界条件时,实验数据如图中直线b所示,则实验可能改变的外界条件是___________ 。
 资源化利用有助于实现“双碳目标”。选择不同条件,利用
资源化利用有助于实现“双碳目标”。选择不同条件,利用 和
和 可获得甲醇、甲醛等多种有机物。回答下列问题:
可获得甲醇、甲醛等多种有机物。回答下列问题:(1)工业上在
 催化下利用
催化下利用 发生如下反应I生产甲醇,同时伴有反应Ⅱ发生。
发生如下反应I生产甲醇,同时伴有反应Ⅱ发生。I.
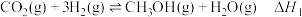
Ⅱ.
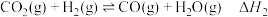
①已知反应过程中相关物质的相对能量如图所示,则反应I的


 的
的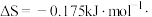
 ,则下列温度下该反应能自发进行的是
,则下列温度下该反应能自发进行的是A.5℃ B.10℃ C.50℃ D.500℃
③按照
 投料,在恒容密闭容器中进行反应,
投料,在恒容密闭容器中进行反应, 的平衡转化率随温度和压强的变化如图所示,则压强
的平衡转化率随温度和压强的变化如图所示,则压强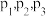 由大到小的顺序为
由大到小的顺序为 压强下,温度高于300℃之后,随着温度升高,
压强下,温度高于300℃之后,随着温度升高, 的平衡转化率增大,原因是
的平衡转化率增大,原因是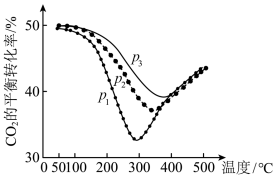
 时,向
时,向 恒容密闭容器中充入一定量的
恒容密闭容器中充入一定量的 和
和 ,使初始压强为
,使初始压强为 。在催化条件下发生反应:
。在催化条件下发生反应: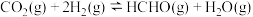 。反应达到平衡时,
。反应达到平衡时,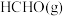 的分压
的分压 与起始时
与起始时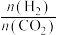 的关系如图所示。当起始时
的关系如图所示。当起始时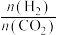
 ,反应达到平衡时,平衡常数
,反应达到平衡时,平衡常数
 (保留一位小数)。反应达到平衡后,若再向容器中加入
(保留一位小数)。反应达到平衡后,若再向容器中加入 和
和 ,使两者分压均增大
,使两者分压均增大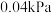 ,则达到新平衡时,
,则达到新平衡时, 的平衡转化率
的平衡转化率
 的过程中发生如下反应:
的过程中发生如下反应:I.

Ⅱ.
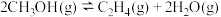
已知Arrhenius经验公式为
 为活化能,
为活化能, 为速率常数,R和C为常数),反应I的Arrhenius经验公式的实验数据如图中直线a所示,则该反应的活化能
为速率常数,R和C为常数),反应I的Arrhenius经验公式的实验数据如图中直线a所示,则该反应的活化能
 。当改变外界条件时,实验数据如图中直线b所示,则实验可能改变的外界条件是
。当改变外界条件时,实验数据如图中直线b所示,则实验可能改变的外界条件是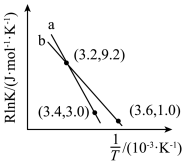
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】现有下列物质:①KOH溶液②NaClO溶液③KHSO4溶液④SO2气体⑤碘水⑥氨水⑦NH4HSO4溶液
(1)①的导电能力比⑥的______ (填“强”、“弱”或“无法判断”),理由是____________ 。
(2) 的③的
的③的
______ 。
(3)将少量④通入②中,发生反应的离子方程式为____________ 。
(4)为得到浓度较大的⑤,实验室在配制时,常加入KI,溶液中存在如下平衡: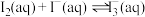 。向⑤中加入一定量的①,该平衡将
。向⑤中加入一定量的①,该平衡将______ (填“正向”或“逆向”)移动。
(5)浓度均为 的⑥⑦中,
的⑥⑦中, 的浓度由大到小的顺序是
的浓度由大到小的顺序是______ (填标号,下同),pH由大到小的顺序是______ 。
(1)①的导电能力比⑥的
(2)
 的③的
的③的
(3)将少量④通入②中,发生反应的离子方程式为
(4)为得到浓度较大的⑤,实验室在配制时,常加入KI,溶液中存在如下平衡:
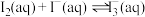 。向⑤中加入一定量的①,该平衡将
。向⑤中加入一定量的①,该平衡将(5)浓度均为
 的⑥⑦中,
的⑥⑦中, 的浓度由大到小的顺序是
的浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】弱电解质有许多如:醋酸、碳酸、氢氰酸、一水合氨等,已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如表:
(1)25℃时,pH相等的三种溶液①CH3COONa溶液、②Na2CO3溶液、③NaCN溶液,浓度由大到小的顺序为__ 。(填序号)
(2)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为__ 。
(3)将浓度为0.02mol/L的HCN与0.01mol/LNaOH溶液等体积混合,则混合溶液中c(H+)___ c(OH-)。(用“<”或“>”或“=”填空)
(4)常温下,向浓度为0.1mol•L-1、体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图中信息回答下列问题:
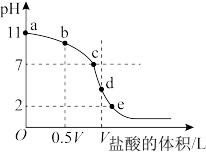
①该温度时NH3•H2O的电离常数K=___ 。
②比较b、c、d三点时的溶液中,由水电离出的c(H+)由大到小顺序为__ 。(填字母,下同)
③滴定时,由b点到c点的过程中,下列各选项中数值保持不变的__ 。
A.c(H+)•c(OH-) B.
C.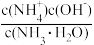 D.
D.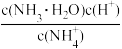
| 氢氰酸 | 碳酸 | 醋酸 |
| Ka=6.2×10-10 | Ka1=4.2×10-7Ka2=5.6×10-11 | Ka=1.7×10-5 |
(1)25℃时,pH相等的三种溶液①CH3COONa溶液、②Na2CO3溶液、③NaCN溶液,浓度由大到小的顺序为
(2)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为
(3)将浓度为0.02mol/L的HCN与0.01mol/LNaOH溶液等体积混合,则混合溶液中c(H+)
(4)常温下,向浓度为0.1mol•L-1、体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图中信息回答下列问题:

①该温度时NH3•H2O的电离常数K=
②比较b、c、d三点时的溶液中,由水电离出的c(H+)由大到小顺序为
③滴定时,由b点到c点的过程中,下列各选项中数值保持不变的
A.c(H+)•c(OH-) B.

C.
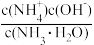 D.
D.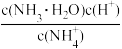
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】以含锌废渣(主要成分为 ,另含少量
,另含少量 、
、 、
、 等)为原料可生产草酸锌晶体(
等)为原料可生产草酸锌晶体(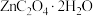 ,微溶于水),其工艺流程为:
,微溶于水),其工艺流程为:

常温时,部分金属离子开始沉淀及沉淀完全的 如下表所示(浓度
如下表所示(浓度 时可认为金属离子沉淀完全):
时可认为金属离子沉淀完全):
(1)酸浸时应适当增大盐酸的浓度,原因是_______ 和_______ 。
(2)氧化时反应的离子方程式为_______ 。
(3)为不引入杂质,物质X可以是_______ (填化学式)。
(4)“调 ”时应控制溶液的
”时应控制溶液的 范围是
范围是_______ 。
(5)将过滤II所得滤液与草酸钠 溶液按一定方式混合,可析出草酸锌晶体。
溶液按一定方式混合,可析出草酸锌晶体。
①滤液与草酸钠溶液混合方式不正确,会生成杂质沉淀。则滤液与草酸钠溶液的正确混合方式为_______ 。
②若将草酸钠换成草酸铵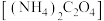 溶液,则不同的混合方式均不会生成杂质沉淀,原因是
溶液,则不同的混合方式均不会生成杂质沉淀,原因是_______ 。
(6)根据表格数据可知常温下,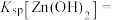
_______ 。
 ,另含少量
,另含少量 、
、 、
、 等)为原料可生产草酸锌晶体(
等)为原料可生产草酸锌晶体(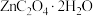 ,微溶于水),其工艺流程为:
,微溶于水),其工艺流程为:
常温时,部分金属离子开始沉淀及沉淀完全的
 如下表所示(浓度
如下表所示(浓度 时可认为金属离子沉淀完全):
时可认为金属离子沉淀完全):| 沉淀 | 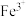 |  |  |  |
开始沉淀时的 |  | 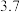 | 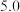 | 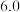 |
恰好完全沉淀时的 |  |  | 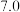 |  |
(1)酸浸时应适当增大盐酸的浓度,原因是
(2)氧化时反应的离子方程式为
(3)为不引入杂质,物质X可以是
(4)“调
 ”时应控制溶液的
”时应控制溶液的 范围是
范围是(5)将过滤II所得滤液与草酸钠
 溶液按一定方式混合,可析出草酸锌晶体。
溶液按一定方式混合,可析出草酸锌晶体。①滤液与草酸钠溶液混合方式不正确,会生成杂质沉淀。则滤液与草酸钠溶液的正确混合方式为
②若将草酸钠换成草酸铵
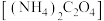 溶液,则不同的混合方式均不会生成杂质沉淀,原因是
溶液,则不同的混合方式均不会生成杂质沉淀,原因是(6)根据表格数据可知常温下,
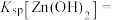
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】CO2资源化利用的方法之一是合成二甲醚(CH3OCH3)。
(1)CO2 催化加氢合成二甲醚的过程中主要发生下列反应:
反应I: CO2(g) + H2(g) CO(g) + H2O(g) ∆H= + 41.2 kJ·mol−1
CO(g) + H2O(g) ∆H= + 41.2 kJ·mol−1
反应II:2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g) ∆H = -122.5 kJ·mol−1
CH3OCH3(g) + 3H2O(g) ∆H = -122.5 kJ·mol−1
其中,反应II分以下①、②两步完成,请写出反应①的热化学方程式:①___________
② 2CH3OH(g) CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol−1
CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol−1
(2)二甲醚直接燃料电池具有启动快、效率高等优点。若电解质为碱性,二甲醚直接燃料电池的负极反应式为____________ 。以该电池为电源,用惰性电极电解饱和食盐水的化学方程式为________ 。
(3)反应I产生的CO,有人设想按下列反应除去:2CO(g) = 2C(s) + O2(g),已知该反应的∆H>0,简述该设想能否实现的依据_____________ 。
(4)CO2在自然界循环时可与CaCO3反应,Ksp(CaCO3)=2.8×10−9。 CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为5.6×10−5mol·L−1,则生成沉淀所需CaCl2溶液的最小浓度为________ 。
(1)CO2 催化加氢合成二甲醚的过程中主要发生下列反应:
反应I: CO2(g) + H2(g)
 CO(g) + H2O(g) ∆H= + 41.2 kJ·mol−1
CO(g) + H2O(g) ∆H= + 41.2 kJ·mol−1反应II:2CO2(g) + 6H2(g)
 CH3OCH3(g) + 3H2O(g) ∆H = -122.5 kJ·mol−1
CH3OCH3(g) + 3H2O(g) ∆H = -122.5 kJ·mol−1其中,反应II分以下①、②两步完成,请写出反应①的热化学方程式:①
② 2CH3OH(g)
 CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol−1
CH3OCH3(g) + H2O(g) ∆H = -23.5 kJ·mol−1(2)二甲醚直接燃料电池具有启动快、效率高等优点。若电解质为碱性,二甲醚直接燃料电池的负极反应式为
(3)反应I产生的CO,有人设想按下列反应除去:2CO(g) = 2C(s) + O2(g),已知该反应的∆H>0,简述该设想能否实现的依据
(4)CO2在自然界循环时可与CaCO3反应,Ksp(CaCO3)=2.8×10−9。 CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为5.6×10−5mol·L−1,则生成沉淀所需CaCl2溶液的最小浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】能源是人类生存和发展的重要支柱,化学在能源的开发与利用方面起着十分重要的作用。某学习小组按如下图所示装置探究化学能与电能的相互转化:
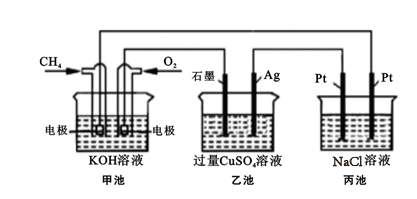
(1)甲池是_______ 装置,通入 气体的电极上的反应式为
气体的电极上的反应式为_______ 。乙池中 。移向
。移向_______ 电极(填“石墨”或“Ag”)。
(2)当甲池消耗标况下33.6LO2时,电解质KOH的物质的量变化_______ mol,乙池若要恢复电解前的状态则需要加入_______ (填化学式)。
(3)丙池中发生的电解反应的离子方程式为_______ 。

(1)甲池是
 气体的电极上的反应式为
气体的电极上的反应式为 。移向
。移向(2)当甲池消耗标况下33.6LO2时,电解质KOH的物质的量变化
(3)丙池中发生的电解反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】研究氮的固定具有重要意义。
(1)雷雨天气中发生自然固氮后,氮元素转化为硝酸盐而存在于土壤中。处于研究阶段的化学固氮新方法是N2在催化剂表面与水发生如下反应:
2N2(g)+6H2O(l)=4NH3(g)+3O2(g) △H K ①
已知:N2(g)+3H2(g)=2NH3(g) △H1=-92.4kJ·mol-1 K1②
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1 K2③
则△H=___ ;K=___ (用K1和K2表示)。
(2)四个容积为2L的密闭容器中,分别充入1molN2、3molH2O,在催化剂条件下进行反应①,反应3小时后,测得实验数据见表:
若第三组反应3h后已达平衡,与前三组相比,第四组中NH3生成量最小的原因最可能是(且80℃无其他副反应):___ 。第四组反应中以NH3表示的反应速率是___ 。
(3)美国化学家发明一种新型催化剂可以在常温下合成氨,将其附着在电池的正、负极上实现氮的电化学固定,其装置示意图如图所示:
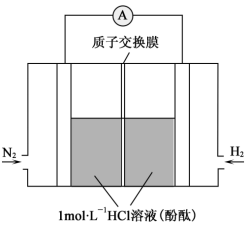
则开始阶段正极反应式为___ ;忽略过程中溶液体积变化,当电池中正极区溶液pH=7时,溶液中NH3·H2O的浓度为__ (Kb=2×10-5mol·L-1);当电池中正极区呈红色时,正极区溶液中c(NH )
)__ c(Cl-)(填“>”“=”“<”)。
(1)雷雨天气中发生自然固氮后,氮元素转化为硝酸盐而存在于土壤中。处于研究阶段的化学固氮新方法是N2在催化剂表面与水发生如下反应:
2N2(g)+6H2O(l)=4NH3(g)+3O2(g) △H K ①
已知:N2(g)+3H2(g)=2NH3(g) △H1=-92.4kJ·mol-1 K1②
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1 K2③
则△H=
(2)四个容积为2L的密闭容器中,分别充入1molN2、3molH2O,在催化剂条件下进行反应①,反应3小时后,测得实验数据见表:
| 序号 | 第一组 | 第二组 | 第三组 | 第四组 |
| t/℃ | 30 | 40 | 50 | 80 |
| NH3生成量/mol | 0.8 | 0.9 | 1.0 | 0.6 |
若第三组反应3h后已达平衡,与前三组相比,第四组中NH3生成量最小的原因最可能是(且80℃无其他副反应):
(3)美国化学家发明一种新型催化剂可以在常温下合成氨,将其附着在电池的正、负极上实现氮的电化学固定,其装置示意图如图所示:

则开始阶段正极反应式为
 )
)
您最近一年使用:0次



