Ⅰ.研究氮和碳的化合物对工业生产和防治污染有重要意义,回答下列问题:
(1)化学键键能数据如下:
合成氨反应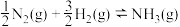 的活化能
的活化能 ,由此计算氨分解反应
,由此计算氨分解反应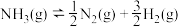 的活化能
的活化能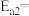
_______  。
。
(2)利用 的还原性可以消除氮氧化物的污染,其中除去
的还原性可以消除氮氧化物的污染,其中除去 的主要反应如下:
的主要反应如下:
 。某研究小组将
。某研究小组将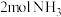 、
、 和一定量的
和一定量的 充入
充入 密闭容器中,在
密闭容器中,在 催化剂表面发生上述反应,
催化剂表面发生上述反应, 的转化率随温度变化的情况如图所示:
的转化率随温度变化的情况如图所示:
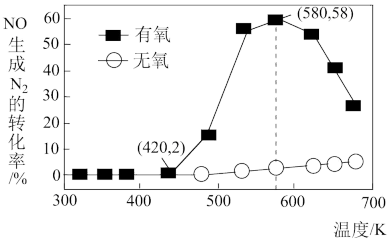
①温度从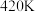 升高到
升高到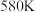 用时
用时 ,则此时段内
,则此时段内 的平均反应速率
的平均反应速率
_______ ;
②在有氧条件下,温度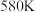 之后
之后 生成
生成 的转化率降低的原因可能是
的转化率降低的原因可能是_______ 。
Ⅱ. 目前有一种新的循环利用方案处理航天员呼吸产生的 ,是用
,是用 反应
反应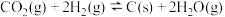
 ,再电解水实现
,再电解水实现 的循环利用。
的循环利用。
(3)若要此反应自发进行_______ (填“高温”或“低温”)更有利。
(4) 时,向体积为
时,向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入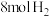 和
和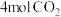 发生以上反应,若反应起始和平衡时温度相同(均为
发生以上反应,若反应起始和平衡时温度相同(均为 ),测得反应过程中压强随时间的变化如表所示:
),测得反应过程中压强随时间的变化如表所示:
① 时
时 反应的
反应的
_______ ( 为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
② 反应的速率方程:
反应的速率方程: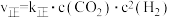 ,
,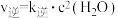 (k是速率常数,只与温度有关)。
(k是速率常数,只与温度有关)。
 时,
时,
_______ 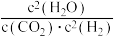 (填“
(填“ ”“
”“ ”或“
”或“ ”)
”)
(5)工业上常用氨水吸收二氧化硫,通过计算判断常温下 溶液的酸碱性并说明判断依据:
溶液的酸碱性并说明判断依据:_______ 。(已知: 的
的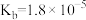 ;
; 的
的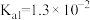 ,
,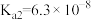 。)
。)
(1)化学键键能数据如下:
| 化学键 |  |  |  |
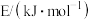 | 436 | 946 | 391 |
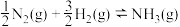 的活化能
的活化能 ,由此计算氨分解反应
,由此计算氨分解反应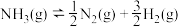 的活化能
的活化能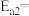
 。
。(2)利用
 的还原性可以消除氮氧化物的污染,其中除去
的还原性可以消除氮氧化物的污染,其中除去 的主要反应如下:
的主要反应如下:
 。某研究小组将
。某研究小组将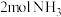 、
、 和一定量的
和一定量的 充入
充入 密闭容器中,在
密闭容器中,在 催化剂表面发生上述反应,
催化剂表面发生上述反应, 的转化率随温度变化的情况如图所示:
的转化率随温度变化的情况如图所示:
①温度从
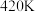 升高到
升高到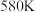 用时
用时 ,则此时段内
,则此时段内 的平均反应速率
的平均反应速率
②在有氧条件下,温度
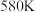 之后
之后 生成
生成 的转化率降低的原因可能是
的转化率降低的原因可能是Ⅱ. 目前有一种新的循环利用方案处理航天员呼吸产生的
 ,是用
,是用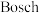 反应
反应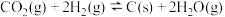
 ,再电解水实现
,再电解水实现 的循环利用。
的循环利用。(3)若要此反应自发进行
(4)
 时,向体积为
时,向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入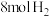 和
和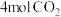 发生以上反应,若反应起始和平衡时温度相同(均为
发生以上反应,若反应起始和平衡时温度相同(均为 ),测得反应过程中压强随时间的变化如表所示:
),测得反应过程中压强随时间的变化如表所示:时间/ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强 |  |  | 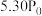 | 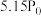 | 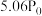 |  |  |
 时
时 反应的
反应的
 为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)②
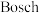 反应的速率方程:
反应的速率方程: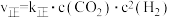 ,
,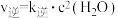 (k是速率常数,只与温度有关)。
(k是速率常数,只与温度有关)。 时,
时,
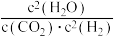 (填“
(填“ ”“
”“ ”或“
”或“ ”)
”)(5)工业上常用氨水吸收二氧化硫,通过计算判断常温下
 溶液的酸碱性并说明判断依据:
溶液的酸碱性并说明判断依据: 的
的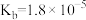 ;
; 的
的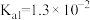 ,
,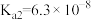 。)
。)
更新时间:2021-09-23 07:36:39
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮氧化物会造成环境污染,我国科学家正着力研究SCR技术(NH3选择性催化还原氮氧化物)对燃煤电厂烟气进行脱硝处理。
(1)氮氧化物(以NO为主)直接排放到空气中会形成硝酸型酸雨,反应的化学方程式为_______ 。
(2)NH3催化还原NO的化学方程式为_______ 。
(3)铁基催化剂在260~300℃范围内实现SCR技术的过程如下: ) 2与NO的物质的量之比为
) 2与NO的物质的量之比为_______ 。
② 适当增大催化剂用量可以明显加快脱硝速率,结合上述过程解释原因:_______ 。
③ 向反应体系中添加NH4NO3可显著提高NO脱除率。原因如下:
NO 与NO发生反应NO
与NO发生反应NO + NO = NO2 + NO
+ NO = NO2 + NO ;
;
NO2与NH 发生反应iii和反应iv转化为N2;
发生反应iii和反应iv转化为N2;
NO 与NH
与NH 发生反应
发生反应_______ (填离子方程式)转化为N2。
(4)相比于铁基催化剂,使用锰基催化剂(活性物质为MnO2)时,烟气中含有的SO2会明显降低NO脱除率。
① 推测SO2与MnO2会发生反应使催化剂失效,其化学方程式是_______ 。
② 持续通入含SO2的烟气。不同温度下,每隔1 h测定NO脱除率,结果如下:_______ 。
(1)氮氧化物(以NO为主)直接排放到空气中会形成硝酸型酸雨,反应的化学方程式为
(2)NH3催化还原NO的化学方程式为
(3)铁基催化剂在260~300℃范围内实现SCR技术的过程如下:
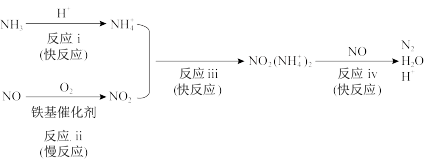
 ) 2与NO的物质的量之比为
) 2与NO的物质的量之比为② 适当增大催化剂用量可以明显加快脱硝速率,结合上述过程解释原因:
③ 向反应体系中添加NH4NO3可显著提高NO脱除率。原因如下:
NO
 与NO发生反应NO
与NO发生反应NO + NO = NO2 + NO
+ NO = NO2 + NO ;
;NO2与NH
 发生反应iii和反应iv转化为N2;
发生反应iii和反应iv转化为N2;NO
 与NH
与NH 发生反应
发生反应(4)相比于铁基催化剂,使用锰基催化剂(活性物质为MnO2)时,烟气中含有的SO2会明显降低NO脱除率。
① 推测SO2与MnO2会发生反应使催化剂失效,其化学方程式是
② 持续通入含SO2的烟气。不同温度下,每隔1 h测定NO脱除率,结果如下:

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】科学家积极探索新技术对CO2进行综合利用。请回答下列问题:
(1)已知: H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为1411.0kJ/mol,且H2O(g)=H2O(l)ΔH=-44.0kJ/mol,则CO2和H2反应生成乙烯和水蒸气的热化学方程式为____________ ,上述反应在__________ 下自发进行(填“高温”或“低温”)。
(2)乙烯是一种重要的气体燃料,可与氧气、熔融碳酸钠组成燃料电池。写出该燃料电池负极的电极反应式:_______________________ .
(3)在体积为1L的密闭容器中,充入3mol H2和1mol CO2,测得温度对CO2的平衡转化率和催化剂催化效率的影响如图所示。
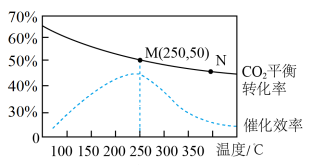
①平衡常数: KM__________ KN (填“>”“<”或“=”)。
②下列说法正确的是_________ (填序号)。
A.当混合气体密度不变时,说明反应达到平衡状态
B.当压强或n(H2)/n(CO2)不变时,均可证明反应已达平衡状态
C.当温度高于250℃时,因为催化剂的催化效率降低,所以平衡向逆反应方向移动
D.若将容器由“恒容”换为“恒压”,其他条件不变,则CO2的平衡转化率增大
③250℃时,将平衡后的混合气体(不考虑平衡移动) 通入300mL 3mol/L的NaOH溶液中充分反应,则所得溶液中所有离子的浓度大小关系为__________
④图中M点对应乙烯的质量分数为_____________ 。
(5)达平衡后,将容器体积瞬间扩大至2L并保持不变,平衡向_____ 移动(填“正向”“逆向”或“不”),容器内混合气体的平均相对分子质量______ (填“增大”“减小”或“不变”)。
(1)已知: H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为1411.0kJ/mol,且H2O(g)=H2O(l)ΔH=-44.0kJ/mol,则CO2和H2反应生成乙烯和水蒸气的热化学方程式为
(2)乙烯是一种重要的气体燃料,可与氧气、熔融碳酸钠组成燃料电池。写出该燃料电池负极的电极反应式:
(3)在体积为1L的密闭容器中,充入3mol H2和1mol CO2,测得温度对CO2的平衡转化率和催化剂催化效率的影响如图所示。

①平衡常数: KM
②下列说法正确的是
A.当混合气体密度不变时,说明反应达到平衡状态
B.当压强或n(H2)/n(CO2)不变时,均可证明反应已达平衡状态
C.当温度高于250℃时,因为催化剂的催化效率降低,所以平衡向逆反应方向移动
D.若将容器由“恒容”换为“恒压”,其他条件不变,则CO2的平衡转化率增大
③250℃时,将平衡后的混合气体(不考虑平衡移动) 通入300mL 3mol/L的NaOH溶液中充分反应,则所得溶液中所有离子的浓度大小关系为
④图中M点对应乙烯的质量分数为
(5)达平衡后,将容器体积瞬间扩大至2L并保持不变,平衡向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】以天然气为主要原料合成氨工艺流程大致分为三步:
第一步:原料气的制备。在Ni的催化作用下,天然气主要成分CH4发生如下反应:
①CH4(g)+H2O(g)⇌CO(g)+3H2(g)+Q1 (Q1<0);② CO(g)+H2O(g)⇌ CO2(g)+H2(g)+Q2
完成下列填空:
(1)天然气中的含硫化合物(如H2S、COS等)在反应前需除去的主要原因是___________ 。在恒温恒容条件下,欲提高反应①中CH4的反应速率和平衡转化率,可进一步采取的措施是(任写一个)___________ 。
(2)反应②平衡常数随温度变化如表:
a>b,则Q2___________ 0(选填“>”、“<”或“=”);若等物质的量的CO和H2O(g)发生该反应,进行到某一时刻,反应温度400℃,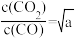 ,此时v正
,此时v正___________ v逆 (选填“>”、“<”或“=”)。
第二步:原料气的净化。在将氢氮原料气送入合成塔前必须净化,工业上用热K2CO3溶液吸收CO2。
(3)产物KHCO3溶液显___________ 性,理由是___________ 。用平衡移动原理解释吸收CO2的反应在加压下进行的原因。___________
第三步:原料气的压缩和氨的合成。将氢氮混合气压缩后在高温高压催化剂条件下合成氨气。
(4)若合成1 mol NH3(g)放热46.2kJ,画出合成氨反应的能量变化示意图________ 。

第一步:原料气的制备。在Ni的催化作用下,天然气主要成分CH4发生如下反应:
①CH4(g)+H2O(g)⇌CO(g)+3H2(g)+Q1 (Q1<0);② CO(g)+H2O(g)⇌ CO2(g)+H2(g)+Q2
完成下列填空:
(1)天然气中的含硫化合物(如H2S、COS等)在反应前需除去的主要原因是
(2)反应②平衡常数随温度变化如表:
| 温度/℃ | 500 | 800 |
| K | a | b |
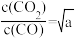 ,此时v正
,此时v正第二步:原料气的净化。在将氢氮原料气送入合成塔前必须净化,工业上用热K2CO3溶液吸收CO2。
(3)产物KHCO3溶液显
第三步:原料气的压缩和氨的合成。将氢氮混合气压缩后在高温高压催化剂条件下合成氨气。
(4)若合成1 mol NH3(g)放热46.2kJ,画出合成氨反应的能量变化示意图

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】(1)基态Fe2+的核外电子排布式为_______________ ,基态Ti3+的未成对电子有_____ 个。
(2)1mol[Ni(CO)4]2+中,配离子中含有σ键数目为________________
(3)有机物 HCHO的VSEPR构型为_______________ 。(填名称)
(4)抗坏血酸的分子结构如图所示,该分子中碳原子的轨道杂化类型为_________ 、____________

(5)向硫酸铜溶液中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,请根据实验现象写出有关反应的离子方程式______________ ; ________ 。
(6)已知:下列物质断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表:
则合成氨反应:N2(g)+3H2(g)=2NH3(g)△H=_________ kJ•mol﹣1
(2)1mol[Ni(CO)4]2+中,配离子中含有σ键数目为
(3)有机物 HCHO的VSEPR构型为
(4)抗坏血酸的分子结构如图所示,该分子中碳原子的轨道杂化类型为

(5)向硫酸铜溶液中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,请根据实验现象写出有关反应的离子方程式
(6)已知:下列物质断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如表:
| 共价键 | H﹣H | N﹣H | N≡N |
| 能量变化/kJ•mol﹣1 | 436 | 390.8 | 946 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】Ⅰ、甲醇既是重要的化工原料,又可作为燃料,利用CO和H2在催化剂作用下可合成甲醇(g)。
(1)已知相关的化学键键能数据如下:
合成甲醇(g)的热化学方程式为______________________________________________ 。
(2)500K、101KPa条件下,反应过程中测得n(CO)、n(H2)、n(CH3OH)随时间t变化的关系如图甲所示。现保持其它条件不变,起始只改变温度,在改变的这个温度下反应至t1时刻,此时n(H2)比图象中的值大,那么该温度可能是________ 。
A、700K B、373K C、以上均不对

(3)在一容积可变的密闭容器中充入1 mol CO和2 mol H2,发生反应并达到平衡,CO的平衡转化率随温度(T)和压强(P)的变化曲线如图乙所示。P1、P2的大小关系为________ ;A、B、C三点的平衡常数(K)大小关系为______________________ 。
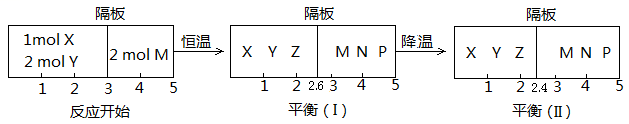
Ⅱ、可逆反应:①X(g)+2Y(g)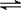 2Z(g);②2M(g)
2Z(g);②2M(g)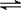 N(g)+P(g),分别在密闭容器的两个反应室中进行,反应室之间放有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g),分别在密闭容器的两个反应室中进行,反应室之间放有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
(4)反应①的正反应ΔH______ 0(填“>”或“<”)。
(5)反应开始时体系的压强与达平衡(Ⅰ)时体系的压强之比为_________ (用分数表示)。
(6)在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数(Ⅰ)______ (Ⅱ)。
A、大于B、小于C、等于D、无法确定
(1)已知相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
合成甲醇(g)的热化学方程式为
(2)500K、101KPa条件下,反应过程中测得n(CO)、n(H2)、n(CH3OH)随时间t变化的关系如图甲所示。现保持其它条件不变,起始只改变温度,在改变的这个温度下反应至t1时刻,此时n(H2)比图象中的值大,那么该温度可能是
A、700K B、373K C、以上均不对

(3)在一容积可变的密闭容器中充入1 mol CO和2 mol H2,发生反应并达到平衡,CO的平衡转化率随温度(T)和压强(P)的变化曲线如图乙所示。P1、P2的大小关系为
Ⅱ、可逆反应:①X(g)+2Y(g)
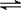 2Z(g);②2M(g)
2Z(g);②2M(g)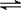 N(g)+P(g),分别在密闭容器的两个反应室中进行,反应室之间放有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g),分别在密闭容器的两个反应室中进行,反应室之间放有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
(4)反应①的正反应ΔH
(5)反应开始时体系的压强与达平衡(Ⅰ)时体系的压强之比为
(6)在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数(Ⅰ)
A、大于B、小于C、等于D、无法确定
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氨的用途十分广泛,是制造硝酸和氮肥的重要原料。
(1)工业合成氨中,合成塔中每产生2 molNH3,放出92.2kJ热量。
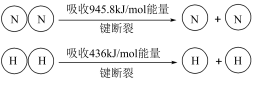
1 mol N-H键断裂吸收的能量约等于_______ kJ
(2)一定条件下,在恒温恒容的密闭容器中充入等物质的量N2和H2发生反应生成NH3,下列状态能说明反应达到平衡的是_______(填标号)。
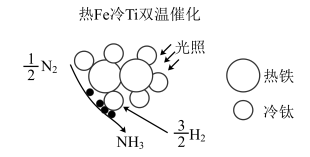
(3)近期我国科学家为了解决合成氨反应速率和平衡产率的矛盾,选择使用Fe-TiO2-xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2-xHy的温度为415℃)。结合图示解释该双催化剂的工作原理是_______ 。
(4)已知合成氨反应的速率方程为:ν=kcα(N2)cβ(H2)c-1(NH3),在合成氨过程中,需要不断分离出氨,可能的原因为_______
_______ 。
(5)以氨为原料生产尿素的方程式为2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g)。
①为进一步提高NH3的平衡转化率,下列措施能达到目的的是_______ (填标号)。
A.增大CO2的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂
②尿素的合成分两步进行:a.2NH3(g)+CO2(g)⇌NH2COONH4(1) ΔH=-117 kJ/mol
b.NH2COONH4(1)⇌CO(NH2)2(1)+H2O(g) ΔH=+15 kJ/mol,第一步反应速率快,可判断活化能较大的是_______ (填“第一步”或“第二步”)。
③某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应:2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g),反应过程中混合气体中NH3的体积分数如下图所示。
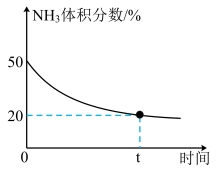
实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数Kp=_______ (已知:分压=总压×体积分数)。
(1)工业合成氨中,合成塔中每产生2 molNH3,放出92.2kJ热量。

1 mol N-H键断裂吸收的能量约等于
(2)一定条件下,在恒温恒容的密闭容器中充入等物质的量N2和H2发生反应生成NH3,下列状态能说明反应达到平衡的是_______(填标号)。
| A.容器内压强不变 | B.N2的体积分数不变 |
| C.气体的密度不再改变 | D.V正(N2)=3V逆(H2) |

(4)已知合成氨反应的速率方程为:ν=kcα(N2)cβ(H2)c-1(NH3),在合成氨过程中,需要不断分离出氨,可能的原因为
(5)以氨为原料生产尿素的方程式为2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g)。
①为进一步提高NH3的平衡转化率,下列措施能达到目的的是
A.增大CO2的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂
②尿素的合成分两步进行:a.2NH3(g)+CO2(g)⇌NH2COONH4(1) ΔH=-117 kJ/mol
b.NH2COONH4(1)⇌CO(NH2)2(1)+H2O(g) ΔH=+15 kJ/mol,第一步反应速率快,可判断活化能较大的是
③某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应:2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g),反应过程中混合气体中NH3的体积分数如下图所示。

实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数Kp=
您最近一年使用:0次
【推荐1】在恒容密闭容器中通入CH4与CO2,使其物质的量浓度均为1.0 mol·L-1,在一定条件下发生反应:CO2(g)+CH4(g)⇌2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图所示:
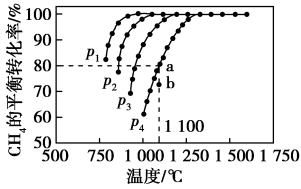
则:(1)该反应的ΔH________ 0(填“<”“=”或“>”)。
(2)压强p1、p2、p3、p4由大到小的顺序为______________ 。压强为p4时,在b点:v(正)________ v(逆)(填“<”“=”或“>”)。
(3)对于气相反应,用某组分(B)的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数(记作Kp),则该反应的平衡常数的表达式Kp=________ ;如果p4=0.36 MPa,求a点的平衡常数Kp=________ (保留3位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)为探究速率与浓度的关系,该实验中,根据相关实验数据,粗略绘制出了2条速率—浓度关系曲线:v正~c(CH4)和v逆~c(CO)。
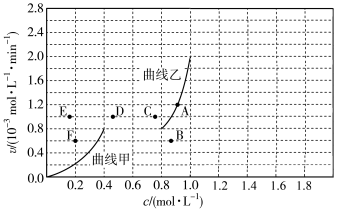
则:①与曲线v正~c(CH4)相对应的是上图中曲线______ (填“甲”或“乙”)。
②当降低到某一温度时,反应重新达到平衡,相应的平衡点分别为________ (填字母)。

则:(1)该反应的ΔH
(2)压强p1、p2、p3、p4由大到小的顺序为
(3)对于气相反应,用某组分(B)的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数(记作Kp),则该反应的平衡常数的表达式Kp=
(4)为探究速率与浓度的关系,该实验中,根据相关实验数据,粗略绘制出了2条速率—浓度关系曲线:v正~c(CH4)和v逆~c(CO)。

则:①与曲线v正~c(CH4)相对应的是上图中曲线
②当降低到某一温度时,反应重新达到平衡,相应的平衡点分别为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】含铁锌精矿(主要含有ZnS和FeS)焙烧可以得到 ,
, 通常作为锌渣处理,一种回收利用锌渣制取ZnSO4溶液和FeOOH的流程如下图所示。
通常作为锌渣处理,一种回收利用锌渣制取ZnSO4溶液和FeOOH的流程如下图所示。

(1)基态Fe2+的电子排布式为_______ 。
(2)写出由含铁锌精矿焙烧得到ZnFe2O4的化学方程式:_______ 。
(3)锌渣浸出时发生如下反应:
反应1: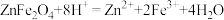
反应2: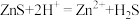
反应3: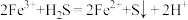
①已知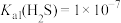 、
、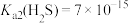 、
、 ,则反应2的平衡常数K=
,则反应2的平衡常数K=_______ 。
②浸出过程中,溶液中Fe2+、Fe3+、总Fe的浓度随时间的变化关系如图所示。0~50min时间内,溶液中Fe3+的浓度随时间延长而逐渐增大的原因是_______ 。

(4)水热时需控制溶液pH在4~4.5之间,温度为80℃,写出水热反应中Fe2+所发生反应的离子方程式:_______ 。
 ,
, 通常作为锌渣处理,一种回收利用锌渣制取ZnSO4溶液和FeOOH的流程如下图所示。
通常作为锌渣处理,一种回收利用锌渣制取ZnSO4溶液和FeOOH的流程如下图所示。
(1)基态Fe2+的电子排布式为
(2)写出由含铁锌精矿焙烧得到ZnFe2O4的化学方程式:
(3)锌渣浸出时发生如下反应:
反应1:
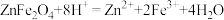
反应2:
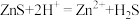
反应3:
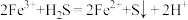
①已知
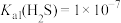 、
、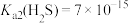 、
、 ,则反应2的平衡常数K=
,则反应2的平衡常数K=②浸出过程中,溶液中Fe2+、Fe3+、总Fe的浓度随时间的变化关系如图所示。0~50min时间内,溶液中Fe3+的浓度随时间延长而逐渐增大的原因是

(4)水热时需控制溶液pH在4~4.5之间,温度为80℃,写出水热反应中Fe2+所发生反应的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】大气中的部分碘源于O3对海水中I-的氧化。将O3持续通入NaI酸性溶液中进行模拟研究。
(1)O3将I-氧化成I2的过程可发生如下反应:
②IO-(aq)+H+(aq) HOI(aq)
HOI(aq) 
③HOI(aq)+I-(aq)+H+(aq) I2(aq)+H2O(l)
I2(aq)+H2O(l) 
写出O3将I-氧化的总反应的热化学方程式为:____________ 。
(2)在溶液中存在化学平衡I2(aq)+I-(aq) I3-(aq),在反应的整个过程中I3-物质的量浓度变化情况是
I3-(aq),在反应的整个过程中I3-物质的量浓度变化情况是_______ 。
(3)为探究温度对I2(aq)+I-(aq) I3-(aq)
I3-(aq) 反应的影响。在某温度T1下,将NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与I-反应反应)。在t时刻,测得容器中I2(g)的浓度,然后分别在温度为T2、T3、T4、T5下,保证其他初始实验条件不变,重复上述实验,经过相同时间测得I2(g)的浓度。得到趋势图(如下图一所示)
反应的影响。在某温度T1下,将NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与I-反应反应)。在t时刻,测得容器中I2(g)的浓度,然后分别在温度为T2、T3、T4、T5下,保证其他初始实验条件不变,重复上述实验,经过相同时间测得I2(g)的浓度。得到趋势图(如下图一所示)

①若在T3时,容器中无O3,T4~T5温度区间容器内I2(g)浓度呈现如图一所示的变化趋势。则
______ 0(填“>0”、“=”或“<”);该条件下在温度T4时,将一定量的I2投入0.20
 溶液中充分反应,测得I-浓度变化如图二所示。在t2时刻,将该反应体系温度从T4上升到T5,并维持该温度。请在图二中画出t2时刻后溶液中I-浓度变化总趋势曲线
溶液中充分反应,测得I-浓度变化如图二所示。在t2时刻,将该反应体系温度从T4上升到T5,并维持该温度。请在图二中画出t2时刻后溶液中I-浓度变化总趋势曲线______ 。
②由I2(aq)+I-(aq) I3-(aq),在水溶液中难以准确测定I2的浓度。本实验将一定量的I2投入0.20
I3-(aq),在水溶液中难以准确测定I2的浓度。本实验将一定量的I2投入0.20
 溶液中充分反应,并在溶液中加入一定量的CCl4充分萃取后,测出CCl4中I2的浓度为0.11
溶液中充分反应,并在溶液中加入一定量的CCl4充分萃取后,测出CCl4中I2的浓度为0.11 ,此时溶液中I-为0.10
,此时溶液中I-为0.10 。查阅资料可知,在一定温度下,发生萃取后I2在CCl4中的浓度与I2在水中的浓度之比为一常数
。查阅资料可知,在一定温度下,发生萃取后I2在CCl4中的浓度与I2在水中的浓度之比为一常数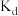 (已知
(已知 时,
时,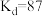 )。根据上述实验相关数据,计算温度为
)。根据上述实验相关数据,计算温度为 时,I2(aq)+I-(aq)
时,I2(aq)+I-(aq)  I3-(aq)反应的平衡常数K的值为
I3-(aq)反应的平衡常数K的值为___________ 。
③已知该反应中υ正=k正·c(I2)·c(I-),υ逆=k逆·c(I3-),其中 、
、 均为速率常数,则
均为速率常数,则 为
为________________ 。(以K和 表示)。
表示)。
(4)优质的锂电池可用于心脏起搏器延续患者的生命。它的正极材料是聚2-乙烯吡啶(简写为P2VP)和I2的复合物,电解质是固态薄膜状碘化锂。总反应为: P2VP·nI2+2Li=P2VP·(n-1)I2+2LiI。该电池的正极反应式为________ 。
(1)O3将I-氧化成I2的过程可发生如下反应:
①I-(aq)+O3(g)=IO-(aq)+O2(g) 
②IO-(aq)+H+(aq)
 HOI(aq)
HOI(aq) 
③HOI(aq)+I-(aq)+H+(aq)
 I2(aq)+H2O(l)
I2(aq)+H2O(l) 
写出O3将I-氧化的总反应的热化学方程式为:
(2)在溶液中存在化学平衡I2(aq)+I-(aq)
 I3-(aq),在反应的整个过程中I3-物质的量浓度变化情况是
I3-(aq),在反应的整个过程中I3-物质的量浓度变化情况是(3)为探究温度对I2(aq)+I-(aq)
 I3-(aq)
I3-(aq) 反应的影响。在某温度T1下,将NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与I-反应反应)。在t时刻,测得容器中I2(g)的浓度,然后分别在温度为T2、T3、T4、T5下,保证其他初始实验条件不变,重复上述实验,经过相同时间测得I2(g)的浓度。得到趋势图(如下图一所示)
反应的影响。在某温度T1下,将NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与I-反应反应)。在t时刻,测得容器中I2(g)的浓度,然后分别在温度为T2、T3、T4、T5下,保证其他初始实验条件不变,重复上述实验,经过相同时间测得I2(g)的浓度。得到趋势图(如下图一所示)
①若在T3时,容器中无O3,T4~T5温度区间容器内I2(g)浓度呈现如图一所示的变化趋势。则


 溶液中充分反应,测得I-浓度变化如图二所示。在t2时刻,将该反应体系温度从T4上升到T5,并维持该温度。请在图二中画出t2时刻后溶液中I-浓度变化总趋势曲线
溶液中充分反应,测得I-浓度变化如图二所示。在t2时刻,将该反应体系温度从T4上升到T5,并维持该温度。请在图二中画出t2时刻后溶液中I-浓度变化总趋势曲线②由I2(aq)+I-(aq)
 I3-(aq),在水溶液中难以准确测定I2的浓度。本实验将一定量的I2投入0.20
I3-(aq),在水溶液中难以准确测定I2的浓度。本实验将一定量的I2投入0.20
 溶液中充分反应,并在溶液中加入一定量的CCl4充分萃取后,测出CCl4中I2的浓度为0.11
溶液中充分反应,并在溶液中加入一定量的CCl4充分萃取后,测出CCl4中I2的浓度为0.11 ,此时溶液中I-为0.10
,此时溶液中I-为0.10 。查阅资料可知,在一定温度下,发生萃取后I2在CCl4中的浓度与I2在水中的浓度之比为一常数
。查阅资料可知,在一定温度下,发生萃取后I2在CCl4中的浓度与I2在水中的浓度之比为一常数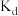 (已知
(已知 时,
时,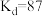 )。根据上述实验相关数据,计算温度为
)。根据上述实验相关数据,计算温度为 时,I2(aq)+I-(aq)
时,I2(aq)+I-(aq)  I3-(aq)反应的平衡常数K的值为
I3-(aq)反应的平衡常数K的值为③已知该反应中υ正=k正·c(I2)·c(I-),υ逆=k逆·c(I3-),其中
 、
、 均为速率常数,则
均为速率常数,则 为
为 表示)。
表示)。(4)优质的锂电池可用于心脏起搏器延续患者的生命。它的正极材料是聚2-乙烯吡啶(简写为P2VP)和I2的复合物,电解质是固态薄膜状碘化锂。总反应为: P2VP·nI2+2Li=P2VP·(n-1)I2+2LiI。该电池的正极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题。
(1)氯化铵的水溶液显弱酸性,其原因为___________ (用离子方程式表示),若加入少量的明矾,对溶液中的 的水解起
的水解起___________ 作用(填“抑制”或“促进”)。 的氨水中加入少量的
的氨水中加入少量的 固体,溶液的pOH
固体,溶液的pOH___________ (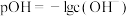 填“升高”或“降低”)。
填“升高”或“降低”)。
(2)25℃,两种酸的电离平衡常数如下表。
①物质的量浓度均为0.1mol/L的四种溶液:
a. b.
b. c.NaClO d.
c.NaClO d.
 由大到小的顺序为
由大到小的顺序为________ (用编号填写)。
②根据上表数据判断,下列离子方程式正确的是________ 。
A. (过量)
(过量)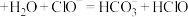
B. (过量)
(过量)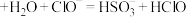
C. (少量)
(少量)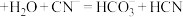
D. (少量)
(少量)
E. (少量)
(少量)
③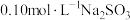 溶液中
溶液中 、
、 、
、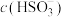 由大到小的顺序为
由大到小的顺序为________ 。
④25℃时,NaClO与HClO的混合溶液,若 ,则溶液中pH=
,则溶液中pH=________ (已知1g2=0.3,1g3=0.5)。
⑤25℃时,若向 溶液中加入少量的
溶液中加入少量的 ,则溶液中发生的离子反应为
,则溶液中发生的离子反应为________ 。
(1)氯化铵的水溶液显弱酸性,其原因为
 的水解起
的水解起 的氨水中加入少量的
的氨水中加入少量的 固体,溶液的pOH
固体,溶液的pOH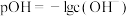 填“升高”或“降低”)。
填“升高”或“降低”)。(2)25℃,两种酸的电离平衡常数如下表。
| 化学式 |  |  | HCN | HClO |  |
| 电离常数 |  |   | 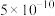 |  | 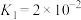 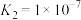 |
a.
 b.
b. c.NaClO d.
c.NaClO d.
 由大到小的顺序为
由大到小的顺序为②根据上表数据判断,下列离子方程式正确的是
A.
 (过量)
(过量)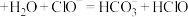
B.
 (过量)
(过量)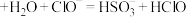
C.
 (少量)
(少量)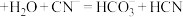
D.
 (少量)
(少量)
E.
 (少量)
(少量)
③
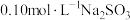 溶液中
溶液中 、
、 、
、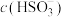 由大到小的顺序为
由大到小的顺序为④25℃时,NaClO与HClO的混合溶液,若
 ,则溶液中pH=
,则溶液中pH=⑤25℃时,若向
 溶液中加入少量的
溶液中加入少量的 ,则溶液中发生的离子反应为
,则溶液中发生的离子反应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】硫及其化合物在生产生活中具有广泛的应用,根据所学知识,回答下列问题:
(1) 溶液显
溶液显_______________ 性,判断的理由是_______________ (用离子方程式表示),若将该溶液蒸干,最终所得固体为_______________ (填化学式)。
(2) 的
的 溶液中,各离子浓度由大到小的关系为
溶液中,各离子浓度由大到小的关系为_______________ 。
(3)常温下,在某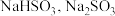 混合溶液中,部分含硫微粒的物质的量分数随
混合溶液中,部分含硫微粒的物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数
的水解平衡常数
_______________ 。
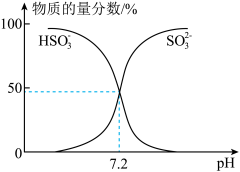
(4)常温下,某浓度的 溶液中:
溶液中:
① 为
为_______________ (填“强”或“弱”)电解质。
②往 溶液中滴加少量的
溶液中滴加少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______________ ,此时所得溶液的
_______________ (填“变大”、“变小”或“不变”)。
(5)在 的
的 溶液中加入等体积
溶液中加入等体积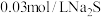 溶液,有黑色
溶液,有黑色 沉淀生成,反应后溶液中
沉淀生成,反应后溶液中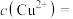
_______________ [已知: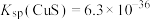 ](忽略溶液混合时体积的变化)。
](忽略溶液混合时体积的变化)。
(1)
 溶液显
溶液显(2)
 的
的 溶液中,各离子浓度由大到小的关系为
溶液中,各离子浓度由大到小的关系为(3)常温下,在某
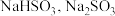 混合溶液中,部分含硫微粒的物质的量分数随
混合溶液中,部分含硫微粒的物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数
的水解平衡常数

(4)常温下,某浓度的
 溶液中:
溶液中:①
 为
为②往
 溶液中滴加少量的
溶液中滴加少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
(5)在
 的
的 溶液中加入等体积
溶液中加入等体积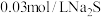 溶液,有黑色
溶液,有黑色 沉淀生成,反应后溶液中
沉淀生成,反应后溶液中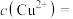
 ](忽略溶液混合时体积的变化)。
](忽略溶液混合时体积的变化)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。
(1)高温下,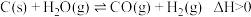 ,反应的化学平衡常数表达式
,反应的化学平衡常数表达式
_______ ,该反应随温度升高,K值_______ (填“增大”、“减小”或“不变”)。
(2)已知常温下部分弱电解质的电离平衡常数如下表:
①常温下,物质的量浓度相同的三种溶液①NaF溶液;②NaClO溶液;③ 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是_______ (填序号)
②0.1mol/L的NaClO溶液和0.1mol/L的 溶液中,
溶液中,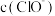
_______ 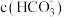 (填“>”“<”或“=”)
(填“>”“<”或“=”)
③常温下,0.1mol/L的氨水和0.1mol/L的 溶液等体积混合,判断混合溶液的酸碱性
溶液等体积混合,判断混合溶液的酸碱性_______ (填“酸性”“碱性”“中性”)
(3)已知几种离子开始沉淀时溶液的pH如下表所示:
当向含有相同浓度的 、
、 、
、 的溶液中滴加氢氧化钠溶液时,
的溶液中滴加氢氧化钠溶液时,_______ (填离子符号)先沉淀;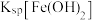
_______ (填“>”“=”或“<”)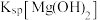 ;要使
;要使 的硫酸铜溶液中铜离子沉淀较完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠使溶液
的硫酸铜溶液中铜离子沉淀较完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠使溶液
_______ 。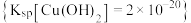
(1)高温下,
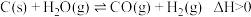 ,反应的化学平衡常数表达式
,反应的化学平衡常数表达式
(2)已知常温下部分弱电解质的电离平衡常数如下表:
| 化学式 | HF | HClO |  |  |
| 电离常数 | 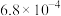 | 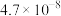 |  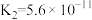 | 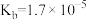 |
①常温下,物质的量浓度相同的三种溶液①NaF溶液;②NaClO溶液;③
 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是②0.1mol/L的NaClO溶液和0.1mol/L的
 溶液中,
溶液中,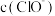
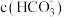 (填“>”“<”或“=”)
(填“>”“<”或“=”)③常温下,0.1mol/L的氨水和0.1mol/L的
 溶液等体积混合,判断混合溶液的酸碱性
溶液等体积混合,判断混合溶液的酸碱性(3)已知几种离子开始沉淀时溶液的pH如下表所示:
| 离子 |  |  |  |
| pH | 7.6 | 5.2 | 10.4 |
当向含有相同浓度的
 、
、 、
、 的溶液中滴加氢氧化钠溶液时,
的溶液中滴加氢氧化钠溶液时,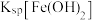
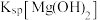 ;要使
;要使 的硫酸铜溶液中铜离子沉淀较完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠使溶液
的硫酸铜溶液中铜离子沉淀较完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠使溶液
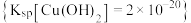
您最近一年使用:0次



